BK
TPHCM
TS.LÊ HOÀNG NGHIÊM
2
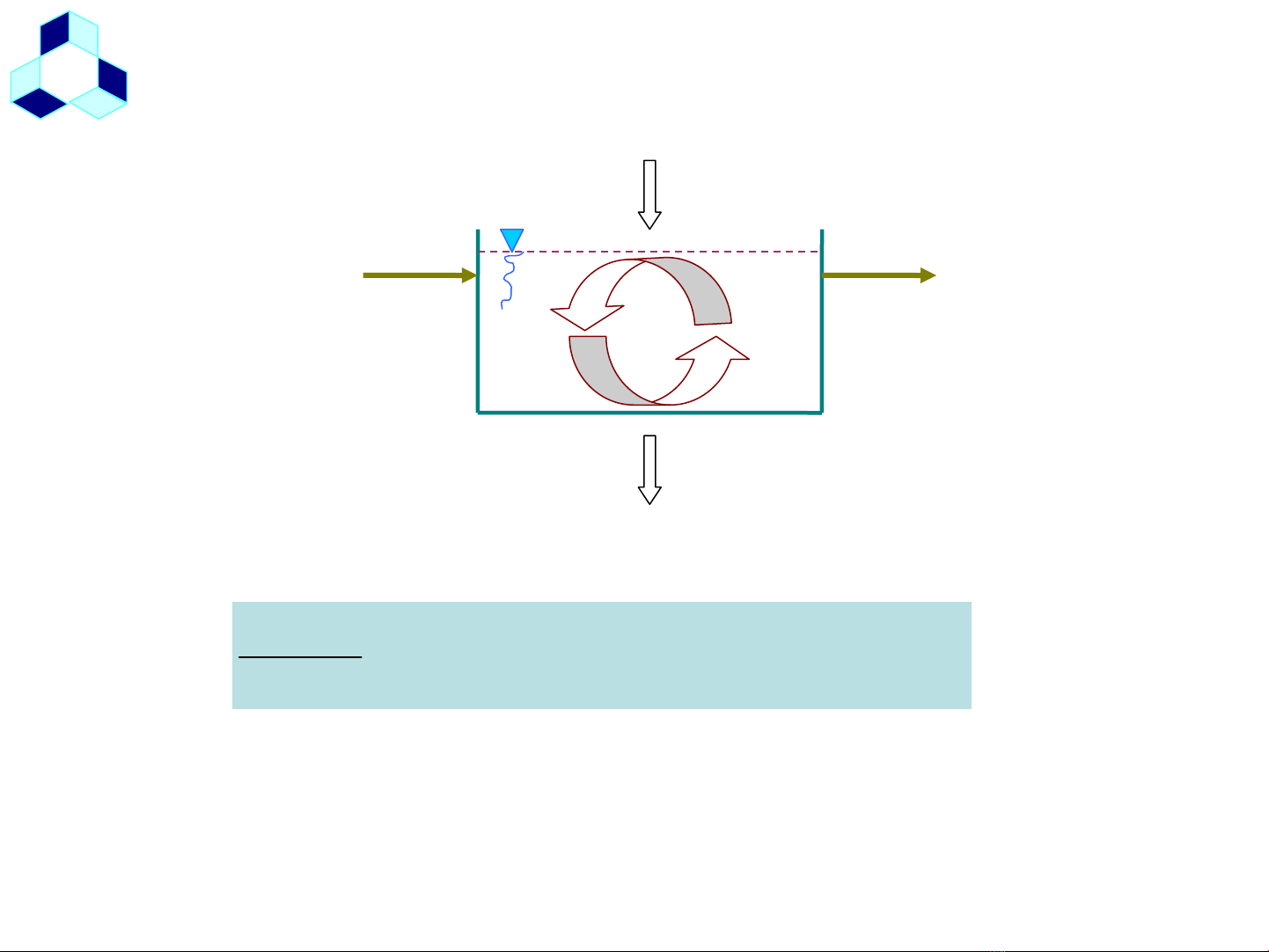
2.1. CAÂN BAÈNG VAÄT CHAÁT
öùng phaûnchaát Vaät ra ñichaát Vaät - vaøo ñichaát Vaät soaùt kieåm tích theå trong beân luõy tíchchaát Vaät
chuyeån Vaän
±= 444444344444421
Qout
, C
V, C
Qin
, Cin
rp
, V
rc
, V
Sinh
ra
Tiêu
thụ
Vào
(input) Ra (output)
).(....
).( 12
0VrVrCQCQ
dt
V
C
d
cp −+−=
C –
nồng
đô ta
cchấttạithời
điểmnhất
định
(ML-3); C0
–nồng
đô đầuvàocủacơ
chất(ML
-3)
V –
thê tıch
củaphản
ứng
(hòa
trộn
hoàn
toàn) (L3); Q –
lưulương
(L3T-1); t –
thơi gian
(T);
rp
–tôc đô phan ứng
cua sảnphâm (ML-3T-1); rc
–tôc đô phan ứng
cua chât tiêu
thu (ML-3T-1)
BK
TPHCM
TS.LÊ HOÀNG NGHIÊM
3
2.1. CAÂN BAÈNG VAÄT CHAÁT
Phương
trình
(2.1) có
thể
triểnkhaivế
trái
và
biểudiễn
dướcdạng
sau
:
Thể
tích
bể
phản
ứng
thường
là
cốđịnh
(dV/dt
= 0) ta
có:
).(...... 22
0VrVrCQCQ
dt
dC
V
dt
dV
Ccp ++−=+
).(..... 32
0VrVrCQCQ
dt
d
C
Vcp −+−=
).(....
).( 12
0VrVrCQCQ
dt
V
C
d
cp −+−=

BK
TPHCM
TS.LÊ HOÀNG NGHIÊM
4
2.1. CAÂN BAÈNG VAÄT CHAÁT
Trạng
thái
ổn
định
và
trạng
thái
động
học
Mô hình toán họccủahệthống có thểxây dựng ởhai điềukiện
trạng thái:
9Trạng thái ổnđịnh (steady state); và
9Trạng thái động học(dynamic state)
Trạng thái ổnđịnh (steady state) là trạng thái không có tích lũy
vậtchấttronghệthống, dC/dt = 0, nghĩalànồng độ củachấtphản
ứng trong hệthống là hằng số. Phương trình (2.3) trởthành:
0 = Q.C0
–
Q.C + rp
.V
–
rc
.V
(2.4)
Trạng thái động học (dynamic state) là trạng thái có sựtích lũy
khốilượng vậtchấttronghệthống. Vì vậy, dC/dt =/ 0. Nồng độ của
chấtphảnứng thay đổitheothờigianvà có thểtăng hay giảm.
BK
TPHCM
TS.LÊ HOÀNG NGHIÊM
5
2.1. CAÂN BAÈNG VAÄT CHAÁT
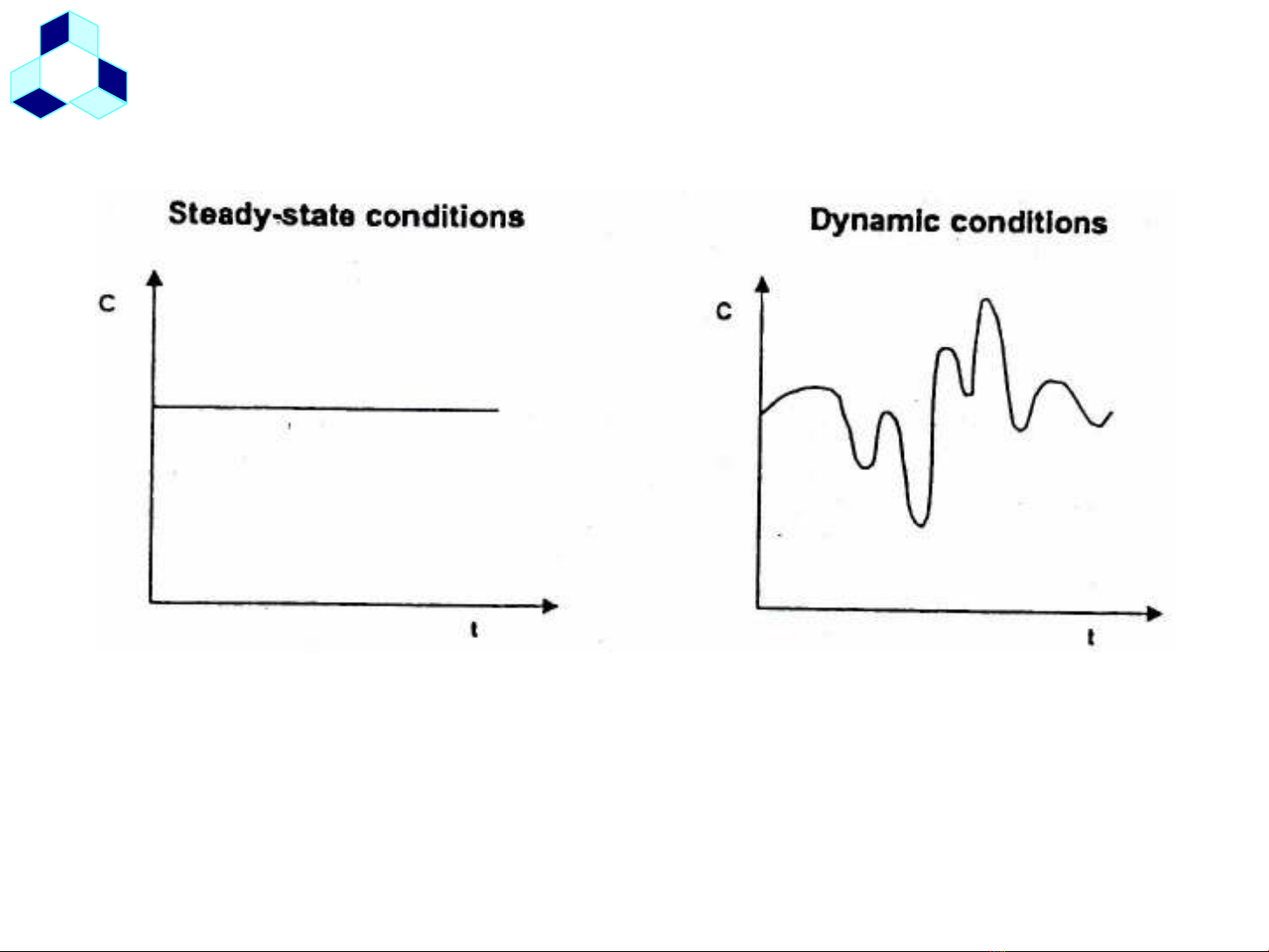
Hình
vẽ
: Minh họasự
biến
đổinồng
độ
theo
thờigiancủa
điềukiệntrạng
thái
ổn
định
và
trạng
thái
động
học.















![Đề cương ôn tập Giáo dục môi trường cho học sinh tiểu học [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20251212/tambang1205/135x160/621768815662.jpg)











