8/18/2014
ĐỀ CƯƠNG ÔN THI
HẾT HỌC PHẦN
MÔN: Kiểm Nghiệm Thú Sản
Học kỳ III năm học 2013-2014
Thach Van Manh
Website: sites.google.com/site/thachvanmanh
Mail: thachvanmanh@gmail.com
Tel : +84983912823
Vietnam National University of Agriculture
Faculty of Veterinary Medicine
Thạch Văn Mạnh TYD-K55
1
A. Phần thực hành
Kiểm nghiệm trứng
a. Quan sát : độ sạch bẩn, độ nguyên vẹn...
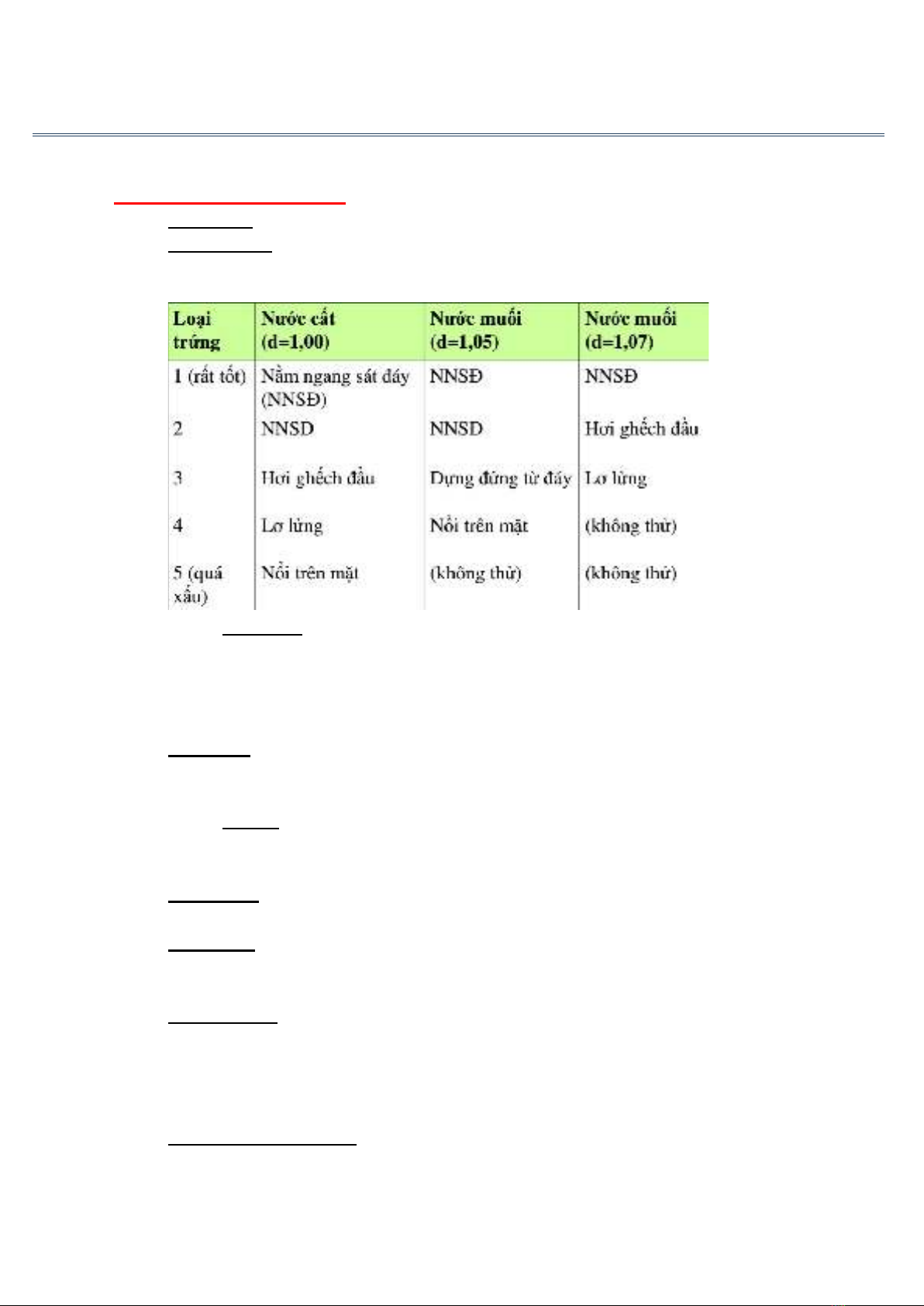
b. Đo tỷ trọng : thả trứng lần lượt vào 3 bình dung dịch có tỷ trọng 1,00 ; 1,05 ; 1,07 để
đánh giá trạng thái của quả trứng trong đó.
- Đo tỉ trọng
Nhận xét
- Trứng giống: lấy loại 1
- Trứng tươi xuất khẩu: lấy loại 1 và 2
- Trứng làm thực phẩm: lấy loại 1, 2 và 3 nhưng có kỳ hạn
- Trứng loại 4 phải dùng ngay
c. Soi trứng
- Là khâu qtrọng nhất trong KN. Có thể dùng ÁS mặt trời, đèn dầu, đèn điện...
yêu cầu AS tập trung và chiếu trực tiếp.
Xđịnh: độ lớn buồng hơi, vị trí và sự di động của lòng đỏ, phát hiện dị vật
phân loại trứng theo độ lớn buồng hơi. Độ lớn càng ít thì trứng càng mới
và ngược lại.
d. Cân trứng
- Xác định P1, P10
e. Lắc trứng
- (dùng với trứng ăn ngay): Với trứng có buồng hơi quá to và lòng trắng bị loãng
khi lắc có tiếng óc ách.
f. Xem cấu tạo
- Thẩm định lại kquả của các khâu nói trên.
Dùng dao chặt ở 1/3đầu to quả trứng, bóc vỏ vàđổ nhẹ nhàng ra đĩa lồng.
Quan sát: tính chất lòng trắng (đặc), dây chằng, chỉ số lòng đỏ, đĩa phôi,
tìm dị vật.
g. Cảm quan trứng luộc

Thạch Văn Mạnh TYD-K55
2
quan sát bên ngoài hộp ktra sự phồng méo, han rỉ. Ktra bột trứng về
màu sắc, mùi, vị, tìm dị vật. Bột trứng tốt có màu vàng nhạt, mịn đều, mùi
thơm và 0 có chất lạ.
Xác định độ tươi của thịt gia súc
1. Cảm quan
2. Đo pH nước chiết thịt
- Nguyên lý: Trong thịt có sự biến đổi pH,
• Mới mổ pH=7,2 – 7,4
• Q/trình toan hóa: tích tụ a.lactic và H3PO4 pH giảm tới 5,8-6,2
• Thịt hư hỏng: pH lại tăng đến trung tính hay kiềm yếu (tùy mức độ).
• Cách làm (thực tập): so màu, pH met
3. Phản ứng sa lắng protit
- Nguyên lý: Một số Pr (globulin) 0 tan trong mtrường a-xít hay trung tính
mà chỉ tan trong mtrường kiềm hay muối. Thịt hư hỏng tạo ra nhiều muối
(NH4+) và mtrường kiềm Pr tan nhiều hơn. Dùng muối k/loại nặng
(CuSO4 1-5%) hay a-xít yếu (CH3COOH)để phát hiện Pr hòa tan.
- Cách làm: Lấy vào 2 ống nghiệm mỗi ống 2 ml nước chiết thịt của mỗi
- mẫu tương ứng. Nhỏ 5 giọt CuSO4 (1 – 5%), để yên 30 phút, quan sát:
+ P/ư(+): dung dịch vẩn đục sau đó lắng cặn ở đáy
+ P/ư(-): dung dịch bình thường
4. Phản ứng Nessler (xđịnh NH3)
- Nguyên lý: NH3 là SP phân giải của thịt, thịt càng bị phân giải nhiều thì hàm
lượng NH3 càng cao. NH3 + dd Nessler (HgCl2 + KI + KOH) NH2Hg2IO

Thạch Văn Mạnh TYD-K55
3
(Iodua dimercua ammonium/ ammonium dimercuric iodide màu vàng) + KCl +
H2O
- Cách làm: Lấy vào 2 ống nghiệm mỗi ống 2 ml nước chiết thịt của mỗi mẫu
tương ứng. Nhỏ từ từ từng giọtdung dịch Nessler (tối đa 10 giọt) đến khi xuất
hiện màu vàng thì dừng lại. Màu xuất hiện càng sớm NH3 càng nhiều và ngược
lại.
5. Phản ứng Benzidine (thử hoạt tính men peroxydaza)
- Nguyên lý: gsúc khỏe, giết mổ đúng quy cách, thịt còn tươi thì hlượng
peroxydase nhiều, hoạt tính cao. Và ngược lại, gsúc ốm yếu, giết mổ 0 đúng
quy cách (vchuyển đến giết mổ ngay) hay thịt đã ôi thì lượng peroxydase ít, hoạt
tính thấp.
- Cách làm: Lấy vào 2 ống nghiệm mỗi ống 2 ml nước chiết thịt của mỗi mẫu
tương ứng. Nhỏ5 giọt Benzidine + 2 giọt H2O2. Căn cứ vào sự chuyển màu
(xanh --> nâu) và bọt khí (O2) để đánh giá hoạt tính men peroxydaza. Chuyển
màu càng nhanh, bọt khí càng nhiều hoạt tính men càng mạnh.
6. Phản ứng Eber
- Nguyên lý: NH3+ HCl NH4Cl tạo lớp sương mờ trắng xquanh miếng thịt
(quan sát trên nền đen).
- Ddịch Eber gồm: HCl nguyên chất 1V + cồn 96% 3V + Ete 1V)
- Để định lượng NH3 có thể dùng ppháp chưng cất lôi cuốn rồi chuẩn độ
7. Xác định H2S
- Nguyên lý: Sự pgiải a-xít amin có S tạo ra H2S
- H2S + Pb(CH3COO)2(NaOH xúc tác) PbS kết tủa đen + 2CH3COOH
P/ưnày cóđộ tin cậy thấp vì chỉ khi thịt ôi rất rõ, lượng H2S nhiều mới cho
kquả (+)
- Cách làm: Cắt nhỏvào ống nghiệm khoảng 10-20 g thịt. Dùng miếng giấy đã tẩm
sẵn axetát chì cho vào ống nghiệm, nút chặt, để yên 30 phút và quan sát đánh giá
hiện tượng. Màu miếng giấy càng đậm thì H2S càng nhiều.
Kiểm nghiệm sữa tươi
1. Kiểm tra độ sạch bẩn
a. Cơ sở khoa học
- Lọc sữa qua bông hay giấy lọc và ktra
– Sữa loại 1: 0 có cặn cơ giới
– Sữa loại 2: có vết bẩn hoặc có ít cặn
– Sữa loại 3: có nhiều cặn cơ giới kích thước khác nhau.
b. Cách tiến hành
- Lọc 350 – 400 ml sữa qua bông (hay giấy lọc) vào ống đong 500 ml, lấy bông ra
- hộp lồng và kiểm tra cặn:
- Sữa loại 1: không có cặn cơgiới

Thạch Văn Mạnh TYD-K55
4
- Sữa loại 2: có vết bẩn hoặc có ít cặn
- Sữa loại 3: có nhiều cặn cơgiới kích thước khác nhau.
2. Đo đậm độ
a. Cơ sở khoa học
• Dùng đậm độ kế (Lactodensimetre), lấy chuẩn ở 20 độ C, khi nđộ >20 độ C
+0,0002 vào đậm độ/1 độ C, và ngược lại nđộ <20 độ C thì cứ mỗi độ -
0,0002.
• Sữa bquản bằng K2Cr2O7 trừ đi 0,0007. Yêu cầu nđộ khi đo d nằm
trong khoảng 15-25 độ C
• Giả mạo: pha thêm nước d giảm (10% nước d giảm 0,003 (30A); lấy bớt mỡ
d tăng...
b. Cách tiến hành
- Dùng đậm độ kế sữa (Lactodensimeter), lấy chuẩn ở 20 độC, khi nhiệt độ>20 độ
C thì cứ mỗi độ cộng thêm 0,0002 vào đậm độ, và ngược lại khi nhiệt độ<20 độ
C thì cứ mỗi độ trừ đi 0,0002. Thả nhẹ nhàng đậm độ kế vào cốc đong 500 ml có
sữa (từ bước trước), đến khi đứng yên thì đọc kết quả. Bề mặt sữa đến đâu thì đọc
ở đó.
- Đo đậm độ để đánh giá chất lượng và bản chất thật của sữa (phát hiện giảmạo).
Khi pha thêm nước đậm độgiảm, khi lấy bớt bơ đậm độ tăng (sữa bò bình thường
có đậm độ1,026 – 1,033).
3. Xác định độ axít tổng số(oT - độ Thorner)
a. Cơ sở khoa học
- Độ a xít tổng số (chung; có thể chuẩn độ):
• Dùng để đgiá độ tươi của sữa.
• Là số ml ddịch NaOH hoặc KOH cần thiết để trung hòa độ chua của 100 ml sữa.
• Tùy theo nồng độ NaOH/KOH mà có cách gọi khác nhau.
• Do các muối phốt phát, casein, CO2...





![Bài giảng Kiểm nghiệm thú sản [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2022/20221111/bbichhien0210/135x160/3261668128890.jpg)




![Giáo trình Thực tập cuối khoá Thú y (CĐ/TC) - Trường Cao đẳng nghề Đồng Tháp [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2022/20221003/namkimcham25/135x160/6031664764495.jpg)









![Giáo trình Dinh dưỡng và thức ăn chăn nuôi (Nghề Thú y) - Trường Trung cấp nghề Trà Vinh [Mới Nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/68591778489721.jpg)





