
Së GD&§T H¶i Phßng
---------------------
K× thi chän Häc Sinh Giái líp 11
M«n: ho¸ häc (b¶ng B)
N¨m häc 2003 - 2004
===============
(Thêi gian lµm bµi: 180 phót)
Bµi 1( 3,0 ®iÓm)
1- Hoµn thµnh c¸c ph¬ng tr×nh ph¶n øng sau (d¹ng ph©n tö) , ghi cÆp oxi ho¸-khö cña ph¶n
øng.
a) K2Cr2O7 + ....
Cr(OH)3 + S + NH3
b) Cr2O72- + ....
Cr2(SO4)3 + KI3 + ....
2- XÐt kh¶ n¨ng hoµ tan Ag kim lo¹i trong dung dÞch chøa NH3 vµ NH4ClO4 ë ®iÒu kiÖn chuÈn
trong 2 trêng hîp sau:
a) Kh«ng cã kh«ng khÝ
b) Cã kh«ng khÝ
Cho : 2 2
0 0
/
/
0,81 ; 1, 23
O H O
Ag Ag
E v E v
Ag+ + 2NH3
Ag(NH3)2+ K1 = 107,24
NH4+
NH3 + H+ K2 = 10-9,24
Bµi 2: (3,0 ®iÓm)
1- Trén lÉn 30 ml dung dÞch HClO4 víi 50 ml dung dÞch Ca(OH)2 (pH = 12,5) ®îc dung dÞch
A cã pH = 10 . TÝnh nång ®é ban ®Çu cña dung dÞch HClO4.
2- Ion H2PO2- trong m«i trêng baz¬ cã thÓ khö ®îc Zn2+ trong dung dÞch1M thµnh Zn
kh«ng? T¬ng tù xÐt víi trêng hîp dung dÞch Cr3+ 1M.
Cho:
2
4
( ) 2 4
Zn OH e Zn OH
E0 = -1,22v
Cr(OH)3 + 3e
Cr + 3OH- E0 = -1,30v
H2PO2- + 3OH-
HPO32- + 2H2O + 2e E0 = 1,6 v
Bµi 3: (3,0 ®iÓm)
1- S¾p xÕp c¸c ph©n tö sau theo chiÒu ®é ph©n cùc ph©n tö gi¶m dÇn, gi¶i thÝch.
CH2=CH-Cl ; CH3-CH2-Cl ; CH2=CH-CH=O ; CH3-CH=O
(A) (B) (C) (D)
2- ViÕt ph¬ng tr×nh ph¶n øng nitro ho¸:
a) 1-Brom-3-clobenzen
b) 1-Clo-3-metylbenzen
Víi s¶n phÈm cã tØ lÖ % lín nhÊt.
3- ViÕt ph¬ng tr×nh ph¶n øng sau theo tû lÖ sè mol chÊt tham gia ph¶n øng 1:1 vµ 1:3
OH
+ HBr
Bµi 4: (3,0 ®iÓm)
Dung dÞch b·o hoµ Mg(OH)2 cã pH = 10,5
1- TÝnh tÝch sè tan Tt cña Mg(OH)2.
2- TÝnh ®é tan S cña Mg(OH)2 trong dung dÞch NaOH 0,01M
3- Trén 10 g Mg(OH)2 víi 100 ml dung dÞch HCl 0,1M tÝnh pH cña dung dÞch khi c©n b»ng
®îc thiÕt lËp.
Bµi 5: (3,0 ®iÓm)
Hçn hîp (A) gåm 2 hi®rocacbon thÓ khÝ ë ®iÒu kiÖn thêng cã c«ng thøc tæng qu¸t
kh¸c nhau. §Ó ®èt ch¸y hoµn toµn 1 thÓ tÝch (A) cÇn 5,25 thÓ tÝch O2 cïng ®iÒu kiÖn, sau ph¶n
øng thu ®îc sè mol CO2 vµ sè mol H2O b»ng nhau.
X¸c ®Þnh c«ng thøc ph©n tö hai hi®rocacbon. ViÕt c¸c ®ång ph©n cña 2 hi®rocacbon.
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.

Së GD&§T H¶i Phßng
---------------------
híng dÉn chÊm ®Ò thi Häc Sinh Giái líp 11
M«n: ho¸ häc (B¶ng B )
N¨m häc 2003 - 2004
===============
Bµi 1:(3,0 ®iÓm)
1- (1,5 ®iÓm)
a) K2Cr2O7 + 3(NH4)2S + H2O
2Cr(OH)3 + 3S + 6NH3 + 2KOH
CÆp oxi ho¸ - khö: Cr2O72-/Cr(OH)3 vµ S/S2-
b) K2Cr2O7 + 7H2SO4 + 9KI
Cr2(SO4)3 + 3KI3 + 7H2O + 4K2SO4
CÆp oxi ho¸-khö: Cr2O72-/2Cr3+ vµ I3-/3I-.
2- (1,5 ®iÓm)
a) Khi kh«ng cã kh«ng khÝ cã c¸c c©n b»ng:
NH4+
NH3 + H+ K2 = 10-9,24
Ag
Ag+ + e K3 =
0,8.1
0,059
10
2H+ +2e
H2 K4 =1
Ag+ + 2NH3
Ag(NH3)2+ K1 = 107,24
Nh©n hÖ sè thÝch hîp cho c¸c c©n b»ng råi tæ hîp l¹i ta cã c©n b»ng:
2Ag + 2NH3 + 2NH4+
2Ag(NH3)2+ + H2 K = (K2)2.(K3)2.K4 .(K1)2
K = 10-31,12 << => Ag rÊt khã hoµ tan.
b) Khi cã mÆt kh«ng khÝ cã c¸c c©n b»ng:
NH4+
NH3 + H+ K2 = 10-9,24
Ag
Ag+ + e K3 =
0,8.1
0,059
10
O2 + 4H+ + 4e
2H2O K4 =
4.1,23
0,059
10
Ag+ + 2NH3
Ag(NH3)2+ K1 = 107,24
Nh©n hÖ sè thÝch hîp cho c¸c c©n b»ng råi tæ hîp l¹i ta cã c©n b»ng:
4Ag + O2 + 4NH3 + 4NH4+
4Ag(NH3)2+ + 2H2O K = (K2)4.(K3)4.K4 .(K1)4
K = 1021,16. Ph¶n øng x¶y ra dÔ rµng.
Bµi 2: (3,0 ®iÓm)
1- (1,0 ®iÓm)
HClO4
H+ + ClO4-
Ca(OH)
Ca2+ + 2OH-
H+ + OH-
H2O
pH dd Ca(OH)2 = 12,5 =>
12,5
10H
=>
OH
= 10-1,5
Sau khi trén (cha ph¶n øng)
1,5
.30 10 .50
;
80 80
C
H OH
Sau ph¶n øng dd cã pH = 10 nªn
OH
=10-4
VËy:
1,5
4
.30 10 .50
10
80 80
C
=> C =
4
HClO
C= 0,0524(M)
2- (2,0 ®iÓm)
+ Víi dd Zn2+ 1M:
2
4
( ) 2 4
Zn OH e Zn OH
E0 = -1,22v
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
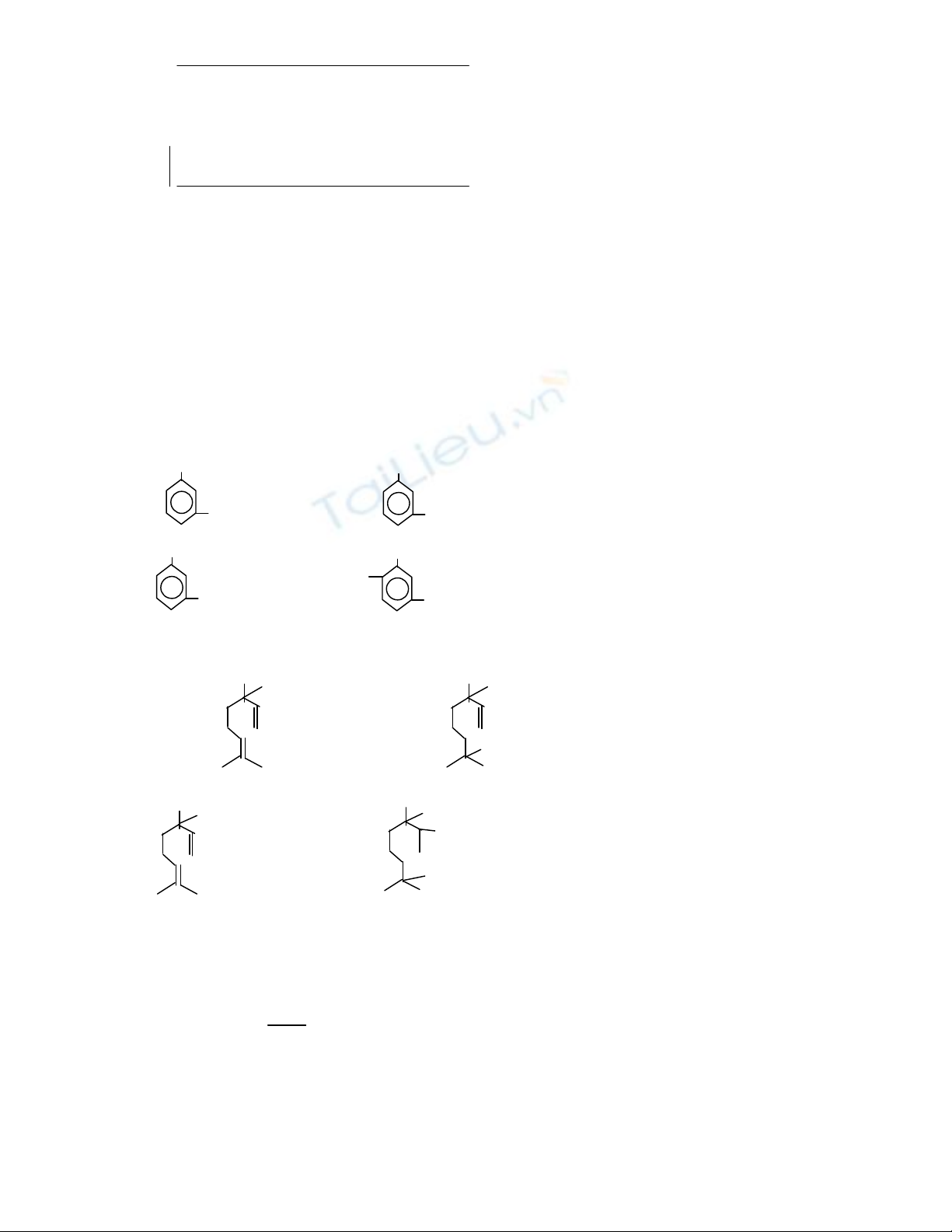
H2PO2- + 3OH-
HPO32- + 2H2O + 2e E0 = 1,6 v
H2PO2- +
2
4
( )
Zn OH
Zn + HPO32- + 2H2O + OH- E0P¦ = 0,38v >0
Ph¶n øng cã thÓ x¶y ra.
+ Víi dd Cr3+ 1M:
2x Cr(OH)3 + 3e
Cr + 3OH- E0 = -1,30v
3x H2PO2- + 3OH-
HPO32- + 2H2O + 2e E0 = 1,6 v
3H2PO2- + 2Cr(OH)3 + 3OH-
3HPO3- + 2Cr + 6H2O E0P¦ = 0,3v > 0
Ph¶n øng cã thÓ x¶y ra.
Bµi 3: (3,0 ®iÓm)
1- (1,0 ®iÓm)
- §é ph©n cùc ph©n tö: (C) > (D) >(B)>(A)
- (C) cã sù liªn hîp ph©n tö lµm t¨ng kh¶ n¨ng chuyÓn e vÒ nguyªn tö oxi (
=2,95D).
- (D) cã -I ; - C lµm t¨ng ®é ph©n cùc ph©n tö (
=2,60D).
- B cã -I (
=2,02D).
-(A) cã sù chuyÓn cÆp e cha liªn kÕt cña Cl vµo nèi ®«i lµm gi¶m m¹nh ®é ph©n cùc ph©n tö :
-I ; +C (
=1,44D).
2-ViÕt ph¬ng tr×nh ph¶n øng nitro ho¸: (1,0 ®iÓm)
a)
Cl Cl
Br + HNO3
Br + H2O
NO2
b) CH3 CH3
O2N
Cl + HNO3
Cl + H2O
3- (1,0 ®iÓm) OH OH
+ HBr 1:1
Br
OH Br
Br
+3 HBr 1:3
+ H2O
Br
Bµi 4( 3,0 ®iÓm)
1- (1,0 ®iÓm)
Mg(OH)2
Mg2+ + 2OH-
S 2S
2S = 10-3,5 => S =
3,5
10
2
=> Tt = S.(2S)2 = 4S3 = 10-10,8
2- (1,0 ®iÓm) Mg(OH)2
Mg2+ + 2OH-
S 2S+ 0,01
Tt = S.(2S+0,01)2 = 10-10,8 .v× Tt<< => S << 0,01 => 10-4S = 10-10,8 => S =10-6,8
3-( 1,0 ®iÓm)
Mg(OH)2 + 2HCl
MgCl2 + 2H2O
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
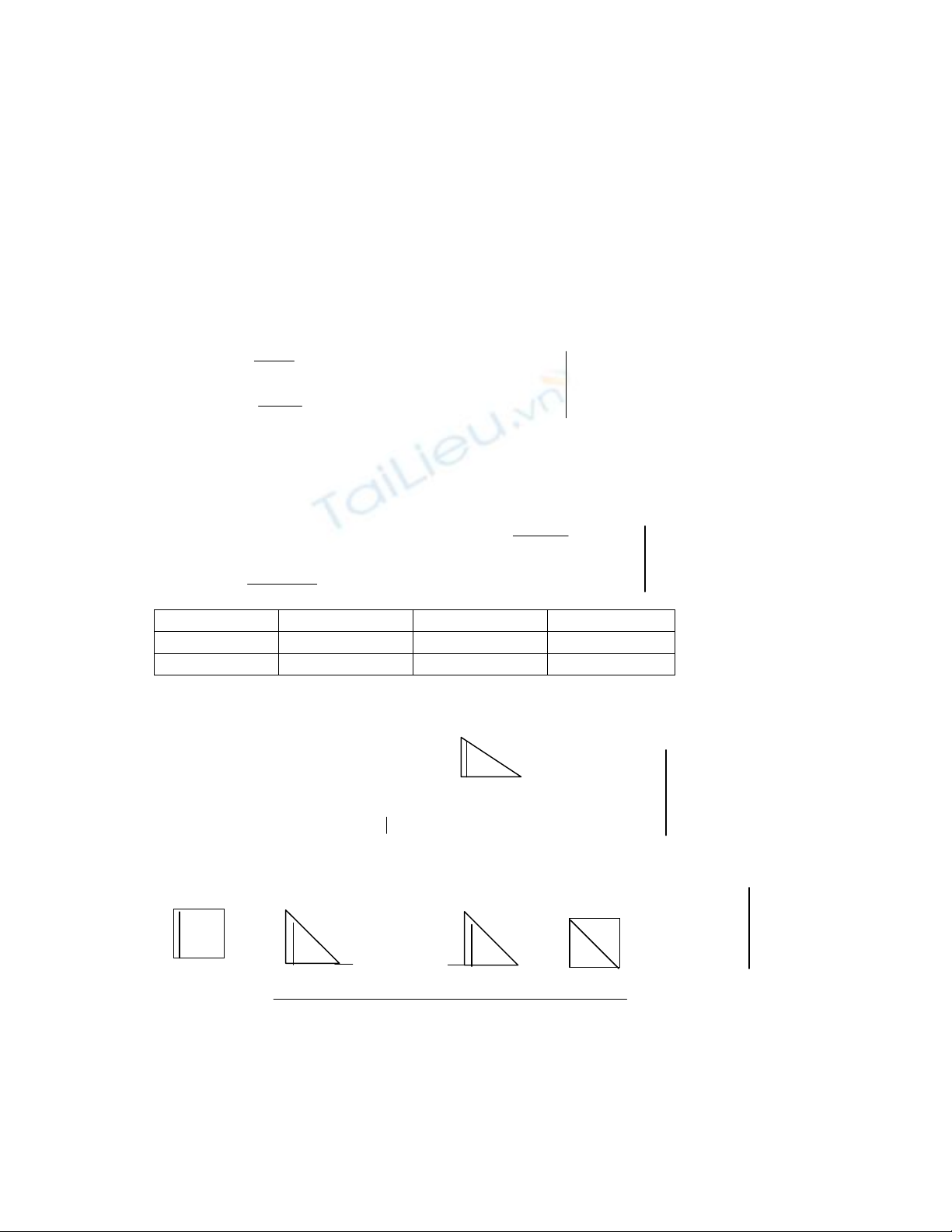
B® 0,1724 mol 0,01 mol
P 0,005 0,01 0,005
Cßn 0,1674 0 0,005
Mg(OH)2
Mg2+ + 2OH-
0,05
0,05 + S 2S
Tt = (0,05+S)(2S)2 = 10-10,8 chÊp nhËn S << 0,05 => 0,2S2 = 10-10,8
S = 10-5,05 =>
OH
= 2S = 2.10-5,05 =>
H
=10-9,25 => pH = 9,25
Bµi 5:(3,0 ®iÓm)
V× (A) + O2
nCO2 + nH2O . MÆt kh¸c 2 hi®rocacbon trong (A) kh«ng cïng
CTTQ nªn 2 hi®rocacbon cã c«ng thøc TQ: CnH2n+2 vµ CmH2m-2 .
Ph¶n øng ®èt ch¸y:
CnH2n+2 +
3 1
2
n
O2
nCO2 + (n+1)H2O (0,5 ®iÓm)
CmH2m-2 +
3 1
2
m
O2
mCO2 + (m-1)H2O
Gäi sè mol CnH2n+2 lµ a ; sè mol CmH2m-2 lµ b (0,5 ®iÓm)
na+mb =na+mb + a-b => a=b
Gi¶ sö sè mol CO2 sinh ra = sè mol H2O sinh ra = 1mol, theo ®Çu bµi cã
Khèi lîng O2 = 32+16 = 48 (g) ; (A) = 12+2 = 14 (g)
V× thÓ tÝch A = 1/5,25 thÓ tÝch oxi => sè mol A =
48
32.5, 25
(0,5 ®iÓm)
(14n+2+14m-2) 48
2.32.5, 25
=14 => n+m =7 ®/k: 4
m
2
m 2 3 4
n 5 4 3
Hi®rocacbon
lo¹i C3H4 ; C4H10 C4H6 ; C3H8
C«ng thøc ph©n tö 2 hi®rocacbon lµ C3H4 vµ C4H10 hoÆc C4H6 ; C3H8 ( 0,5 ®iÓm)
C¸c ®ång ph©n:
C3H4: CH3 -C
CH ; CH2=C=CH2 ;
( 0,5 ®iÓm)
C4H10: CH3-CH2-CH2-CH3 ; CH3-CH -CH3
CH3
C3H8: CH3-CH2-CH3
C4H6 : CH3-CH2-C
CH ; CH3-C
C -CH3 ; CH2=C=CH-CH3 ; CH2=CH-CH=CH2
( 0,5 ®iÓm)
CH3 H3C
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.










![Đề Thi Học Sinh Giỏi Hóa 11 Thành Phố Đà Nẵng [2005-2006] - Tuyển Tập Đề Thi](https://cdn.tailieu.vn/images/document/thumbnail/2010/20100913/trungtran5/135x160/_hoahoc11_thihsgthanhphodanang_2006_2007_4413.jpg)











![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



