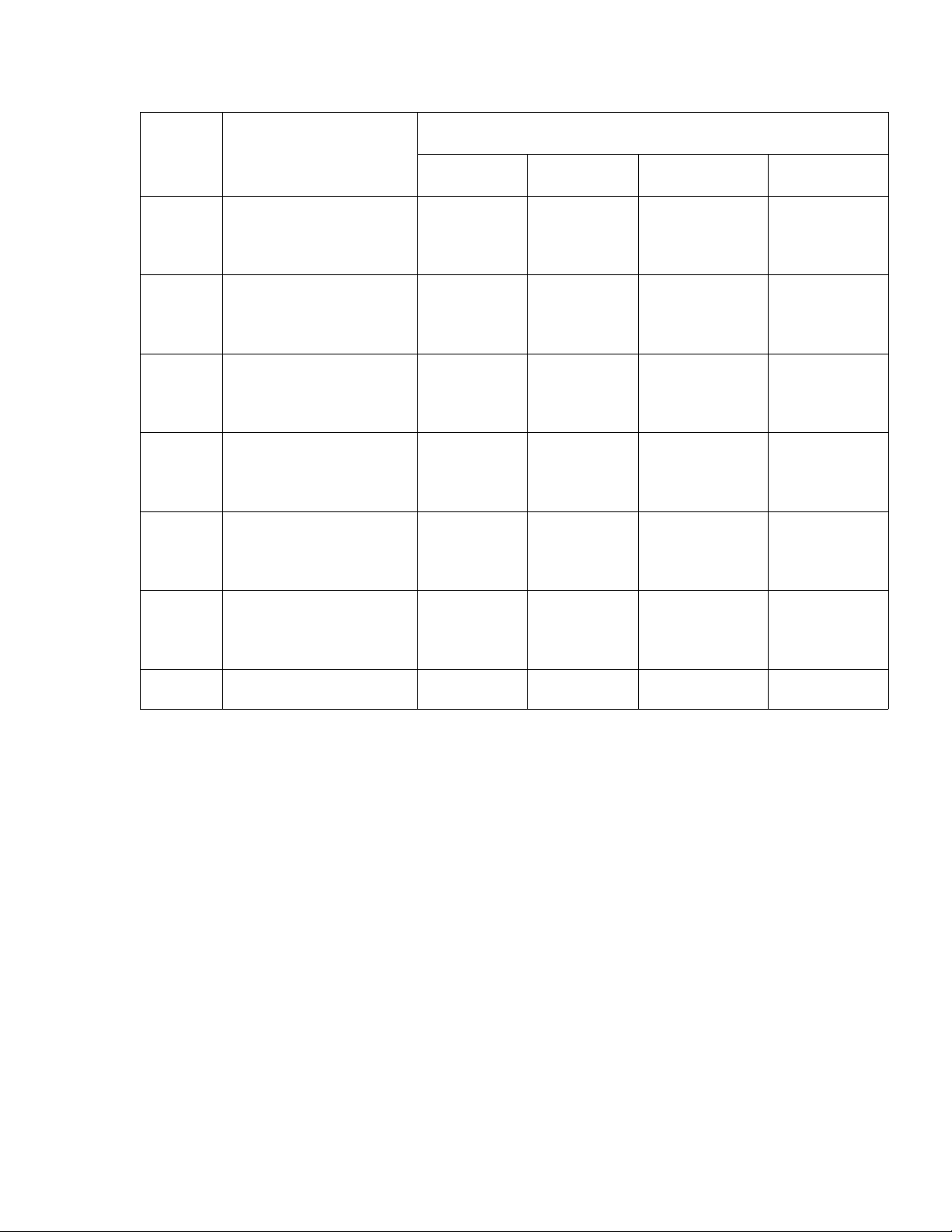
S TTốTên các bài trong
mô đun
Th i gianờ
T ng sổ ố Lý thuy tếTh c hànhựKi m tra*ể
1 M đu v dungở ầ ề
d chị
0 0 0 0
2 Pha ch dung d chế ị
ch t ch th ấ ỉ ị
8 0 8 0
3 Pha ch dung d chế ị
thu c th h u cố ử ữ ơ
7 0 7 0
4 Pha ch dung d chế ị
đm ệ
5 0 5 0
5 Pha ch dung d chế ị
chu n ẩ
15 0 15 0
6 Pha ch dung d chế ị
ch t t y r a ấ ẩ ử
10 0 5 5
C ngộ45 45 40 5
ĐÁNH GIÁ MÔN H CỌ
Môn h c s không thi. Đi m t ng k t môn h c s đc tính nh sau:ọ ẽ ể ổ ế ọ ẽ ượ ư
Đi m t ng k t môn h c b ng trung bình c ng đi m các bài th c t p vàể ổ ế ọ ằ ộ ể ự ậ
đi m thi th c hành.ể ự
Đi m li t: sinh viên b ể ệ ị đi m không (0)ể trong m t bài th c t p (khôngộ ự ậ
n p báo cáo, ngh h c không phép, b gi ng viên m i ra kh i l p …) sộ ỉ ọ ị ả ờ ỏ ớ ẽ
KHÔNG ĐTẠ môn h c này.ọ

Đi m t ng k t môn h c l y đn 1 s l sau d u ph y.ể ổ ế ọ ấ ế ố ẻ ấ ẩ
Sinh viên làm h h ng, n t v d ng c không b i th ng đúng h n sư ỏ ứ ỡ ụ ụ ồ ườ ạ ẽ
không đc công nh n k t qu môn h c.ượ ậ ế ả ọ
Sinh viên gian l n trong h c t p (không làm bài mà t ch s li u, saoậ ọ ậ ự ế ố ệ
chép bài c a b n) s b h y k t qu và nh n đi m không (0) cho mônủ ạ ẽ ị ủ ế ả ậ ể
h c.ọ

THANG ĐI M ĐÁNH GIÁ BÀI TH C HÀNHỂ Ự
M i bài th c hành s đc ch m đi m d a theo các tiêu chí sauỗ ự ẽ ượ ấ ể ự
Các tiêu chí Đi m t i đaể ố Ch m đi mấ ể
T ch cổ ứ 1 đi mểTr t t , n n pậ ự ề ế
Thao tác 3 đi mểLàm sai thao tác s b tr đi mẽ ị ừ ể
An toàn 1 đi mểX y ra cháy n , đ v s b tr đi mả ổ ổ ỡ ẽ ị ừ ể
K t quế ả 1 đi mểĐ chính xác c a k t quộ ủ ế ả
Th i gianờ1 đi mểLàm th c nghi m quá gi b tr đi mự ệ ờ ị ừ ể
Báo cáo 3 đi mểCh m theo bài báo cáo thí nghi m SV n pấ ệ ộ
T NGỔ10 đi mể

N I QUY - QUY ĐNH TH C HÀNHỘ Ị Ự
H c sinh, sinh viên (SV) vào phòng thí nghi m (PTN), ph i tuân th th cọ ệ ả ủ ự
hi n m i yêu c u c a giáo viên hệ ọ ầ ủ ng d n th c hành (GVHD) và cán bướ ẫ ự ộ
phòng thí nghi m (CBPTN)ệ
Đi h c đúng gi , SV đi tr quá 15 phút không đc vào th c hành.ọ ờ ễ ượ ự
Khi vào PTN, n u SV không thu c bài th c hành, thì GVHD yêu c u sinhế ộ ự ầ
viên ra kh i PTNỏ
SV ch u trách nhi m v các d ng c , thi t b đc giao khi vào phòng thíị ệ ề ụ ụ ế ị ượ
nghi m. N u làm hệ ế h ng, SV ph i ch u đn bù cho CBPTN, và b GVHDư ỏ ả ị ề ị
tr đi m bài th c hành đóừ ể ự
Khi th c t p, ph i tuy t đi gi im l ng, không đc nói l n ti ng, hútự ậ ả ệ ố ữ ặ ượ ớ ế
thu c lá, n ào, làm m t tr t t trong phòng thí nghi mố ồ ấ ậ ự ệ
Khi x lý m u, đun trên b p đi n có mùi, hay ph i làm vi c v i acid đc,ử ẫ ế ệ ả ệ ớ ặ
ki m đc, các dung môi bay h i, thì nh t thi t ph i làm trong t hút.ề ặ ơ ấ ế ả ủ
Các máy móc thi t b ph i v n hành đúng theo s ch d n c a GVHD, SVế ị ả ậ ự ỉ ẫ ủ
không đc t ý v n hành khi chượ ự ậ a đc h ng d n.ư ượ ướ ẫ
Các máy móc tr c và sau khi đo ph i ki m tra ngu n đi n, ngu n n c,ướ ả ể ồ ệ ồ ướ
v sinh máy, không đc di chuy n máy trong phệ ượ ể òng hay ra ngoài phòng..
Không đc t ti n l y hoá ch t, v t t thi t b , d ng c ra kh i PTN.ượ ự ệ ấ ấ ậ ư ế ị ụ ụ ỏ
Ph i n m v ng quy trình phân tích, tìm hi u ý nghĩa c a m i thao tácả ắ ữ ể ủ ỗ
tr c khi làm, không đc làm c u th , vô ướ ượ ẩ ả ý th c, làm hao phí hóa ch t.ứ ấ
Ph i có s tay ghi các thông s , lả ổ ố u ưý trong quá trình th c nghi m.ự ệ
Khi ra v , ph i r a s ch s các d ng c , d n d p ngăn n p, giao tr d ngề ả ử ạ ẽ ụ ụ ọ ẹ ắ ả ụ
c cho CBPTNụ

M i s làm m t mát, họ ự ấ h ng do SV gây ra, SV ph i ch u trách nhi m v iư ỏ ả ị ệ ớ
Nhà Tr ng, t k lu t đn bù, h h nh ki m đn bu c thôi h c.ườ ừ ỷ ậ ề ạ ạ ể ế ộ ọ

![Tài liệu thực hành hoá sinh [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260406/hoahongxanh0906/135x160/90741775619537.jpg)
![Tài liệu Hướng dẫn thực tập môn Hóa nước [Chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20251231/kimphuong1001/135x160/22661767942303.jpg)

![Bài giảng Thực hành Hóa hữu cơ 2 Trường ĐH Võ Trường Toản [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230606/loivokiet/135x160/428504094.jpg)















![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



