
1
ĐT V N ĐẶ Ấ Ề
Ung th bi u mô t bào gan (Hepatocellular carcinoma - HCC,ư ể ế
UTBMTBG) là m t trong nh ng b nh lý ác tính hay g p hàng đu th gi i.ộ ữ ệ ặ ầ ế ớ
B nh đng hàng th 6 trong 10 lo i ung th hay g p, là nguyên nhân th baệ ứ ứ ạ ư ặ ứ
gây t vong do ung th . Theo GLOBOCAN c tính riêng năm 2018 đã cóử ư ướ
841.00 tr ng h p m c m i và 782.000 b nh nhân t vong do UTBMTBGườ ợ ắ ớ ệ ử
[1]. Các nghiên c u đã ghi nh n nhi m virus viêm gan B (HBV) m n làứ ậ ễ ạ
nguyên nhân chính gây UTBMTBG. Vi t Nam có t l nhi m HBV caoệ ỷ ệ ễ
t ng ng có s ng i m c UTBMTBG t ng đi l n. Đây là lo i ung thươ ứ ố ườ ắ ươ ố ớ ạ ư
có tiên l ng x u v i th i gian s ng thêm ng n, liên quan đn kh năngượ ấ ớ ờ ố ắ ế ả
ch n đoán s m còn nhi u h n ch . Do ẩ ớ ề ạ ế v y, hi n nay trên th gi i nh ngậ ệ ế ớ ữ
nghiên c u v sinh b nh h c c a UTBMTBG nh m m c tiêu nh n di nứ ề ệ ọ ủ ằ ụ ậ ệ
nh ng d u n sinh h c có giá tr trong ch n đoán, đi u tr đã đc ti nữ ấ ấ ọ ị ẩ ề ị ượ ế
hành r ng rãi. ộ
V i s phát tri n m nh m c a sinh h c phân t , nhi u nghiên c u đãớ ự ể ạ ẽ ủ ọ ử ề ứ
ghi nh n vai trò ki u gen, đc bi tậ ể ặ ệ các đa hình gen (SNP: Single nucleotide
polymorphism) c a v t ch đóng vai trò quan tr ng trong đáp ng mi nủ ậ ủ ọ ứ ễ
d ch c a c th khi nhi m HBV, nh h ng đn quá trình hình thành viêmị ủ ơ ể ễ ả ưở ế
gan m n, x gan, phát tri n UTBMTBG. Nh v y, nghiên c u đa hình genạ ơ ể ư ậ ứ
giúp phân t ng đi t ng nguy c , c i thi n phát hi n s m và k t qu đi uầ ố ượ ơ ả ệ ệ ớ ế ả ề
tr b nh [2], [3]. Gen ị ệ TNF - α n m trên nhằánh ng n c a nhi m s c th s 6ắ ủ ễ ắ ể ố
(NST 6p21). Đây là m t gen có nhi u đi m đa hình đn, đi m đa hình t i vộ ề ể ơ ể ạ ị
trí -308 đc đánh giá có liên quan đn nguy c UTBMTBG. Các nghiênượ ế ơ
c u cho th y alen A c a đi m đa hình trên liên quan đn tăng c ng s nứ ấ ủ ể ế ườ ả
xu t TNF – trên c αấ ả in vitro và in vivo. Ngoài ra, ng i mang alen A cóườ

2
tăng nguy c UTBMTBG cao h n khi so sánh v i ng i mang alen G [4],ơ ơ ớ ườ
[5].
Gen TGF – 1β n m trên nhánh dài nhi m s c th s 19 (19q13.1-13.3),ằ ễ ắ ể ố
có nhi u đi m đa hình, trong đó đề ể i mể đa hình t i v trí -509 C>T đã đcạ ị ượ
đánh giá có liên quan đn n ng đ TGF huy t t ng. H n n a, phân tíchβế ồ ộ ế ươ ơ ữ
đi m đa hình ểTGF – 1-509 C>Tβ th y nh ng cá th có alen T tăng nguy cấ ữ ể ơ
UTBMTBG so v i nh ng cá th mang alen C [6].ớ ữ ể
Nhi u nghiên c u cho th y các đi m đa hình ề ứ ấ ể TNF - -308α và TGF -
1-509β nh h ng đn ti n tri n c a viêm gan m n, x gan, hình thành,ả ưở ế ế ể ủ ạ ơ
phát tri n và di căn c a UTBMTBG thông qua vi c ki m soát n ng đ cácể ủ ệ ể ồ ộ
cytokine t ng ng [3], [7], [8]. TNF và TGF là nh ng cytokine đa ch cα βươ ứ ữ ứ
năng, đóng vai trò ki m soát nhi u quá trình cể ề ủa t bào nh tăng tr ng, bi tế ư ưở ệ
hóa, hình thành m ng l i gian bào, đáp ng mi n d ch, sinh m ch máu, ch tạ ướ ứ ễ ị ạ ế
theo ch ng trình. ươ Bên c nh đó, trong vi môi tr ng sinh u các cytokine nàyạ ườ
t ng tác, h tr l n nhau làm tăng c ng quá trình hình thành và ti n tri nươ ỗ ợ ẫ ườ ế ể
UTBMTBG [5],[3],[9].
Vi t Nam là qu c gia có t l nhi m HBV và m c UTBMTBG cao v iệ ố ỷ ệ ễ ắ ớ
nh ng h u qu vô cùng n ng n . Tuy nhiên, cho đn nay ch a có m tữ ậ ả ặ ề ế ư ộ
nghiên c u nào đánh giá nh h ng c a đa hình hai gen trên v i nguy c bứ ả ưở ủ ớ ơ ị
UTBMTBG. Vì v y, chúng tôi ti n hành đ tài “ậ ế ề Nghiên c u đa hình genứ
TNF- -308 và TGF- 1-509 b nh nhân ung th bi u mô t bào gan cóα β ở ệ ư ể ế
HBsAg d ng tínhươ ” v i 2 m c tiêu:ớ ụ
1.Xác đnh t l ki u gen và alen c a 2 đi m đa hình genị ỷ ệ ể ủ ể TNF - - 308,α
TGF - 1 - 509 b nh nhân UTBMTBG có HBsAg (+).βở ệ

3
2.Phân tích m i liên quan c a đa hình gen TNF- - 308, TGF- 1- 509α βố ủ
v i nguy c UTBMTBG và m t s đc đi m lâm sàng, c n lâm sàngớ ơ ộ ố ặ ể ậ
c a b nh nhân UTBMTBG có HBsAg (+).ủ ệ

4
CH NG 1ƯƠ
T NG QUAN TÀI LI UỔ Ệ
1.1. UNG TH BI U MÔ T BÀO GANƯ Ể Ế
Ung th bi u mô t bào gan (UTBMTBG) là m t b nh ác tính kh iư ể ế ộ ệ ở
phát t t bào gan (HCC: hepatocellular carcinoma), chi m đa s các b nhừ ế ế ố ệ
ác tính c a gan (> 90%)ủ [10].
1.1.1. D ch t ung th bi u mô t bào gan trên th gi iị ễ ư ể ế ế ớ
Ung th bi u mô t bào gan là lo i ung th đng hàng th 6 trong 10ư ể ế ạ ư ứ ứ
lo i ung th ph bi n trên toàn c u (th 5 v i nam, th 9 đi v i n ). Đcạ ư ổ ế ầ ứ ớ ứ ố ớ ữ ặ
đi m d ch t c a UTBMTBG khác nhau các vùng trên th gi i, nh ngể ị ễ ủ ở ế ớ ữ
vùng có t l m c cao bao g m Sahara châu Phi, Đông Á, Đông Nam Á,ỷ ệ ắ ồ
Trung Qu c, Đài Loan, Hàn Qu c, Nh t B n, do đây là n i l u hành d ch tố ố ậ ả ơ ư ị ễ
c a HBV, lo i virus có m i liên quan ch t ch v i UTBMTBG [11]. Theoủ ạ ố ặ ẽ ớ
T ch c Y t Th gi i, c tính riêng năm 2018 đã có t i 841.000 tr ngổ ứ ế ế ớ ướ ớ ườ
h p m c m i UTBMTBG trên toàn c u, ch u trách nhi m cho 782.000ợ ắ ớ ầ ị ệ
tr ng h p t vong cùng năm. S tr ng h p t vong g n b ng s m iườ ợ ử ố ườ ợ ử ầ ằ ố ớ
m c, ph n ánh UTBMTBG là m t b nh có tiên l ng n ng, th i gian s ngắ ả ộ ệ ượ ặ ờ ố
thêm ng n [12].ắ
Nam gi i có m c b nh cao h n n , g p t 2-4 l n. T l m c tăngớ ắ ệ ơ ữ ấ ừ ầ ỷ ệ ắ
d n theo tu i, cao nh t kho ng 65-70 tu i, trong đó nh ng vùng l u hànhầ ổ ấ ả ổ ở ữ ư
d ch t HBV, đnh m c b nh th p h n ch t 55-60 tu i [10], [13], [14].ị ễ ỉ ắ ệ ấ ơ ỉ ừ ổ
Vài th p k g n đây, xu h ng m c UTBMTBG thay đi khá nhi u.ậ ỷ ầ ướ ắ ổ ề
Trong khi các vùng có t l m c th p (ỷ ệ ắ ấ M , trung tâm châu Âu) b nh ỹ ệ có xu
h ng gia tăng do liên quan đn béo phì và nhi m HCV, các vùng tr c đâyướ ế ễ ướ
5
có t l m c cao ỷ ệ ắ l i có xu h ng gi m vìạ ướ ả áp d ng ch ng trình tiêm phòngụ ươ
HBV [2].
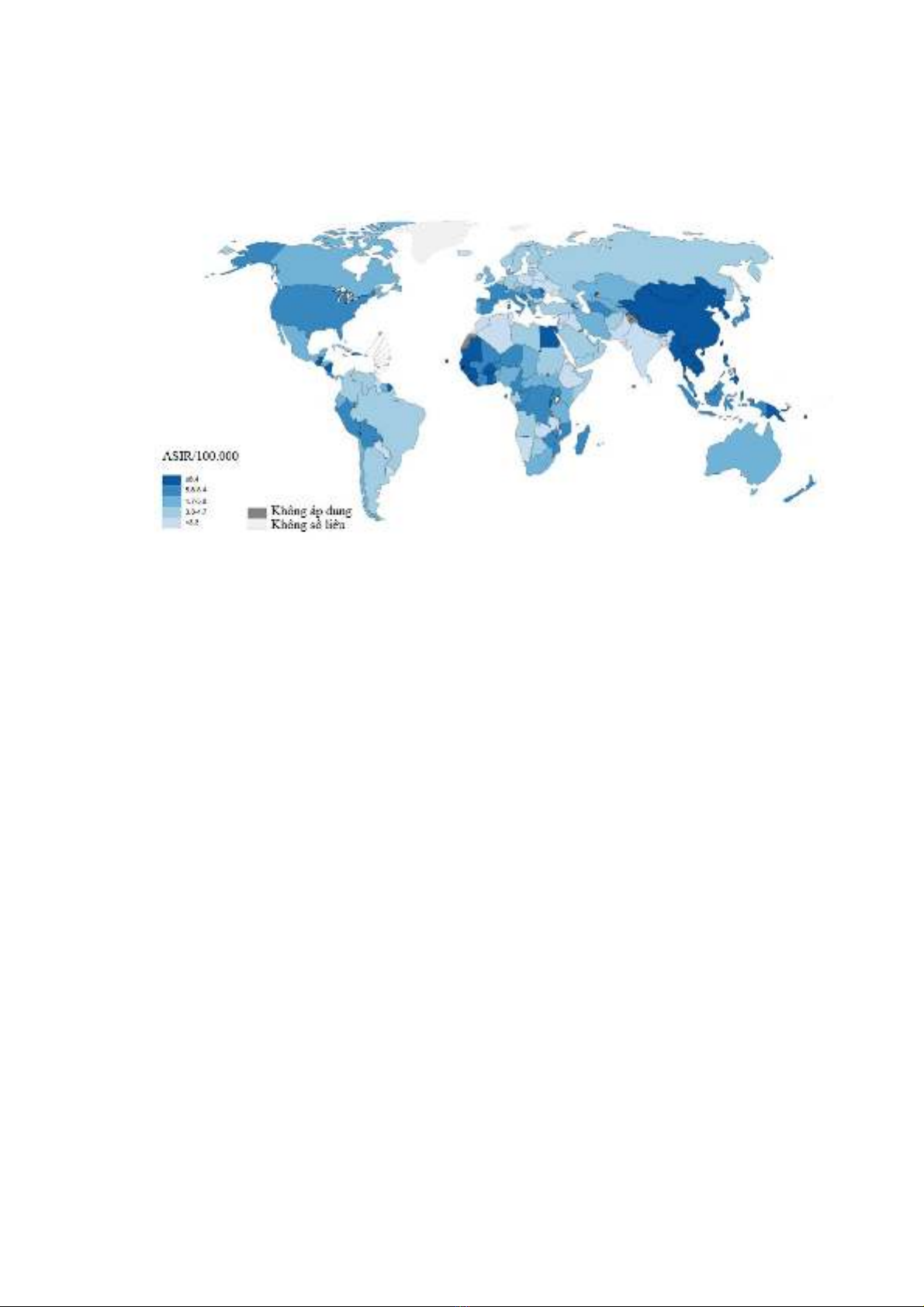
Hình 1.1. T l m c ung th bi u mô t bào gan chu n ỷ ệ ắ ư ể ế ẩ
theo tu i và gi i trên th gi iổ ớ ế ớ
* Ngu n: Singal, A.(2020) [15]ồ
1.1.2. D ch t ung th bi u mô t bào gan Vi t ị ễ ư ể ế ệ Nam
N m trong khu v c Đông Nam Á, đi m nóng c a th gi i vằ ự ể ủ ế ớ ề
UTBMTBG, Vi t Nam có t l m c b nh cao. T ng k t m t s nghiên c uệ ỷ ệ ắ ệ ổ ế ộ ố ứ
đc ti n hành t i nhi u đa ph ng trên toàn qu c, các th i đi m khácượ ế ạ ề ị ươ ố ở ờ ể
nhau cho th y ấUTBMTBG th c s là m t gánh n ng v i n n y t . Báo cáoự ự ộ ặ ớ ề ế
c a Nguy n Văn Vy và cs v công tác phòng ch ng ung th kéo dài 10 nămủ ễ ề ố ư
t i H i Phòng (2003) đã cho th y ạ ả ấ UTBMTBG có m c đ ph bi n đngứ ộ ổ ế ứ
hàng th 3 trong các lo i ung th [16]. M t nghiên c u đc khác ti n hànhứ ạ ư ộ ứ ượ ế
b i Nguy n Đình Tùng (2010) t i Th a Thiên Hu trong th i gian t 2001 –ở ễ ạ ừ ế ờ ừ
2009 v i 7234 tr ng h p m c ung th m i, cũng ghi nh n trong 10 lo iớ ườ ợ ắ ư ớ ậ ạ
ung th hay g p, ư ặ UTBMTBG đng hàng đu nam v i ASRI (Ageứ ầ ở ớ





![Luận văn Thạc sĩ: Tổng hợp và đánh giá hoạt tính chống ung thư của hợp chất lai chứa tetrahydro-β-carboline và imidazo[1,5-a]pyridine](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250807/kimphuong1001/135x160/50321754536913.jpg)




















