
14
Chương 2
Sự đẫn điện của dung dịch chất điện li
1.4 Mở đầu
Dung dịch chất điện li còn gọi là chất dẫn điện loại hai, sự dẫn điện của nó nhờ sự tải
điện của các ion. Kim loại và oxit kim loại dẫn điện bằng electron được gọi là chất dẫn điện
loại 1 và có điện trở khoảng 10−6 ÷ 10−3 Ω.cm.
Nghiên cứu về độ dẫn điện của dung dịch chất điện li có liên quan chặt chẽ với hiện
tượng ăn mòn điện hoá và cho phép giải thích sự khác biệt về tốc độ ăn mòn trong môi trường
nước biển và nước sông, ao, hồ.
Để đánh giá khả năng dẫn điện của dung dịch chất điện li người ta sử dụng hai đại lượng:
độ dẫn điện riêng và độ dẫn điện đương lượng của dung dịch chất điện li.
1.5 Độ dẫn điện riêng và độ dẫn điện đương lượng
2.2.1 Độ dẫn điện riêng
Độ dẫn điện riêng của dung dịch chất điện li đã cho là độ dẫn điện của nó được đặt giữa
hai điện cực song song có diện tích 1 cm2 và cách nhau 1 cm.
Độ dẫn điện riêng χ là đại lượng nghịch đảo của điện trở suất.
χ = ρ
1 (2.1)
Để tìm đơn vị đo χ ta xét điện trở của một ống dung dịch chất điện li tương tự một dây
dẫn kim loại có chiều dài l (cm) và tiết diện S (cm2), điện trở suất của dây kim loại là ρ.
Vậy điện trở R của dây dẫn được tính:
R = ρ.A
S (2.2)
Suy ra: χ = ρ
1 = 1
R.A
S (Ω−1.cm−1) (2.3)
Khác với chất dẫn điện kim loại, độ dẫn điện riêng của chất dẫn điện loại 2 tăng khi tăng
nhiệt độ.
χt = χ18[1 + k(t − 18oC)] (2.4)
trong đó: χt − độ dẫn điện riêng ở nhiệt độ t bất kỳ, toC > 18oC;
χ18 − độ dẫn điện riêng ở nhiệt độ 18oC.
15
Giá trị hệ số k thay đổi tuỳ thuộc vào bản chất dung dịch, đối với dung dịch axit mạnh k
= 0,0164, đối với dung dịch bazơ mạnh k = 0,0190, đối với dung dịch muối k = 0,022.
2.2.2 Độ dẫn điện đương lượng
Độ dẫn điện đương lượng λ của dung dịch chất điện li khảo sát là độ dẫn điện của một
dung dịch chứa đúng một đương lượng gam chất điện li được đặt giữa hai điện cực platin
song song với nhau và cách nhau 1 cm.
Giữa độ dẫn điện đương lượng λ và độ dẫn điện riêng χ có quan hệ với nhau theo phương
trình:
λ = χ1000.
C (2.5)
trong đó C là nồng độ đương lượng gam/lit.
Từ đó suy ra đơn vị đo của λ bằng Ω−1.cm2.đlg−1.
Nếu đặt V = 1
C gọi là độ pha loãng thì công thức (2.5) có dạng:
λ = 1000.V.χ (2.6)
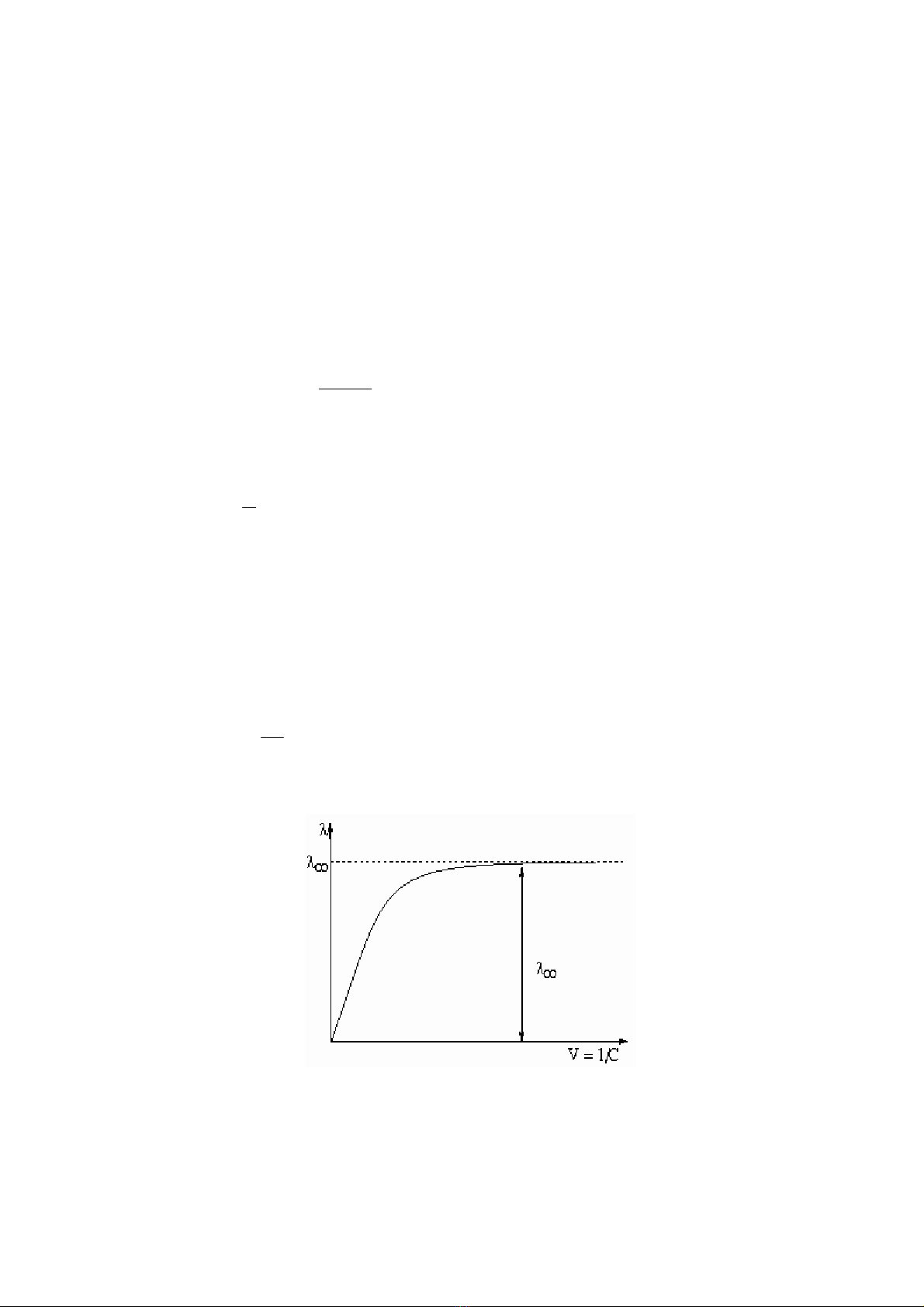
Từ phương trình (2.5) cho thấy khi dung dịch rất loãng (C → 0) thì giá trị λ đạt đến giá
trị tới hạn λ → λ∞.
Đối với dung dịch chất điện li yếu, sự phụ thuộc của độ dẫn điện đương lượng λ vào
nồng độ chất điện li thực chất là phụ thuộc vào sự biến đổi độ điện li α (hình 2.1).
Vậy: λC = α.λ∞ (2.7)
Suy ra: α =
∞
λ
λ
C (2.8)
trong đó: λC − độ dẫn điện đương lượng của dung dịch có nồng độ C.
Hình 2.1
Sự phụ thuộc của độ dẫn điện đương lượng λ vào độ pha loãng V
16
1.6 Quan hệ giữa độ dẫn điện riêng và tốc độ chuyển động của ion
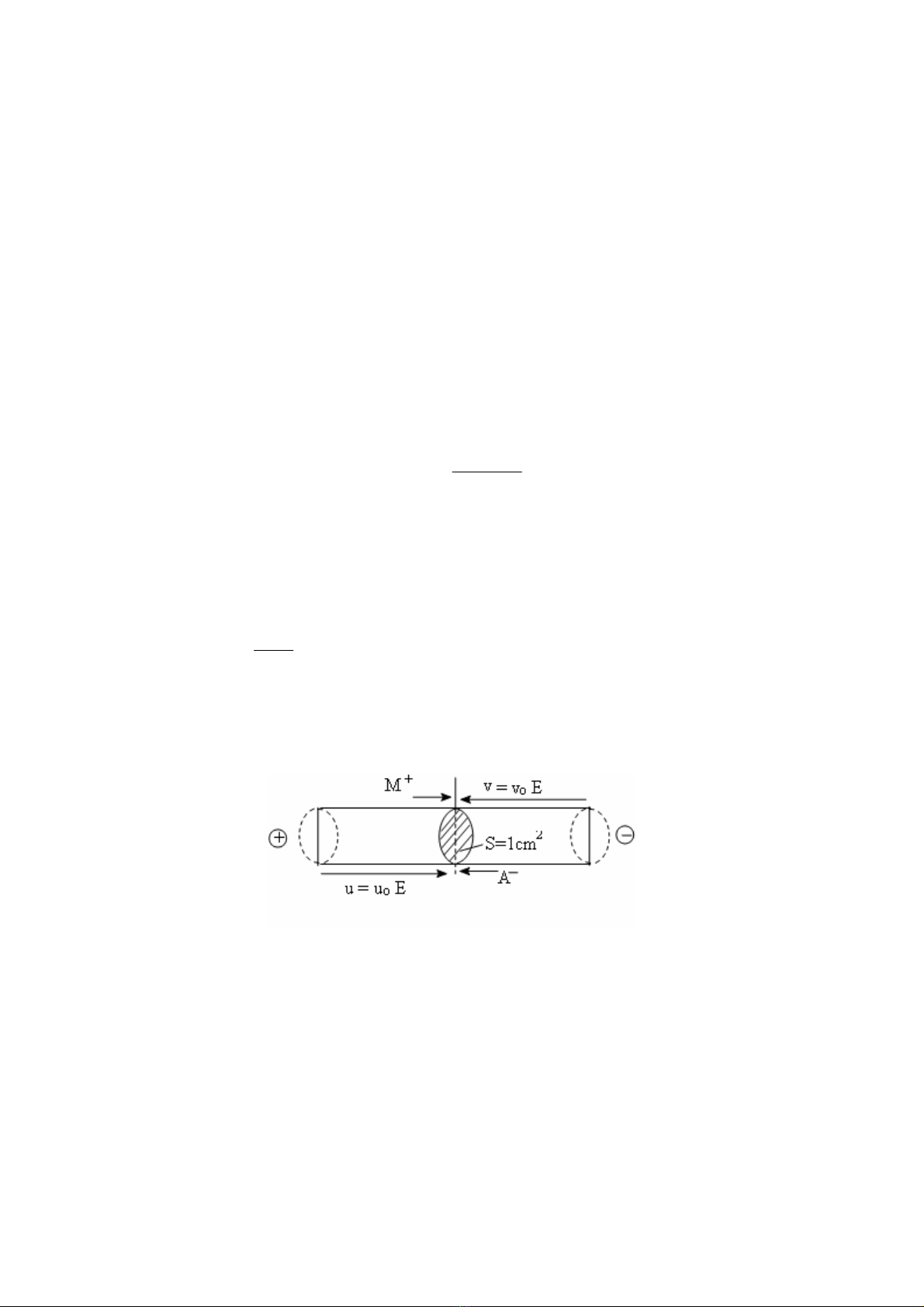
Trong trường hợp đơn giản ta hãy xét một ống dung dịch chất điện li 1-1 (ví dụ KCl,
KNO3...). MA phân li thành các ion M+ và A−.
Gọi Uo - tốc độ chuyển động tuyệt đối của cation M+
và Vo - tốc độ chuyển động tuyệt đối của anion A−.
Nếu đặt ống dung dịch vào điện trường E (V/cm) thì:
Tốc độ chuyển động của cation:
U = Uo.E (cm/giây) (2.9)
Tốc độ chuyển động của anion:
V = Vo.E (cm/giây) (2.10)
Khi E = 1 (V/cm) thì U = Uo và V = Vo ⎛⎞
=
⎜⎟
⎝⎠
2
cm cm / V.s
s.( v / cm )
Dưới tác dụng của điện trường, trong một đơn vị thời gian 1 giây số cation μ+ và anion μ−
đi qua tiết diện S = 1 cm2 bằng:
μ+ = C/α ν+ NA.Uo.E (2.11)
μ− = C/α ν− NA.Vo.E (2.12)
trong đó: C/ = C
1000 gọi là nồng độ ion trong một đơn vị thể tích 1 cm3.
Uo và Vo là tốc độ tuyệt đối của cation và anion và chính là độ dài do cation di chuyển
trong 1 đơn vị thời gian 1 giây với E = 1 (V/cm).
Hình 2.2
Sự di chuyển của các ion dưới tác dụng của điện trường
Phương trình (2.11) và (2.12) có thể viết:
μ+ = C α ν+ NA.Uo.E.10−3 (2.13)
μ− = C α ν− NA.Vo.E.10−3 (2.14)
trong đó: α - độ phân li;
ν+, ν− - số cation và anion;

17
N
A - là số Avogađro.
Nếu gọi Q là điện lượng do cation và anion tải thì:
Q = μ+ Z+ . e + μ− Z− . e (2.15)
trong đó: Z+, Z− là số oxi hoá của cation và anion;
e là điện tích cơ bản, e = 1,602.10−19C.
Đối với chất điện li 1-1, Z1 = Z− = 1
hoặc Q = C α NA e.10−3.E (ν+ Z+ Uo + ν− Z− Vo) (2.16)
Dung dịch chất điện li luôn trung hoà điện nên ν+ Z+ = ν− Z− = ν Z
Vậy phương trình (2.16) có dạng:
Q = i = 10−3 α C F ν Z (Uo + Vo)E (2.17)
Ở đây lượng điện Q do ion tải trong một đơn vị thời gian đi qua 1 cm2 chính là cường độ
dòng điện i đi qua ống dung dịch (hình 2.2).
Tương tự đối với dây dẫn kim loại có điện trở R có dòng điện i đi qua dây dẫn và điện thế
E, đối với ống dung dịch chất điện li (hình 2.2), theo định luật Ôm ta có:
i = χ.E (2.18)
So sánh (2.17) và (2.18) rút ra:
χ = 10−3 α C F ν Z (Uo + Vo) (2.19)
Mặt khác, ta có:
λ = χ
dlg/l
1000.
C = α F (Uo + Vo) (2.20)
Các phương trình (2.19) và (2.20) thể hiện mối quan hệ giữa độ dẫn điện riêng và độ dẫn
điện đương lượng với tốc độ chuyển động tuyệt đối của cation và anion.
1.7 Linh độ ion
Tích số của hằng số Faraday và tốc độ tuyệt đối của cation Uo được gọi là linh độ cation:
U = F . Uo (2.21)
và linh độ anion: V = F . Vo (2.22)
Kết hợp (2.22) và (2.20) ta có:
λ = α (U + V) (2.23)
Đối với dung dịch loãng C → 0, α → 1 khi đó độ dẫn điện đương lượng λ được gọi là độ
dẫn điện đương lượng ở nồng độ vô cùng loãng λ∞ và phương trình (2.23) có dạng:
λ∞ = U∞ + V∞ (2.23a)
trong đó U∞ và V∞ là linh độ cation và anion ở nồng độ vô cùng loãng (còn gọi là linh độ
tới hạn) hoặc:
λ∞ = +
∞
λ +
−
∞
λ (2.24)
18
+
∞
λ và −
∞
λ là độ dẫn điện đương lượng của cation và anion ở nồng độ vô cùng loãng (C
→ 0).
Dựa vào công thức (2.24) khi biết độ dẫn điện đương lượng của ion tại nồng độ vô cùng
loãng tính được độ dẫn điện đương lượng phân tử ở nồng độ vô cùng loãng.
Ví dụ: Tính λ∞ của axit axetic cho biết:
Chất điện li HCl CH3COONa NaCl
λ∞
(Ω−1.cm2.đlg−1) 426,00 91,00 126,50
Theo công thức (2.24) ta có thể viết:
λ∞ (CH3COOH) = λ∞ (H+) + λ∞ (CH3COO−)
= λ∞ (HCl) + λ∞ (CH3COONa) − λ∞ (NaCl)
= 426,00 + 91,00 − 126,50 = 390,6
Giá trị linh độ tới hạn của ion
+
3
HO và OH− rất lớn so với các cation và anion khác. Trong
môi trường nước các ion này chuyển động theo cơ chế đặc biệt - cơ chế truyền cho proton
giữa chúng và phân tử HOH bên cạnh.
Bảng 2.1 Giá trị linh độ tới hạn của một số cation và anion
Cation +
3
HO Na+ K+
+
4
NH Ca2+ Zn
2+
Giá trị linh
độ V∞ (25oC) 349,8 50,1 73,5 73,5 59,5 52,8
Anion OH− F−
−
4
ClO
−
3
HCO −2
4
SO
Giá trị linh
độ V∞ (25oC) 197,6 55,4 67,3 64,6 80
Đối với ion OH−
Mặt khác trong cùng một điều kiện giá trị linh độ tới hạn của ion phụ thuộc vào nồng độ,
nhiệt độ và dung môi (xem bảng 2.2).
H O H
H
+
+ O H
H
O
H
H +
+
H O H
H
+
O
H
H O H
H
+
O
H
O
H



![Lý thuyết đại cương về kim loại và hợp kim [A-Z Mới Nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2015/20150815/vinhthuong2302/135x160/1543768943.jpg)

![Siêu Vật Liệu: [Thêm thông tin chi tiết về loại siêu vật liệu hoặc ứng dụng của nó]](https://cdn.tailieu.vn/images/document/thumbnail/2011/20110820/thuyquynh21/135x160/sieu_vat_lieu_6413.jpg)
![Vật liệu mới thông minh (Phần 2): [Thêm thông tin chi tiết nếu có]](https://cdn.tailieu.vn/images/document/thumbnail/2011/20110728/bupbelen_238/135x160/5_7573.jpg)













![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



