
1
1
Ch ng 2ươ
Ch ng 2ươ
H p Thấ ụ

2
2
Gi i thi uớ ệ
Gi i thi uớ ệ
Trong công nghiêp hoa chât co rât nhiêu
nguyên liêu va san phâm dang khi h n h p. ơ ỗ ợ
Muôn tiêp tuc gia công, chê biên cac hôn h p ơ
khi ta cân lam sach chung khoi cac tap chât hoăc
tach chung thanh cac câu t riêng biêt. ư
Ví d : nh sau khi hóa than ta thu đu c h n ụ ư ợ ỗ
h p khí các ch t Nợ ấ 2 , H2, H2S, NH3, CO, CO2
… mu n dùng h n h p y đ t ng h p NHố ỗ ợ ấ ể ổ ợ 3 đ ể
s n xu t phân đ m (Urê) ta ph i tách chúng ra. ả ấ ạ ả

Muôn tiêp tuc gia công, chê biên cac hôn h p ơ
khi ta cân lam sach chung khoi cac tap chât hoăc
tach chung thanh cac câu t riêng biêt. ư
Ví d : nh sau khi hóa than ta thu đu c h n ụ ư ợ ỗ
h p khí các ch t Nợ ấ 2 , H2, H2S, NH3, CO, CO2
… mu n dùng h n h p y đ t ng h p NHố ỗ ợ ấ ể ổ ợ 3 đ ể
s n xu t phân đ m (Urê) ta ph i tách chúng ra. ả ấ ạ ả
3
3

4
4
Các ph ng pháp tách h n h p khíươ ổ ợ
Các ph ng pháp tách h n h p khíươ ổ ợ
Có nhi u ph ng pháp đ tách h n h p khí ề ươ ể ổ ợ
thành c u t .ấ ử
–Ph ng pháp hóa h c. ươ ọ
–Ph ng pháp c lý (d a trên tính ch t hóa ươ ơ ư ấ
l ng các nhi t đ khác nhau).ỏ ở ệ ộ
–Phu ng pháp hút: dùng ch t l ng hay ch t ơ ấ ỏ ấ
r n x p đ hút. ắ ố ể
N u dùng ch t l ng g i là qúa trình h p th , ế ấ ỏ ọ ấ ụ
n u dùng ch t r n thì qúa trình g i là h p phế ấ ắ ọ ấ ụ
5
5
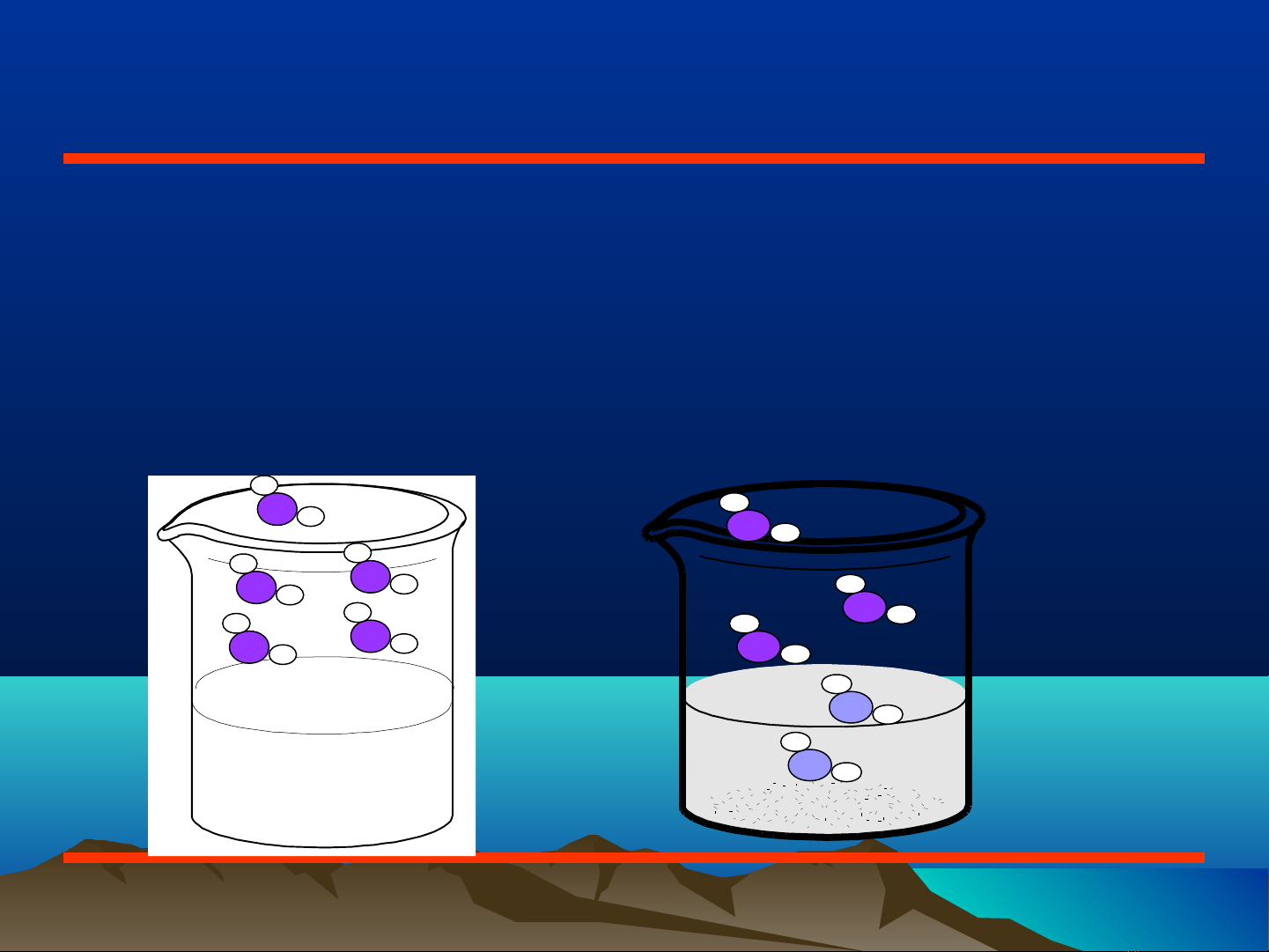
Khái ni m h p thuệ ấ
Khái ni m h p thuệ ấ
H p th là qúa trình h p khí b ng ch t l ng, ấ ụ ấ ằ ấ ỏ
khí đ c hút g i là ch t b h p th , ch t l ng ượ ọ ấ ị ấ ụ ấ ỏ
dùng đ hút g i là dung môi (Còn g i là ch t ể ọ ọ ấ
h p th ), khí không b h p th g i là khí trấ ụ ị ấ ụ ọ ơ.
MEA




















![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



