
CHƯƠNG V: CHUYỂN HÓA
PROTEIN VÀ AMINO ACID

NỘI DUNG
I. SỰ CHUYỂN HOÁ AMINO ACID
1.1. Phản ứng khử amine hoá
1.2. Phản ứng khử carboxyl
1.3. Phản ứng chuyển amine
II. SỰ BÀI TIẾT CÁC CHẤT CẶN BÃ CHỨA
NITƠ
2.1. Sự tổng hợp và bài tiết ure (vòng Ornithine)
2.2. Tổng hợp và bài tiết acid uric
III. SINH TỔNG HỢP AMINO ACID
IV. SINH TỔNG HỢP PROTEIN
I. SỰ CHUYỂN HOÁ AMINO ACID
Phản ứng khử amine hoá
Phản ứng khử carboxyl
Phản ứng chuyển amine
1.1. Phản ứng khử amine hoá
Khử amine oxy hoá nhờ oxydase
Khử amin oxy hoá nhờ dehydrogenase
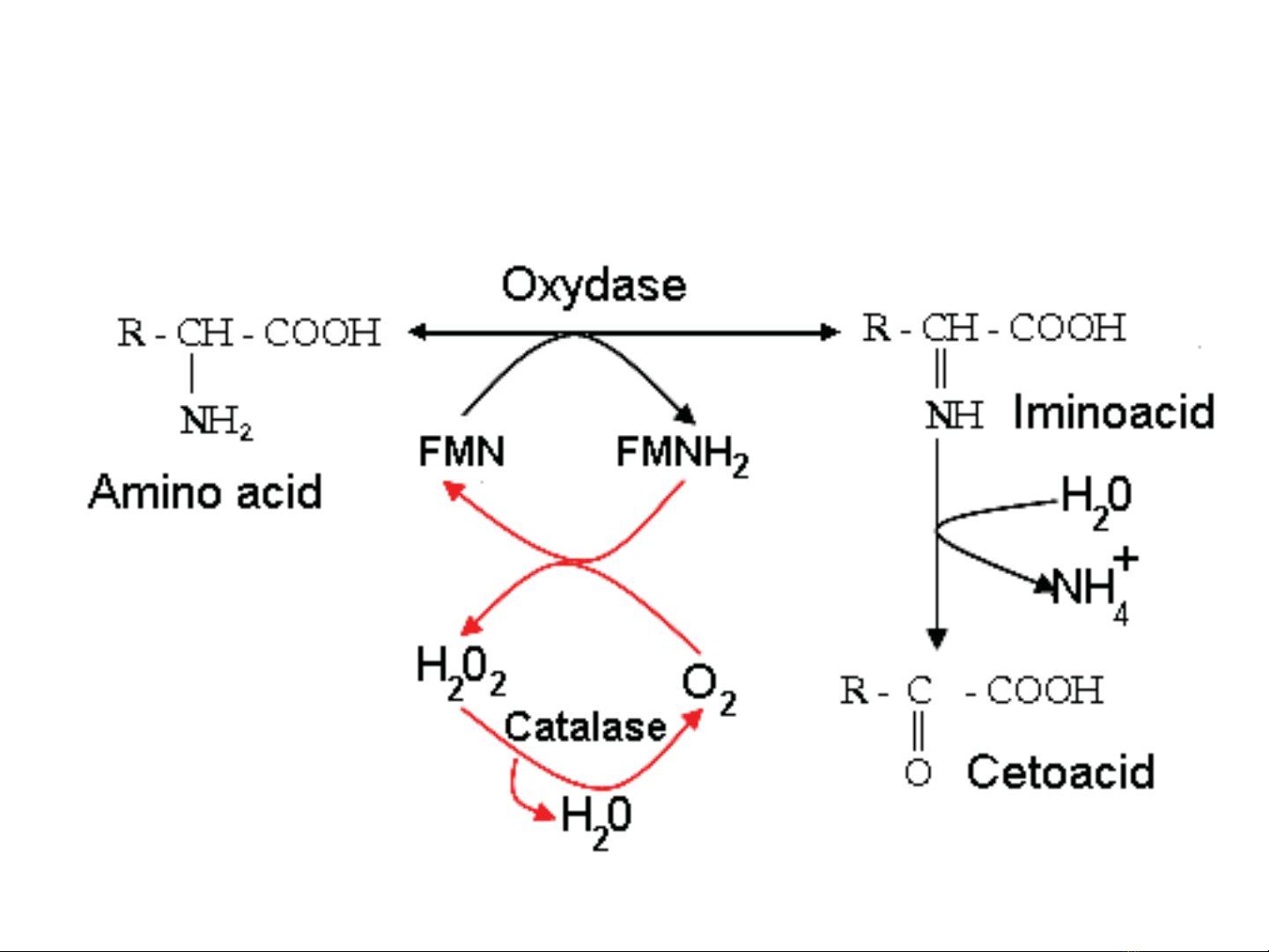
Khử amine oxy hoá nhờ oxydase
(có FMN hoặc FAD)

















![Giáo trình thí nghiệm Hợp chất tự nhiên trong y sinh [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260406/hoahongxanh0906/135x160/39941775556306.jpg)

![Tài liệu giảng dạy Sinh học và di truyền [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260323/hoatudang2026/135x160/42181774414220.jpg)

![Giáo trình Công nghệ vi sinh (Nghề Công nghệ sinh học TC/CĐ) - Trường Cao đẳng Đà Lạt [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260224/hoacattuong2026/135x160/87621772161812.jpg)




