
Giáo án hóa học lớp 11 nâng cao
- BÀI 61. AXIT CACBOXYLIC
TÍNH CHẤT HOÁ HỌC, ĐIỀU CHẾ VÀ ỨNG
DỤNG
I.Mục tiêu bài học:
1. Kiến thức:
- Học sinh hiểu: cấu trúc nhóm cacboxyl, điều
chế, tính chất hoá học của axit cacboxylic.
- Học sinh biết: ứng dụng của axit cacboxylic.
2. Kỹ năng: học sinh có kỹ năng:
- Gọi tên, viết CT của axit cacboxylic.
- Vận dụng cấu trúc, để hiểu tính chất hoá học và
giải đúng bài tập.
- Viết đúng các PTPƯ của anđehit.
- Vận dụng tính chất hoá học để định ra cách
điều chế, cách nhận biết.

3. Thái độ: giáo dục học sinh lòng yêu khoa học
hóa học thông qua các sản phẩm gần gũi trong cuộc
sống.
II. Chuẩn bị
1. Thầy: dung dịch HOOH, CH3COOH, axit
axetic băng, CaCO3.
2. Trò: ôn lại bài axit axetic ở lớp 9.
HOẠT ĐỘNG LÊN LỚP
I. Kiểm tra bài cũ (8’)
1.Câu hỏi: Tìm CTCT của: + Axit no đa chức
(C3H4O3)n.
+ Axit mạch hở, không
phân nhánh (C3H5O2)n.
2. Đáp án – biểu điểm:
(6đ) + (C3H4O3)n hay
2
n3
)
COOH
(
2
n5
H
2
n3
C
Vì axit no .2n
2
n3
2
2
n3
.2
2
n5
Vậy axit là: C3H5(COOH)3.
(4đ) + Vì mạch hở, không phân nhánh nên n = 1 hoặc
2.
n = 1 C3H5O2 Loại!
n = 2 C6H10O4 HOOC-(CH2)4-COOH.
II. Bài mới (35’)
Hoạt động 1:
(?) Nhận xét cấu tạo
phân tử axit?
1
0
’
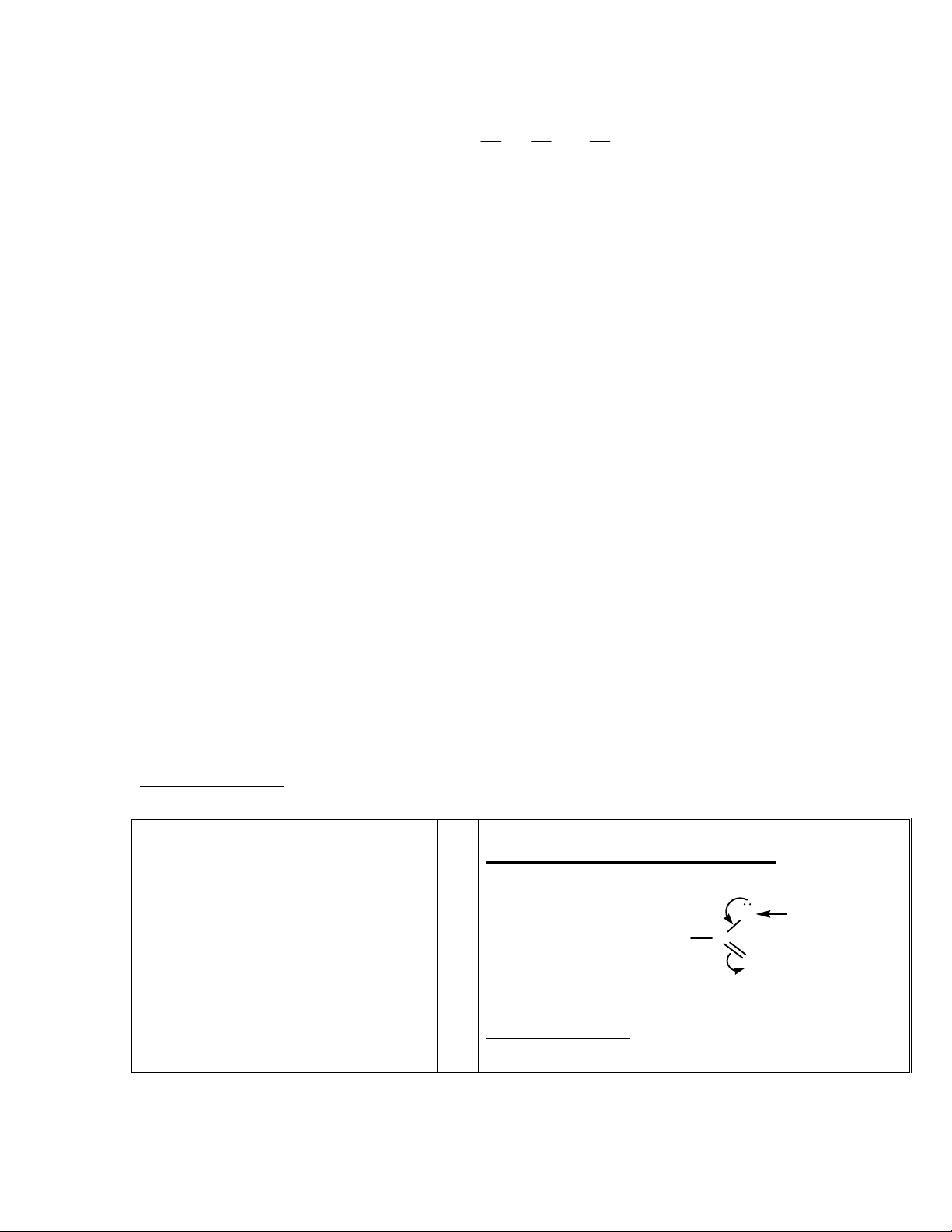
IV. Tính chất hóa học
R C
O
O
H
1. Tính axit

GV làm thí nghiệm:
CH3COOH + quì tím
+ Mg
+ NaOH
+ CaO
+ CaCO3
HS: Nhận xét, viết
phương trình phản
ứng.
a. Đổi màu quì tím
RCOOH H+ + RCOO-
b. Tác dụng với kim loại
2CH3COOH + Mg
(CH3COO)2Mg + H2
Magie
axetat
c. Tác dụng với bazơ v
à oxit
bazơ
HCOOH + NaOH
HCOONa
+ H2O
Natri
fomiat
2CH3COOH + CaO
(CH3COO)2Ca + H2O
Canxi

Hoạt động 2.
(?) Viết phương trình
phản ứng este hóa?
Vai trò của axit
sufuric?
GV : Trình bày như
SGK
Hoạt động 3.
GV trình bày như
SGK.
HS viết phương trình
4
’
8
’
axetat
d. Tác dụng với muối
2CH3COOH + CaCO3
(CH3COO)2Ca + CO2 + H2
O
CH3COOH + NaHCO3
CH3COONa + CO2+ H2O
2. Phản ứng tạo thành d
ẫn xuất
axit.
a. Phản ứng với rượu (ph
ản ứng
este hóa)
CH3COOH + C2H5OH H2SO4 ®, t0CH3COOC2H5 + H
2
b. Phản ứng tách nước li
ên phân
tử.
Khi có xúc tác P2O5.
CH3-CO-OH +H-O-CO-CH3
CH3 CO-O-CO CH3 + H2O
3. Phản ứng ở gốc hiđrocacbon.


























