
MC TIÊU CA CHNG
1. Kin thc
Bit:
- V trí ca các nguyên t kim loi trong bng tun hoàn
- Tính cht và ng dng ca hp kim
- Mt s khái nim trong chương: cp oxi hóa – kh, pin in hóa, sut in ng chun ca pin
in hóa, th in cc chun ca kim loi, s in phân (các phn ng hóa hc xy ra các
in cc)
Hiu:
- Gii thích ưc nhng tính cht vt lí, tính cht hóa hc chung ca kim loi. Dn ra ưc
nhng ví d minh ha và vit các PTHH
- Ý ngha ca dãy in hóa chun ca kim loi:
+ Xác nh chiu ca phn ng gia cht oxi hóa và cht kh trong hai cp oxi hóa – kh
+ Xác nh xut in ng chun ca pin in hóa
- Các phn ng hóa hc xy ra trên các in cc ca pin in hóa khi hot ng và ca quá trình
in phân cht in li
- iu kin, bn cht ca s n mòn in hóa và các bin pháp phòng, chng n mòn kim loi
- Hiu ưc các phương pháp iu ch nhng kim loi c th (kim loi có tính kh mnh, trung
bình, yu)
2. K nng
- Bit vn dng dãy in hóa chun ca kim loi :
+ Xét chiu ca phn ng hóa hc gia cht oxi hóa và cht kh trong hai cp oxi hóa – kh ca
kim loi
+ So sánh tính kh, tính oxi hóa ca các cp oxi – kh
+ Tính sut in ng chun ca pin in hóa
- Bit tính toán khi lưng, lưng cht liên quan vi quá trình in phân (tính toán theo phương
trình in phân và tính toán theo s vn dng nh lut Faraday)
- Thc hin ưc nhng thí nghim chng minh tính cht ca kim loi, thí nghim v pin in
hóa và s in phân, nhng thí nghim v n mòn kim loi và chng n mòn kim loi
KIM LOI VÀ HP KIM
A – KIM LOI
I – V TRÍ CA KIM LOI TRONG BNG TUN HOÀN
- Nhóm IA (tr H), nhóm IIA: các kim loi này là nhng nguyên t s
- Nhóm IIIA (tr B), mt phn ca các nhóm IVA, VA, VIA: các kim loi này là nhng nguyên t p
- Các nhóm B (t IB n VIIIB): các kim loi chuyn tip, chúng là nhng nguyên t d
- H lantan và actini (xp riêng thành hai hàng cui bng): các kim loi thuc hai h này là
nhng nguyên t f
* Nhn xét: a s các nguyên t hóa hc ã bit là nguyên t kim loi (trên 80 %)
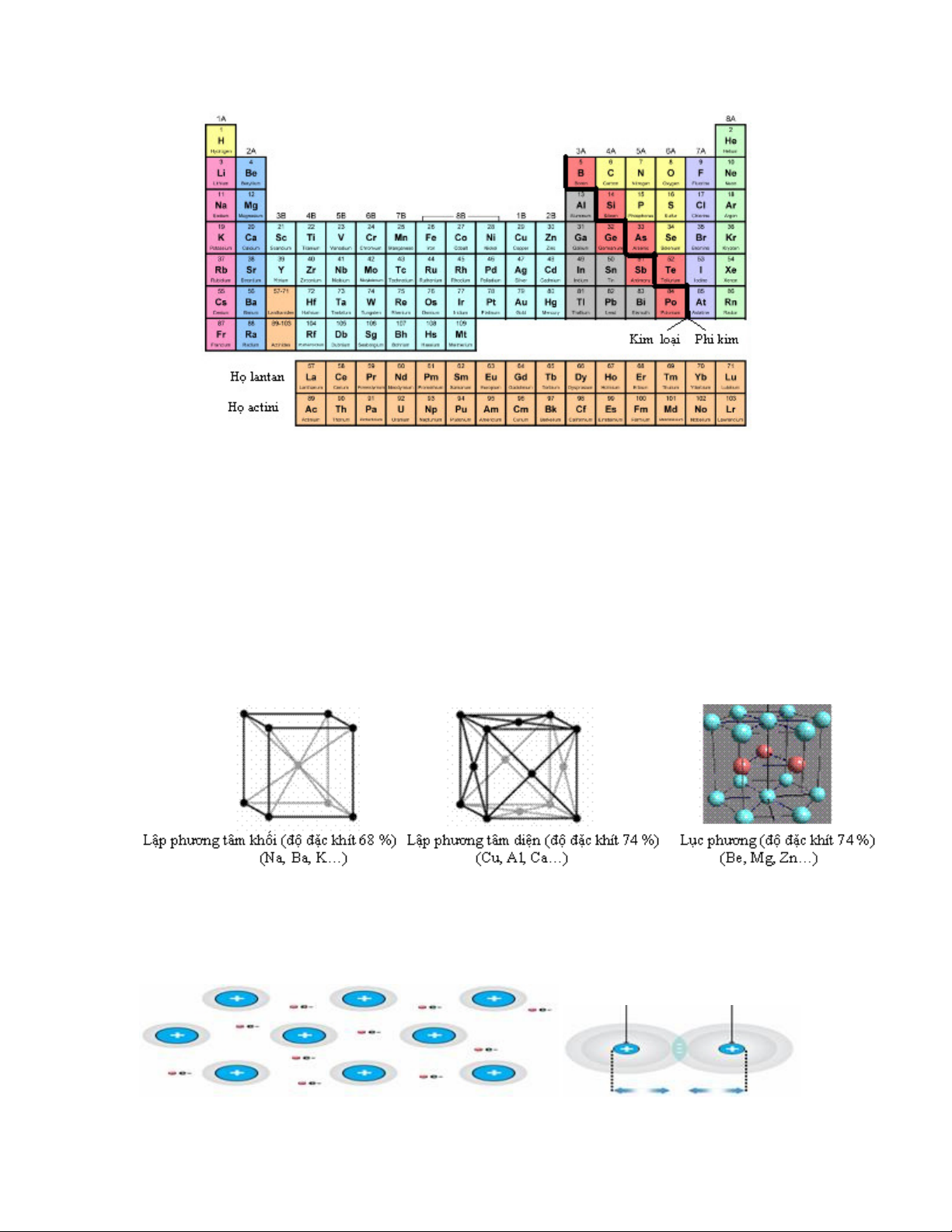
II – CU TO VÀ LIÊN KT TRONG TINH TH KIM LOI
1. Cu to nguyên t kim loi
- Hu ht các nguyên t kim loi có 1, 2 hoc 3 electron lp ngoài cùng
- Bán kính nguyên t ca các nguyên t kim loi ( phía dưi, bên trái bng tun hoàn) nhìn
chung ln hơn bán kính nguyên t các nguyên t phi kim ( phía trên, bên phi bng tun hoàn)
2. Cu to mng tinh th kim loi (SGK lp 10 trang 91)
Có ba kiu mng tinh th kim loi c trưng là lp phương tâm khi, lp phương tâm din và lc
phương
3. Liên kt kim loi
Là liên kt hóa hc hình thành bi lc hút tnh in gia ion dương kim loi n!m các nút mng
tinh th và các electron t do di chuyn trong toàn b mng lưi tinh th kim loi
Ion dương kim loi
Hút nhau

III – TÍNH CHT VT LÍ CA KIM LOI
1. Tính cht chung
Kim loi có nhng tính cht vt lí chung là: tính d"o, tính dn in, tính dn nhit và ánh kim
a) Tính do: các lp mng tinh th kim loi khi trưt lên nhau vn liên kt ưc vi nhau nh# lc
hút tnh in ca các electron t do vi các cation kim loi. Nhng kim loi có tính d"o cao là Au,
Ag, Al, Cu, Zn…
b) Tính dn in: nh# các electron t do có th chuyn d#i thành dòng có hưng dưi tác dng
ca in trư#ng. Nói chung nhit ca kim loi càng cao thì tính dn in ca kim loi càng
gim. Kim loi dn in tt nht là Ag, tip sau là Cu, Au, Al, Fe…
c) Tính dn nhit: nh# s chuyn ng ca các electron t do mang nng lưng (ng nng) t
vùng có nhit cao n vùng có nhit thp ca kim loi. Nói chung kim loi nào dn in tt
thì dn nhit tt
d) Ánh kim: nh# các electron t do có kh nng phn x tt ánh sáng kh kin (ánh sáng nhìn
thy)
Tóm li: nhng tính cht vt lí chung ca kim loi như trên ch yu do các electron t do
trong kim loi gây ra
2. Tính cht riêng
a) Khi lng riêng: ph thuc vào khi lưng nguyên t, bán kính nguyên t và kiu cu trúc
mng tinh th. Li là kim loi có khi lưng riêng nh$ nht (d = 0,5 g/cm
3
) và osimi (Os) có khi
lưng riêng ln nht (d = 22,6 g/cm
3
). Các kim loi có khi lưng riêng nh$ hơn 5 g/cm
3
ưc
gi là kim loi nh% (như Na, K, Mg, Al…) và ln hơn 5 g/cm
3
ưc gi là kim loi nng (như Fe,
Zn, Pb, Cu, Ag, Au…)
b) Nhit nóng chy: ph thuc ch yu vào bn liên kt kim loi. Kim loi có nhit nóng
chy thp nht là Hg (–39
o
C, iu kin thư#ng t&n ti trng thái l$ng) và kim loi có nhit
nóng chy cao nht là W (vonfam, 3410
o
C)
c) Tính cng: ph thuc ch yu vào bn liên kt kim loi. Kim loi mm nht là nhóm kim loi
kim (như Na, K…do bán kính ln, cu trúc r'ng nên liên kt kim loi kém bn) và có nhng kim
loi rt cng không th d(a ưc (như W, Cr…)
IV – TÍNH CHT HÓA HC CHUNG CA KIM LOI
Tính cht c trưng ca kim loi là tính kh (nguyên t kim loi d) b oxi hóa thành ion dương):
M * Mn
+
+ ne

1. Tác dng vi phi kim
Hu ht các kim loi kh ưc phi kim in hình thành ion âm
Ví d: 4Al + 3O
2
2Al
2
O
3
2Fe + 3Cl
2
2FeCl
3
Hg + S * HgS
2. Tác dng vi axit
a) i vi dung dch HCl, H
2
SO
4
loãng:
M + nH
+
* Mn
+
+ n/2H
2
(M ng trưc hiro trong dãy th in cc chun)
b) i vi H
2
SO
4
c, HNO
3
(axit có tính oxi hóa mnh):
- Kim loi th hin nhiu s oxi hóa khác nhau khi phn ng vi H
2
SO
4
c, HNO
3
s+ t s oxi
hóa cao nht
- Hu ht các kim loi phn ng ưc vi H
2
SO
4
c nóng (tr Pt, Au) và H
2
SO
4
c ngui (tr
Pt, Au, Fe, Al, Cr…), khi ó S
+6
trong H
2
SO
4
b kh thành S
+4
(SO
2
) ; S
o
hoc S
-2
(H
2
S)
- Hu ht các kim loi phn ng ưc vi HNO
3
c nóng (tr Pt, Au) và HNO
3
c ngui (tr Pt,
Au, Fe, Al, Cr…), khi ó N
+5
trong HNO
3
b kh thành N
+4
(NO
2
)
- Hu ht các kim loi phn ng ưc vi HNO
3
loãng (tr Pt, Au), khi ó N
+5
trong HNO
3
b kh
thành N
+2
(NO) ; N
+1
(N
2
O) ; N
o
(N
2
) hoc N
-3
(NH
4
+)
- Các kim loi có tính kh càng mnh thư#ng cho sn phm kh có s oxi hóa càng thp. Các
kim loi như Na, K…s+ gây n, khi tip xúc vi các dung dch axit
Ví d: 2Fe + 6H
2
SO
4
(c) Fe
2
(SO
4
)
3
+ 3SO
2
+ 6H
2
O
4Mg + 5H
2
SO
4
(c) 4MgSO
4
+ H
2
S + 4H
2
O
Cu + 4HNO
3
(c) * Cu(NO
3
)
2
+ 2NO
2
+ 2H
2
O
3Cu + 8HNO
3
(loãng) * 3Cu(NO
3
)
2
+ 2NO + 4H
2
O
3. Tác dng vi dung dch mui
- iu kin kim loi M y ưc kim loi X ra kh$i dung dch mui ca nó:
+ M ng trưc X trong dãy th in cc chun
+ C M và X u không tác dng ưc vi nưc iu kin thư#ng
+ Mui tham gia phn ng và mui to thành phi là mui tan: xM (r) + nX
x+
(dd) * xM
n+
(dd) +
nX (r)
- Khi lưng cht r-n tng: .m/ = m
X to ra
– m
M tan
- Khi lưng cht r-n gim: .m0 = m
M tan
– m
X to ra
- H'n hp các kim loi phn ng vi h'n hp dung dch mui theo th t ưu tiên: kim loi kh
mnh nht tác dng vi cation oxi hóa mnh nht to ra kim loi kh yu nht và cation oxi
hóa yu nht
- Vi nhiu anion có tính oxi hóa mnh như NO
3
-, MnO
4
-,…thì kim loi M s+ kh các anion trong
môi trư#ng axit (hoc bazơ)
Ví d: - Khi cho Zn vào dung dch CuSO
4
ta thy lp b mt thanh k+m dn chuyn qua màu $
và màu xanh ca dung dch b nht dn do phn ng: Zn + CuSO
4
* ZnSO
4
+ Cu0
- Khi cho kim loi kim Na vào dung dch CuSO
4
ta thy có si bt khí không màu và xut hin
kt ta keo xanh do các phn ng: Na + H
2
O * NaOH + 1/2H
2
và CuSO
4
+ 2NaOH * Cu(OH)
2
0
+ Na
2
SO
4

- Khi cho bt Cu vào dung dch Cu(NO
3
)
2
có vài git HCl ta thy có khí không màu thoát ra và
hóa nâu trong không khí do phn ng: 3Cu + Cu(NO
3
)
2
+ 8HCl * 4CuCl
2
+ 2NO + 4H
2
O
4. Tác dng vi nưc
- Các kim loi mnh như Li, Na, K, Ca, Sr, Ba…kh nưc d) dàng nhit thư#ng theo phn
ng: M + nH
2
O * M(OH)
n
+ n/2H
2
. Kim loi Mg tan rt chm và Al ch1 tan khi dng h'n hng
(hp kim ca Al và Hg)
- Các kim loi trung bình như Mg, Al, Zn, Fe…phn ng ưc vi hơi nưc nhit cao to
oxit kim loi và hiro
Ví d: Mg + H
2
O
(h)
MgO + H
2
3Fe + 4H
2
O
(h)
Fe
3
O
4
+ 4H
2
Fe + H
2
O
(h)
FeO + H
2
- Các kim loi có tính kh yu như Cu, Ag, Hg…không kh ưc nưc dù nhit cao
5. Tác dng vi dung dch ki m
Các kim loi mà hiroxit ca chúng có tính lư2ng tính như Al, Zn, Be, Sn, Pb…tác dng ưc vi
dung dch kim (c). Trong các phn ng này, kim loi óng vai trò là cht kh, H
2
O là cht oxi
hóa và bazơ làm môi trư#ng cho phn ng
Ví d: phn ng ca Al vi dung dch NaOH ưc hiu là phn ng ca Al vi nưc trong môi
trư#ng kim và g&m hai quá trình: 2Al + 6H
2
O * 2Al(OH)
3
+ 3H
2
Al(OH)
3
+ NaOH * Na[Al(OH)
4
]
Cng hai phương trình trên ta ưc mt phương trình:
2Al + 6H
2
O + 2NaOH * 2Na[Al(OH)
4
] + 3H
2
6. Tác dng vi oxit kim loi
Các kim loi mnh kh ưc các oxit kim loi yu hơn nhit cao thành kim loi
Ví d: 2Al + Fe
2
O
3
2Fe + Al
2
O
3
B – HP KIM
I – !NH NGH"A, CU TO TINH TH CA HP KIM
1. !nh ngha
Hp kim là vt liu kim loi có cha mt kim loi cơ bn và mt s kim loi hoc phi kim khác
Ví d: Thép là hp kim ca s-t vi cacbon và mt s nguyên t khác. uyra là hp kim ca
nhôm vi &ng, magie, mangan, silic
2. Cu to tinh th ca h#p kim
Hp kim có cu to tinh th. Có các loi tinh th sau: tinh th h'n hp, tinh th dung dch r-n và
tinh th hp cht hóa hc
a) Tinh th hn hp:
- Có ngu&n gc t khi h'n hp các ơn cht trong hp kim trng thái l$ng. 3 trng thái này,
các ơn cht không tan vào nhau và c(ng không tác dng hóa hc vi nhau
- Các ơn cht tham gia hp kim có tính cht hóa hc và kiu mng tinh th không khác nhau
nhiu, nhưng kích thưc các ion khác nhau.





![Siêu Vật Liệu: [Thêm thông tin chi tiết về loại siêu vật liệu hoặc ứng dụng của nó]](https://cdn.tailieu.vn/images/document/thumbnail/2011/20110820/thuyquynh21/135x160/sieu_vat_lieu_6413.jpg)
![Vật liệu mới thông minh (Phần 2): [Thêm thông tin chi tiết nếu có]](https://cdn.tailieu.vn/images/document/thumbnail/2011/20110728/bupbelen_238/135x160/5_7573.jpg)













![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



