
- 1 -
SÁNG KIẾN KINH NGHIỆM
ĐỀ TÀI:
RÈN LUYỆN TƯ DUY CHO HỌC SINH
BẰNG CÁC BÀI TẬP NHẬN BIẾT - TÁCH - TINH CHẾ

- 2 -
A. PHẦN MỞ ĐẦU
Bài tập Hoá học được các Giáo viên sử dụng khi giảng dạy Hoá học ở
các trường phổ thông, là một trong những phương pháp tốt nhất để rèn luyện tư
duy tái hiện kiến thức cũ cũng như để nhằm giải quyết các Bài tập nhanh, chính
xác. Một trong số các bài tập đó là nhận biết, tách và tinh chế các chất. Bài tập
loại này có nhiều điểm giống nhau, tuy nhiên cũng có nét riêng biệt, dựa vào
điểm giống nhau - khác nhau đó mà học sinh có các phương án để giải quyết.
Trước khi vào các bài tập ví dụ thì giáo viên cần ôn tập cho học sinh theo kiểu
bảng sơ đồ về đặc điểm chung, riêng của từng chất. Bài tập kiểu này được giáo
viên sử dụng khi giảng dạy hoặc ra đề thi nhằm đánh giá học sinh rất tốt vì ngoài
nắm vững kiến thức cơ bản thì học sinh cần phải có một kỹ năng tư duy tái hiện,
so sánh lựa chọn tốt.
Bài tập nhận biết và phân biệt các chất có nhiều điểm giống nhau. Tuy
nhiên có nét riêng biệt sau đây: Nhận biết có thể là một chất duy nhất nào đó
hoặc là một số riêng biệt ở trạng thái mất nhãn, cần dùng các biện pháp hóa lí
thích hợp để xác định chính xác tên của hóa chất. Khái niệm phân biệt bao hàm ý
so sánh (ít nhất phải có hai hóa chất trở lên) nhưng mục đích cuối cùng của phân
biệt cũng là để nhận biết tên của một số hóa chất nào đó. Tuy nhiên, trong khuôn
khổ giới hạn, bản thân chỉ tập trung đi sâu vào nội dung nhận biết.

- 3 -
B. PHẦN NỘI DUNG
1. Nguyên tắc và yêu cầu khi giải bài tập nhận biết.
- Để nhận biết các chất hóa học cần nắm vững tính chất lí hóa cơ bản của
chất đó, chẳn hạn: Trạng thái tồn tại, màu sắc, mùi vị, độ tan, độ nóng chảy, độ
sôi, các phản ứng hóa học đặc trưng có kèm theo dấu hiệu tạo kết tủa, hòa tan,
sủi bọt khí, thay đổi mời sắc… kể cả những chất do chúng tạo nên trong quá
trình nhận biết.
- Phản ứng hóa học được chọn để nhận biết là phản ứng đặc trưng đơn giản
và có dấu hiệu rõ rệt. Trừ trường học đặc biệt, thông thường muốn nhận biết n
hóa chất cần phải tiến hành (n – l) thí nghiệm.
- Tất cả các chất được lựa chọn dùng để nhận biết các chất theo yêu cầu của
đề bài, đều được coi là thuốc thử.
2. Phương pháp làm bài.
+ Bước 1: Trích mẫu thử (có thể đánh số các ống nghiệm để tiện theo dõi).
+ Bước 2: Chọn thuốc thử (tùy theo yêu cầu đề bài: thuốc thử tùy chọn, hạn
chế hay không dùng thuốc thử nào khác).
+ Bước 3: Cho thuốc thử vào mẫu, trình bày hiện tượng quan sát (mô tả) rút
ra kết luận đã nhận ra hóa chất nào.
+ Bước 4: Viết phương trình phản ứng minh họa.
Chú ý: Có thể gộp bước 2 và bước 3 thành một bảng phân biệt như sau:
Hóa chất cần nhận biết
Thuốc thử A B C …
X
…
Y
…
… …
Kết luận đã nhận ra (A) (B) (C) …
Hoặc dùng sơ đồ để nhận biết :
....
E
D
C
B
A
X
E
D
C
B
Y
E
D
C
Z
D
CTD
.C
B
A
2
)(OHBa
tan
&
- 4 -
3. Các dạng bài tập nhận biết thường gặp.
- Nhận biết các hóa chất (rắn, lỏng, khí) riêng biệt.
- Nhận biết các chất trong cùng một hỗn hợp.
- Xác định sự có mặt của các chất (hoặc các ion) trong cùng một dung dịch.
Tùy theo yêu cầu của bài tập mà trong mỗi dạng lại có thể gặp 1 trong các
trường hợp sau:
- Nhận biết với thuốc tự do (tùy chọn)
- Nhận biết với thuốc thử hạn chế (có giới hạn)
- Nhận biết không được dùng thuốc thử bên ngoài).
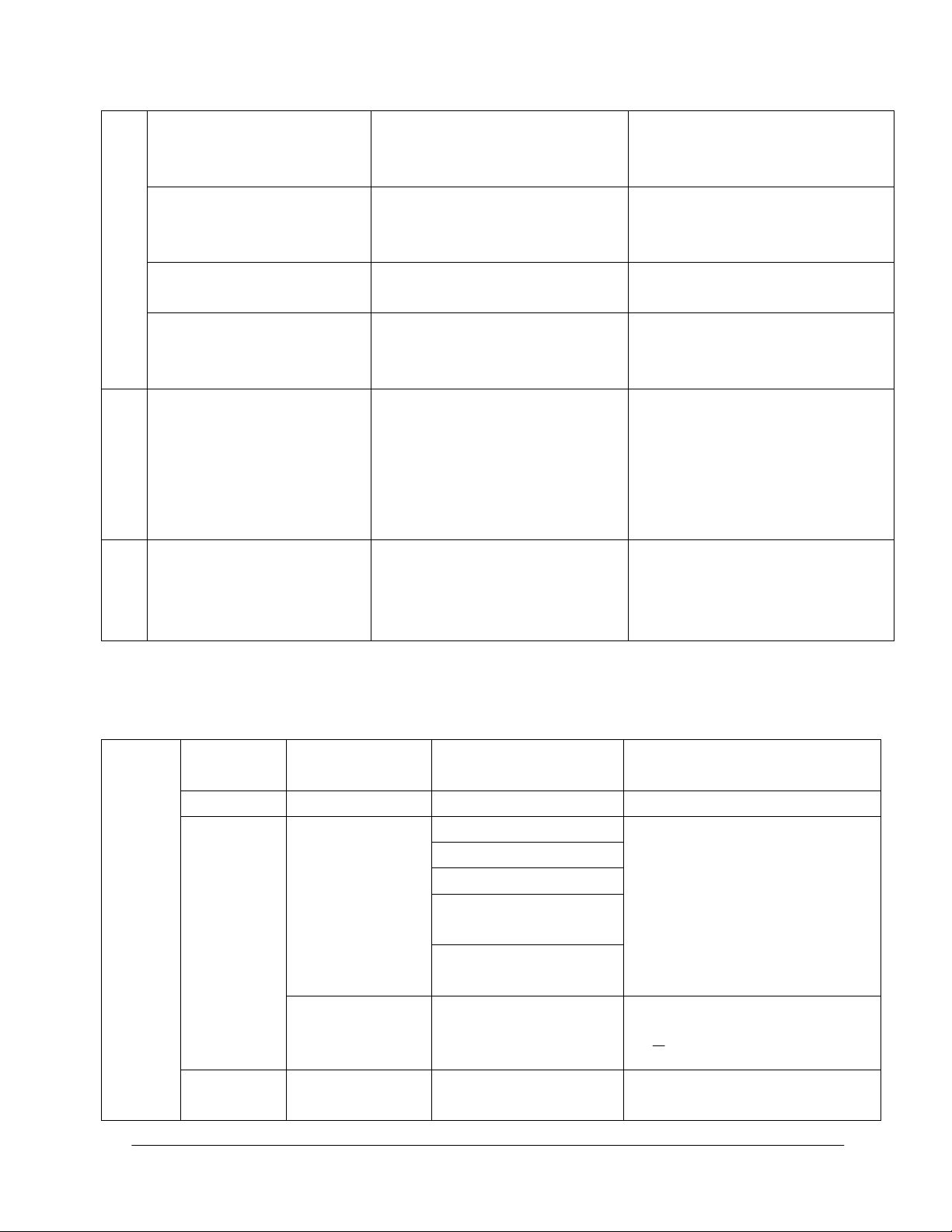
4. Một số thuốc thử vô cơ
a). Một số thuốc thử thông dụng.
TT
Thuốc thử Chất cần nhận biết Hiện tượng
1 Quỳ tím 1. Axit
2. Bazơ kiềm
1. Quỳ tím hóa đỏ
2. Quỳ tím hóa xanh
2 Phenolphtalein
(không màu)
Bazơ kiềm Không màu
màu hồng
3
Nước ( H20)
1. Các kim loại mạnh ( Li,
Na, K, Ca, Ba ).
2. Các oxit kim loại mạnh
(LiO, Na2O, K2O, CaO,
BaO)
3. Các muối của Na+, NO3
-
…
4. Khí NH3
5. Khí HCl, CO2, SO2,
SO3…
6. P2O5
1. Giải phóng H2 (riêng Ca
còn tạo dd đục Ca(OH)2)
2. Tan, tạo dung dịch làm
hồng phenolphtalein (riêng
CaO tạo dung dịch).
3. Tan
4. Tan,dd làm xanh quỳ tím
làm hồng phenolphtalein
5. Tan
dd làm đỏ quỳ
tím
6. Tan
dd làm đỏ quỳ
tím
Dung dịch axit
- Axit nhóm 1 ( tính
oxi hóa do ion H+) :
HCl, H2S04, H3PO4
,
RCOOH,…
1. Muối.
CO 22
3
2
3,, SSO
HCO
3, HSO
3. HS-…
2. Kim loại đứng trước
Hiđro
1. Tan
khí CO2, SO2,
H2S bay ra
2. Tan
Khí H2 bay ra
- Axit nhóm 2 ( tính
oxi hóa do ion gốc axit,
Hầu hết các kim loại (trừ
Tan
Khí NO
2
, SO
2
- 5 -
4
H
+
làm môi trường)
HNO3, H2SO4 đặc
nóng.
Au, Pt)
Axít clohiđric HCl
1. MnO2
2. Ag2O, muối Ag+
3. CuO
1. Khí Cl2 thoát ra
2. Kết tủa trắng AgCl
3. Dung dịch màu xanh
Axít sunfuric H2SO4 Ba, BaO, Ba(OH)2
muối Ba2+
Kết tủa trắng BaSO4
Axít HNO3
Fe, FeO, Fe3O4, FeS FeS2,
FeCO3, Fe(OH)2, CuS,
Cu
2
S...
Khí NO2, SO2, CO2 thoát ra.
5
Dung dịch bazơ (kiềm )
1. Kim loại Be, Zn, Pb, Al
2. Các chất BeO, ZnO,
PbO, Al2O3, Cr2O3,
Be(OH), Zn(OH)2,
Pb(OH)2, Al(OH)3,
Cr(OH)
3
1. Tan
khí H2 bay ra
2. Tan
6
Dung dịch muối
1. Ag+, Pb2+
2. Ba2+
3. Cd2+, Pb2+
1. ion Cl-
2. SO4
2-
3. S2-
1. AgCl trắng (PbCl2)
2. BaSO4trắng
3. CdSvàng, PbS đen
b). Thuốc thử cho một số hóa chất.
Kim loại
Chất cần
nhận biết
Thuốc thử Hiện tượng Phương trình phản ứng
(1) (2) (3) (4)
Li
K
Na
Ca
Ba
Đốt cháy
Ngọn lửa đỏ tia
Không phản ứng
Ngọn lửa tím
Ngọn lửa vàng
Ngọn lửa màu đỏ
da cam
Ngọn lửa màu vàng
lục
H2O dd trong + H2
(với Ca dd đục)
M + nH2O
M(OH)n +
+
2
nH2
Be
Zn
Dd OH
-
(NaOH,
Tan + H
2
M + (4-n)OH
-
+(n-2)H2O
















