1
I,Chất hoạt động bề mặt dựa trên saccharide
A,Giới thiệu:
Có nhiều lý do để chất hoạt động bề mặt dựa trên saccharide được sử dụng ngày càng
tăng trong hai thập kỷ qua. Giả sử sự phát triển bền vững của nền văn minh chúng ta đòi
hỏi rằng tỷ lệ suy giảm các nguồn tài nguyên khó phục hồi, chẳng hạn như nhiên liệu hóa
thạch và khoáng chất, nên được làm chậm lại . Điều này có nghĩa là cơ sở tài nguyên đó
của nhân loại phải được bảo tồn và nâng cao . Trong bối cảnh này, nhiên liệu sinh học có
vẻ là có giá trị lớn như là một nguyên liệu cho ngành công nghiệp hóa chất. Các thành
phần chính là mono-và polysaccharides,và tinh bột. Lợi thế lớn của họ trên nguyên liệu
hóa dầu là chúng không gây nguy hiểm đáng kể về mặt độc tính cấp tính hoặc mãn tính
đến sức khỏe con người và môi trường. Đây là lý do tại sao hóa chất dựa trên saccharide
đáp ứng yêu cầu môi trường đối với nguyên liệu: họ dễ phân hủy sinh học, và thỏa mản
các nguyên tắc của hóa học xanh. Mono-Disaccharides là những chất cao phân tử. Chúng
được sản xuất với khối lượng lớn, với độ tinh khiết cao, và tương đối rẻ . Họ có thể được,
dùng làm chất nền ưa nước để tổng hợp của bề mặt nonion. Năm 1999, sản xuất trên toàn
thế giới đã được khoảng 3,6-3.800.000 tấn, nghĩa là,gần khoảng 38% tổng sản lượng chất
hoạt động bề mặt , chiếm tới ba phần tư số nhiên liệu sinh học của thế giới. Người ta ước
tính rằng khoảng 400 tỷ tấn đường được sản xuất hàng năm.
-Phần lớn các chất HĐBM nonion thường được oligooxythylene và oxypropylene chuỗi
có chứa các hợp chất thu được trong phản ứng của oxirane (ethylene oxit) hoặc
methyloxirane (propylene oxit) với đầu kỵ nước trung gian có chứa một nhóm chức có
chứa một nhóm chức với một nguyên tử hydro đang hoạt động.Chỉ gần đây, các phản ứng
trực tiếp của oxirane với este methyl acid béo trong sự hiện diện của chất xúc tác không
đồng nhất được báo cáo. Tuy nhiên, oxirane, một chất khí không màu hoặc lỏng, là độc
hại, dễ bắt lửa, nổ và phân hủy thành carbon monoxide và methane. Hơn nữa, nó có thể
polymer hóa sự hiện diện của các phân tử tập trung và tỏa một lượng lớn nhiệt. Vì vậy,
một oxirane có thể gây nguy hiểm cho người dân và cả môi trường
Đối với tất cả những lý do này,thì dễ tiếp cận nhất là Disaccharides-glucose, fructose,
sacharose, lactose, maltose, và cellobioseseem được coi là những nguyên liệu có giá trị,
thay thế cho oxirane, để tổng hợp chất hoạt động dạng nonion. Trong thực tế, nó gần đây
đã được báo cáo rằng 63 sản phẩm chính của bề mặt được thương mại hóa, 14 được dựa
hoàn toàn vào vật liệu tái sinh (bao gồm cả đường este axit béo, polyglycosides alkyl, và
glucamides alkyl), và 21 được làm từ hóa dầu và nguyên liệu tự nhiên. Hơn nữa, báo cáo
chỉ ra rằng sự tăng trưởng của tiêu dùng chất hoạt động bề mặt carbohydrate ở phía tây
Châu Âu tăng từ khoảng 20.000 tấn trong những năm 1990 đến 60.000 tấn vào đầu năm
1997.
Trong chất hoạt động bề mặt dựa trên saccharide, một nửa số carbohydrate được gắn vào
một đầu kỵ nước, bình thường trong chuỗi hydrocarbon của một axit béo chuỗi dài rượu
béo hay amin béo, bởi một trong hai nguyên tử oxy (như trong đường este axit béo, trong
alkylpolyglycosides, hoặc, như báo cáo gần đây, trong vòng acetal-loại chất hoạt động bề
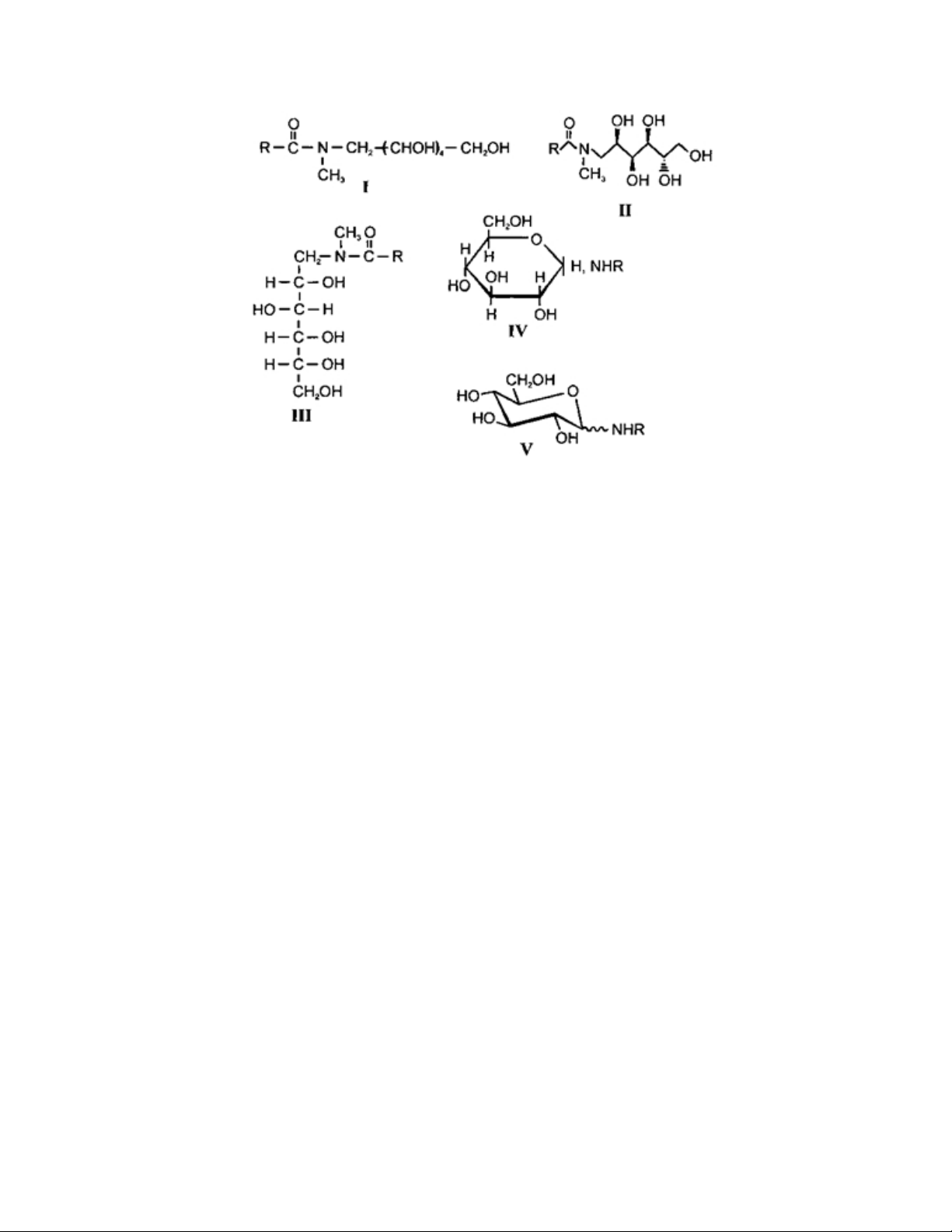
mặt từ đường) hoặc do nguyên tử nitơ (như trong alkylaldosyl-N-amin và dẫn xuất của
họ, N-alkanoyl-N-methylglucamines, và N-alkylaldo namides. Đường, acid béo, este rơi
vào các lớp bề mặt este polyol. Tổng hợp của họ là một ví dụ về sự tổng hợp Nonselective