SỞ GD & ĐT QUẢNG NAM
TRƯỜNG THPT TỐ HỮU
KIỂM TRA GIỮA KÌ 1 – NĂM HỌC 2024 - 2025
MÔN HÓA HỌC 10 - LỚP 10
Thời gian làm bài : 45 Phút; (Đề có 28 câu)
(Đề có 4 trang)
Họ tên : ............................................................... Số báo danh : ...................
Mã đề 102
ĐIỂM LỜI PHÊ CỦA GIÁO VIÊN
I. Trắc nghiệm (7 điểm) Hãy chọn và khoanh tròn đáp án đúng nhất
Câu 1: Theo nguyên lý Pauli, số electron tối đa trên mỗi orbital là
A. 14. B. 10. C. 6. D. 2.
Câu 2: Trong tự nhiên oxygen có 3 đồng vị 16O, 17O và 18O, copper có 2 đồng vị 65Cu và 63Cu. Số
kiểu phân tử copper (I) oxide (Cu2O) tối đa có thể tạo thành từ các đồng vị trên là
A. 12. B. 18. C. 6. D. 9.
Câu 3: Tên gọi và số electron tối đa ở lớp thứ 3 trong lớp vỏ nguyên tử là
A. lớp M, có tối đa 18 electron. B. lớp N, có tối đa 32 electron.
C. lớp K, có tối đa 2 electron. D. lớp L, có tối đa 8 electron.
Câu 4: “p” là viết tắt của hạt nào trong thành phần nguyên tử?
A. Proton. B. Electron. C. Notron. D. Neutron.
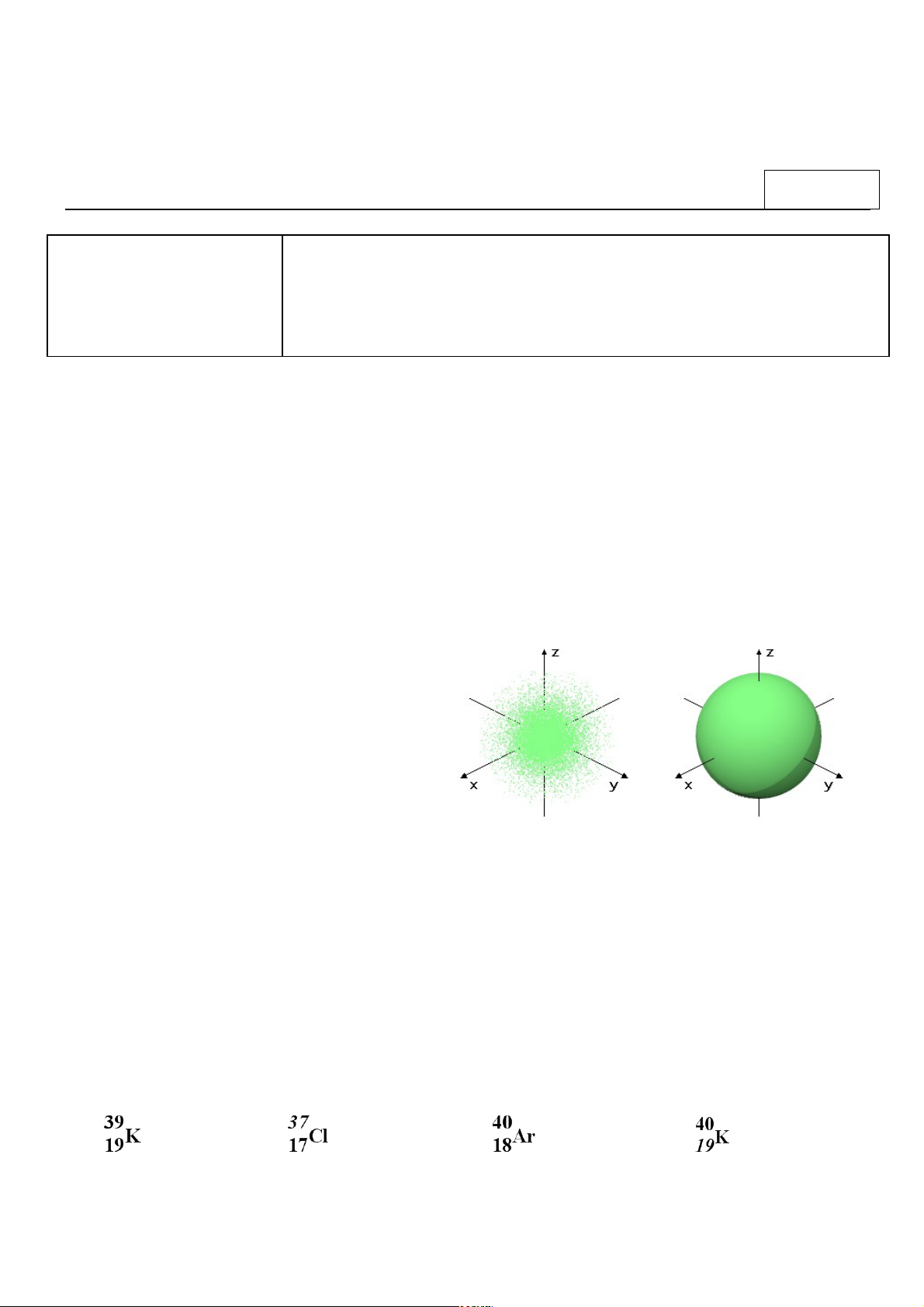
Câu 5: Quan sát hình ảnh bên và cho biết hình
ảnh này mô tả loại orbital nào của nguyên tử?
A. Orbital s. B. Orbital p.
C. Orbital d. D. Orbital f.
Câu 6: : Phát biểu nào sau đây không đúng?
A. Hạt nhân nguyên tử cấu thành từ các hạt proton và neutron.
B. Nguyên tử được cấu thành từ các hạt cơ bản là proton, neutron và electron.
C. Vỏ nguyên tử cấu thành từ các hạt electron.
D. Nguyên tử có cấu trúc đặc khít, gồm vỏ nguyên tử và hạt nhân nguyên tử.
Câu 7: Cho các nguyên tử:
26
13
X
,
26
12
Y
,
24
12
Z
. Phát biểu nào sau đây đúng?
A. Y và Z là các đồng vị của cùng một nguyên tố hóa học.
B. X và Y là các đồng vị của cùng một nguyên tố hóa học.
C. X, Y, Z là các đồng vị của cùng một nguyên tố hóa học.
D. X và Z là các đồng vị của cùng một nguyên tố hóa học.
Câu 8: Nguyên tử nào sau đây chứa 19 electron; 19 proton và 20 neutron?
A. . B. . C. . D. .
Câu 9: Ở lớp thứ hai (n=2) có bao nhiêu phân lớp electron?
A. 4. B. 1. C. 3. D. 2.
Trang 1/4 - Mã đề 102

Câu 10: Nguyên tố hóa học là những nguyên tử có cùng
A. số proton. B. số khối. C. số neutron và số proton. D. số neutron.
Câu 11: Trường hợp nào sau đây có sự tương ứng giữa hạt cơ bản với khối lượng và điện tích của
chúng?
A. Electron, m ≈ 1 amu, q = -1. B. Proton, m ≈0,00055 amu, q=+1.
C. Neutron, m ≈ 1 amu, q = 0. D. Hạt nhân, m ≈ 2 amu, q = +1.
Câu 12: Chỉ tiêu tự khâu dùng để khâu vết thường là sản phẩm nghiên cứu hoá học dùng trong lĩnh
vực
A. xây dựng. B. y khoa. C. mỹ phẩm. D. nông nghiệp.
Câu 13: Phát biểu nào sau đây là không đúng?
A. Số lượng proton và electron trong nguyên tử là bằng nhau.
B. Proton và electron là các hạt mang điện, neutron là hạt không mang điện.
C. Khối lượng của proton lớn hơn rất nhiều so với khối lượng của neutron.
D. Electron tạo nên lớp vỏ nguyên tử.
Câu 14: Orbital nguyên tử là
A. đám mây chứa electron có dạng hình số 8 nổi.
B. đám mây chứa electron có dạng hình cầu.
C. quỹ đạo chuyển động của electron quay quanh hạt nhân có kích thước năng lượng xác định.
D. khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron lớn nhất.
Câu 15: Một nguyên tử X có 17 electron và 20 neutron. Kí hiệu của nguyên tử X là
A.
34
17
X. B.
20
17
X. C.
37
17
X. D.
54
17
X.
Câu 16: Số electron độc thân của nguyên tử X có cấu hình electron là
A. 1. B. 11. C. 2. D. 7.
Câu 17: Tên gọi của orbital tương ứng với hình dạng trong hình sau là
A. px. B.py. C.pz. D. s.
Câu 18: Nội dung nào dưới đây không phải là đối tượng nghiên cứu của Hóa học?
A. Sự lớn lên và sinh sản của tế bào. B. Tính chất, sự biến đổi chất.
C. Thành phần, cấu trúc của chất. D. Ứng dụng của chất.
Câu 19: Mendeleev sắp xếp các nguyên tố vào bảng dựa trên
A. mối liên hệ giữa khối lượng nguyên tử và tính chất các nguyên tố tương ứng.
B. thời điểm khám phá ra nguyên tố hóa học.
C. tên gọi của các nguyên tố hóa học.
D. cấu trúc của nguyên tử các nguyên tố hóa học.
Câu 20: Một nguyên tố hóa học X ở chu kì 3, nhóm VIA. Cấu hình electron của nguyên tử X là
A. 1s22s22p63s23p4. B. 1s22s22p43s23p6. C. 1s22s22p63s23p2. D. 1s22s22p63s13p5.
Trang 2/4 - Mã đề 102

Câu 21: Nguyên tử của nguyên tố M có số hiệu nguyên tử bằng 17. Vị trí của M trong BTH là
A. ô 17, chu kì 3, nhóm VIIA. B. ô 17, chu kì 3, nhóm VIIB.
C. ô 17, chu kì 3, nhóm VB. D. ô 17, chu kì 3, nhóm VA.
Câu 22: Khối lượng nguyên tử tập trung hầu hết ở đâu?
A. Hạt nhân nguyên tử. B. Vỏ nguyên tử.
C. Electron. D. Neutron.
Câu 23: Sắp xếp các orbital sau 3s, 3p, 3d, 4s theo thứ tự mức năng lượng tăng dần:
A. 3s < 3p < 3d < 4s. B. 3s < 3p < 4s < 3d.
C. 3s < 4s < 3p < 3d. D. 3p < 3s < 3d < 4s.
Câu 24: Cho các phát biểu sau:
(1) Tất cả các hạt nhân nguyên tử đều đều chứa proton và neutron.
(2) Khối lượng nguyên tử tập trung phần lớn ở lớp vỏ.
(3) Trong nguyên tử, số electron bằng số proton.
(4) Trong hạt nhân nguyên tử, hạt mang điện là proton và electron.
(5) Trong nguyên tử, hạt electron có khối lượng không đáng kể so với các hạt còn lại.
Số phát biểu sai là
A. 1. B. 3. C. 2. D. 4.
Câu 25: Nguyên tử của nguyên tố Potassium có 19 electron. Ở trạng thái cơ bản, Potassium có số
orbital chứa electron là
A. 9. B. 11. C. 8. D. 10.
Câu 26: Cho biết đâu là hiện tượng hóa học trong các hiện tượng sau:
A. dẫn khí Carbon dioxide vào nước vôI trong làm nước vôi trong bị vẩn đục.
B. nhựa đường nấu ở nhiệt độ cao bị nóng chảy.
C. nước đá để ngoài không khí bị chảy thành nước lỏng.
D. thanh sắt nung nóng, dát mỏng và uốn cong được.
Câu 27: Sulfur dạng kem bôi được sử dụng để điều trị mụn trứng cá. Nguyên tử sulfur có phân lớp
electron ngoài cùng là 3p4. Phát biểu nào sau đây sai khi nói về nguyên tử sulfur?
A. Lớp ngoài cùng của sulfur có 6 electron.
B. Trong bảng tuần hoàn sulfur nằm ở chu kì 3.
C. Sulfur nằm ở nhóm VIA.
D. Hạt nhân nguyên tử sulfur có 16 electron.
Câu 28: Số electron tối đa trên phân lớp p là
A. 2. B. 10. C. 6. D. 14.
II. Tự luận (3 điểm)
Phần chung
Câu 1: (2 điểm) Lithium (Z=3) là nguyên tố có nhiều công dụng, được sử dụng trong chế tạo máy
bay và một số loại pin nhất định. Pin Lithium – Ion đang ngày càng phổ biến, nó cung cấp năng
lượng cho cuộc sống của hàng triệu người mỗi ngày thông qua các thiết bị như máy tính xách tay,
điện thoại di động, xe Hybrid, xe điện, … nhờ trọng lượng nhẹ, cung cấp năng lượng cao và khả năng
xạc lại.
a. Viết cấu hình electron nguyên tử của nguyên tố lithium và cho biết nó là kim loại, phi kim hay
khí hiếm (giải thích ngắn gọn).
b. Xác định vị trí của lithium (ô, chu kì, nhóm) trong bảng tuần hoàn, giải thích.
c. Viết cấu hình electron theo orbital của nguyên tử lithium? Cho biết lithium có bao nhiêu
electron độc thân.
d. Tỉ lệ phần trăm số nguyên tử các đồng vị của lithium được xác định theo phổ khối lượng như
hình dưới (hình 2.6).
Trang 3/4 - Mã đề 102

Tính nguyên tử khối trung bình của của lithium.
Phần riêng (Dành cho 10C1)
Câu 2: (1 điểm) Trong thể dục thể thao, có một số vận động viên sử dụng các loại chất kích thích
trong thi đấu, gọi là doping, dẫn đến thành tích đạt được của họ không thật so với năng lực vốn có.
Một trong các loại doping thường gặp nhất là testosterone tổng hợp.
Tỉ lệ giữa hai đồng vị (98,98%)
và (1,11%) là không đổi đối với
testosterone tự nhiên trong cơ thể. Trong khi
testosterone tổng hợp (tức doping) có phần
trăm số lượng đồng vị ít hơn
testosterone tự nhiên. Đây chính là mấu chốt
của xét nghiệm CIR (Carbon Isotope Ratio – Tỉ lệ đồng vị carbon) một xét nghiệm với mục đích xác
định xem vận động viên có sử dụng doping hay không. Giả sử phân tích CIR của một vận động viên
thu được kết quả phần trăm đồng vị là x và là y. Từ tỉ lệ đó, người ta tính được nguyên tử khối
trung bình của nguyên tố carbon trong mẫu phân tích có giá trị là 12,0198.
Với kết quả thu được, em có nghi ngờ vận động viên này sử dụng doping hay không? Vì sao?
------ HẾT ------
(Học sinh không được sử dụng Bảng tuần hoàn các nguyên tố hóa học)
Trang 4/4 - Mã đề 102






![Đề thi giữa học kì 1 môn Hóa học lớp 10 năm 2022-2023 - Trường THPT Phan Đình Giót, Điện Biên [Có đáp án]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250526/viyuhi/135x160/7101748229497.jpg)



















