
Động học của phản ứng enzyme trong trường hợp
không
có chất kìm hãm.
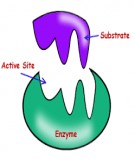
6.1.1. Ở giai đoạn: E + S ES
K+1: hằng số vận tốc của phản ứng thuận.
K-1: hằng số vận tốc của phản ứng nghịch.
Gọi V1 là tốc độ phản ứng thuận.
V-1 là tốc độ phản ứng nghịch.
[E]: nồng độ enzyme.
[S]: nồng độ cơ chất.
Ta có: V1 = K+1 ([E]. [S])
V-1 = K-1 [ES] (1)
Khi phản ứng đạt đến cân bằng (enzyme phản ứng
hết với cơ
chất) thì V1 = V-1 nghĩa là:
K+1([E]. [S]) = K-1[ES]

K+1
E + S ES
K-1
47
từ đó ta có:
1
1
K
K
=
ES
E S
Nếu gọi Ks là hằng số cân bằng các phản ứng bậc I,
ta có:
s K =

ES
E .S s K =
1
1
K
K
(2)
* Nếu Ks có giá trị lớn thì K-1 sẽ lớn và K+1 sẽ nhỏ.
Từ đó ta
thấy phức hợp ES dễ phân giải thành các chất S và E.
Phản ứng
enzyme tiến hành chậm.
* Nếu Ks có giá trị nhỏ thì tốc độ tạo ES sẽ nhanh
đồng thời
phản ứng enzyme cũng tiến hành nhanh. Vậy nếu Ks
càng nhỏ thì

nồng độ ES càng cao.
giai đoạn 1 ta đã tính được: s K =
ES
E S
Hay viết dưới dạng khác là: [E] [S] = Ks[ES]
(3)
Nếu gọi [Eo] là nồng độ chung của enzyme trước khi
bắt đầu
tham gia phản ứng.
[E]: nồng độ enzyme ở dạng tự do (không tạo phức
hợp)
[ES]: nồng độ của phức hệ ES.
thì nồng độ enzyme không tạo phức hợp (ở dạng tự
do) là:
[E] = [Eo] - [ES] (4)
Thay vào phương trình (3), ta có:

([Eo ] - [ES]). [S] = Ks. [ES]
Triển khai:
[Eo ] [S] - [ES] [S] = Ks. [ES] hay là:
Ks [ES] + [ES] [S] = [Eo] [S] hay là:
[ES](Ks + [S]) = [Eo] [S]
Từ đó
[ES] = [Eo ]
K S
S
s
o E
ES =
K S
S
s


![Ứng dụng của enzyme: Tổng hợp, phân tích [năm]](https://cdn.tailieu.vn/images/document/thumbnail/2015/20151110/thuaco/135x160/1557937712.jpg)



![Vector chuyển gen plasmid là gì? [Hướng dẫn chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2013/20130923/butmaulam/135x160/7661379933030.jpg)


![Enzyme giới hạn và hệ thống hạn chế - Cải biên, [Thông tin chi tiết/ Nghiên cứu mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2013/20130923/butmaulam/135x160/9721379933076.jpg)








![Giáo trình thí nghiệm Hợp chất tự nhiên trong y sinh [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260406/hoahongxanh0906/135x160/39941775556306.jpg)

![Tài liệu giảng dạy Sinh học và di truyền [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260323/hoatudang2026/135x160/42181774414220.jpg)

![Giáo trình Công nghệ vi sinh (Nghề Công nghệ sinh học TC/CĐ) - Trường Cao đẳng Đà Lạt [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260224/hoacattuong2026/135x160/87621772161812.jpg)


