35
TỔNG QUAN Y VĂN
Thuốc mới trong điều trị cho bệnh nhân ung thư
biểu mô buồng trứng: Đâu là nhu cầu y khoa
chưa được đáp ứng?
Võ Thanh Nhân*
Tóm tắt
Liệu pháp điều trị bước 1 cho bệnh nhân ung thư biểu mô buồng trứng (UTBMBT) bao gồm
phác đồ hóa trị có chứa Platinum/Taxane, những bệnh nhân UTBMBT tái phát cũng có đáp
ứng tốt với phác đồ hóa chất chứa Platinum. Các thuốc đơn chất, gây độc tế bào, không chứa
platinum thường được sử dụng để điều trị những bệnh nhân tái phát kháng platinum, nhưng
những thuốc này thường có độc tính và tỷ lệ đáp ứng thấp dưới 20%. Những tiến bộ của thuốc
nhắm trúng đích trong điều trị ung thư buồng trứng (UTBT) tái phát mang tới nhiều cơ hội
giúp cải thiện tỷ lệ đáp ứng và kéo dài thời gian sống còn không bệnh. Tuy vậy, việc lựa chọn
phác đồ điều trị cho từng bệnh nhân ở những giai đoạn khác nhau cũng rất phức tạp. UTBT
tiến xa và tái phát hiếm khi điều trị khỏi. Nhiều bước hóa trị có chứa platinum hay không
platinum đều không đáp ứng được nhu cầu điều trị do đó cần có nhiều liệu pháp điều trị hiệu
quả hơn. FDA Hoa Kỳ đã tạo cơ chế “phê duyệt cấp tốc” cho thuốc mới để có thể đáp ứng nhu
cầu điều trị đang rất thiếu. Bài viết sau tổng hợp các nghiên cứu lâm sàng hiện tại và mở ra
hướng mới trong thiết kế nghiên cứu và áp dụng các liệu pháp mới trong điều trị UTBT tái
phát.
Giới thiệu
Hơn 70% phụ nữ UTBT dạng biểu mô,
bao gồm cả ung thư ống dẫn trứng, ung
thư phúc mạc nguyên phát ở giai đoạn tiến
xa lúc chẩn đoán. Mặc dù nhiều bệnh
nhân ung thư giai đoạn tiến xa đáp ứng
hoàn toàn sau phẫu thuật giảm tổng khối
bướu và phác đồ hóa trị chứa platinum và
taxane, vẫn có 80% bệnh nhân sẽ tái phát.1
Mục tiêu chính trong các nghiên cứu là
kéo dài khoảng thời gian sống còn không
bệnh sau điều trị ban đầu và tăng tỷ lệ đáp
ứng cho bệnh nhân. Bài báo này đưa ra cái
nhìn chung của những nghiên cứu hiện tại
đề cập đến hai mục tiêu này và mở ra nhu
cầu chưa thể đáp ứng trong việc chọn lựa
điều trị.
Vai trò của điều trị duy trì như một
phần của điều trị ban đầu?
Hóa trị có chứa platinum vẫn là một lựa
chọn đầu tay cho phụ nữ UTBT giai đoạn
______________________________________________________________________________________________________________________________________
*Bv.Từ Dũ, DĐ: 0989043560
Email: nhanmaptd2016@gmail.com
tiến xa. Tuy nhiên, đã có những cuộc tranh
luận mạnh mẽ về vai trò của hóa trị duy trì
ở bệnh nhân đã có đáp ứng với hóa trị ban
đầu.1,2 Trong những năm 1990, các nghiên
cứu về hóa trị liệu chứa platinum kéo dài
(8-12 chu kỳ) cho thấy không có bằng
chứng cải thiện thời gian sống còn bệnh
không tiến triển (PFS- progression-free
survival) hoặc sống còn toàn bộ (OS-
overall survival) so với 5-6 chu kỳ hóa trị.2
Hơn nữa, phác đồ hóa trị chứa platinum
kéo dài có liên quan đến tăng độc tính.
Hai nghiên cứu (GOG-218 và ICON7) về
việc sử dụng chất kháng sinh mạch
bevacizumab để kéo dài PFS sau khi hóa trị
liệu bước một,3,4 bevacizumab đã được
thêm vào phác đồ hóa trị chuẩn (5 hoặc 6
chu kỳ carboplatin/paclitaxel) và đơn trị
liệu bevacizumab được tiếp tục (trong 12-
22 chu kỳ) sau khi ngừng hóa trị.3,4 Tuy
nhiên, theo dõi lâu dài nghiên cứu ICON7
không cho thấy sự cải thiện đáng kể PFS
hoặc OS trên toàn bộ dân số nghiên cứu,
mặc dù có bằng chứng cho thấy có lợi ích ở
những bệnh nhân nguy cơ cao.5 Nghiên cứu
GOG-218, có ba nhánh điều trị, tất cả đều

36
THỜI SỰ Y HỌC, Chuyên đề SỨC KHỎE SINH SẢN, Tập 20, Số 1, Tháng 6 – 2020
nhận được 6 chu kỳ carboplatin-paclitaxel.
Một nhánh sử dụng bevacizumab đồng thời
với hóa trị liệu, một nhánh sử dụng
bevacizumab đồng thời và kéo dài sau đó
(lên đến 22 chu kỳ) và nhánh thứ ba chỉ
nhận hóa trị. Bệnh nhân ở nhánh sử dụng
bevacizumab kéo dài có PFS dài nhất là
14,1 tháng, hơn đáng kể so với nhánh hóa
trị liệu đơn độc (10,3 tháng; Hazard ratio
HR: 0,717; Khoảng tin cậy 95% CI: 0,625
– 0,824; P <0,001).3 Trong cả hai nghiên
cứu, bevacizumab có liên quan đến tăng
nguy cơ tác dụng phụ, đặc biệt là biến cố
đường tiêu hóa và không nghiên cứu nào
cho thấy lợi ích về OS trên toàn bộ dân số
nghiên cứu.3 Vai trò của bevacizumab sử
dụng đồng thời với hóa trị hoặc duy trì sau
hóa trị vẫn có nhiều tranh cãi. SOLO1 là
nghiên cứu về olaparib đơn trị sử dụng duy
trì sau bước 1 hóa trị có platinum.
Ngoài ra, nghiên cứu ngẫu nhiên, pha 3,
PAOLA-1 (NCT02477644) olaparib kết
hợp bevacizumab so sánh giả dược kết hợp
bevacizumab trong điều trị duy trì ở những
bệnh nhân UTBT tiến xa sau khi dùng hóa
trị có platinum và bevacizumab ở bước 1.6
Olaparib và các thuốc ức chế Poly (ADP-
ribose) polymerase (PARPi) khác sẽ được
thảo luận chi tiết hơn bên dưới.
Ung thư buồng trứng tái phát
Lựa chọn điều trị UTBMBT tiến xa tái phát
thường dựa trên PFS. Khi thời gian đến khi
tiến triển là > 6 tháng sau khi chấm dứt hóa
trị có chứa platinum ban đầu, bệnh nhân
được coi là nhạy với platinum.
Ở những bệnh nhân này, hóa trị liệu có
chứa platinum kết hợp là lựa chọn điều trị
ưu tiên.7 Tỷ lệ đáp ứng với hóa trị có chứa
platinum kết hợp bước 2 ở những bệnh
nhân có khối u nhạy với platinum là
khoảng 50%-65%.8–10 Hóa trị kết hợp đã
được chứng minh có lợi thế hơn phác đồ
platinum đơn chất về cả PFS và OS.11 Khi
tiến triển sau liệu pháp điều trị bước 1 xảy
ra ít hơn 6 tháng sau khi ngừng hóa trị,
bệnh được coi là kháng platinum; khuyến
cáo điều trị bước hai ở những bệnh nhân
này bao gồm chủ yếu là hóa trị đơn chất
không chứa platinum, có thể cân nhắc kết
hợp bevacizumab hoặc pazopanib.7 Khi tiến
triển xảy ra trong quá trình hóa trị hoặc
trong vòng 1 tháng chấm dứt hóa trị, bệnh
nhân được coi là trơ với platinum.12
Cho đến những năm gần đây, về cơ bản
không có lựa chọn điều trị khác ngoài các
đợt hóa trị lặp đi lặp lại ở bệnh nhân có 2
bước hóa trị trở lên. Hơn nữa, gần như tất
cả các bệnh nhân cuối cùng cũng trở nên
kháng với phác đồ có chứa platinum.6 Như
vậy, khái niệm về độ nhạy platinum trở nên
ít quan trọng khi vượt quá 2 hoặc 3 bước
hóa trị. Bằng chứng hạn chế cho thấy khả
năng đáp ứng với phác đồ điều trị bằng
platinum giảm đáng kể sau 2 bước hóa trị,
ngay cả ở những bệnh nhân ban đầu nhạy
với platinum.
Gần đây, các thuốc nhắm trúng đích yếu tố
tăng trưởng nội mô mạch máu (VEGF; ví
dụ bevacizumab) và thuốc ức chế PARP (ví
dụ olaparib, rucaparib và niraparib) nổi lên
như là lựa chọn điều trị ở bệnh nhân ung
thư biểu mô buồng trứng tiến triển nhiều
bước hóa trị.13–24 Cả hai thuốc bevacizumab
và PARPi đều yêu cầu lựa chọn bệnh nhân
kĩ lưỡng.
Vai trò của thuốc ức chế PARP
trong điều trị UTBT tái phát?
Các nghiên cứu lâm sàng gần đây đã đánh
giá vai trò thuốc ức chế PARP (PARPi)
trong điều trị bệnh nhân UTBT tiến triển ở
hai hình thức khác nhau: 1) khi bệnh có tái
phát hoặc tiến triển sau 2 – 3 bước hóa trị
trở lên có chứa platinum và 2) khi bệnh
đang trong tình trạng đáp ứng sau khi hoàn
thành một đợt hóa trị có platinum (điều trị
duy trì). Một số nghiên cứu tiến hành trên
bệnh nhân có đột biến BRCA (dạng
germline hoặc somatic).
Vai trò của PARPi
trong điều trị duy
trì?
Cả olaparib25 và niraparib26 đều đã được
phê duyệt là liệu pháp duy trì ở những bệnh
nhân có đáp ứng hoàn toàn hoặc một phần
với hóa trị có chứa platinum.27–29 Trong
Nghiên cứu 19, pha 2, bệnh nhân trong

37
TỔNG QUAN Y VĂN
nhánh sử dụng olaparib có PFS dài hơn
đáng kể so với nhánh dùng giả dược (8,4 so
với 4,8 tháng; P <0,001).27 Phân tích dưới
nhóm theo tình trạng đột biến BRCA cho
thấy bệnh nhân có đột biến BRCA (dạng
germline hoặc somatic) có lợi ích lớn nhất
từ olaparib so với giả dược (PFS 11,2 so
với 4,3 tháng; P <0,001), tuy nhiên ngay cả
những bệnh nhân có BRCA wild-type vẫn
được hưởng lợi từ liệu pháp điều trị duy trì
olaparib (PFS 7,4 so với 5,5 tháng; P =
0,007).30 Mặc dù không có sự khác biệt
đáng kể về OS trên toàn bộ dân số, tuy
nhiên trên bệnh nhân có đột biến BRCA,
tái phát nhạy với platinum thì OS kéo dài
hơn khi được điều trị bằng olaparib.31
Nghiên cứu pha 3, SOLO-2 đã chứng minh
hiệu quả của viên nén olaparib trong điều
trị duy trì, đơn trị liệu ở những bệnh nhân
UTBT tái phát nhạy với platinum, có đột
biến gen BRCA dạng di truyền.29 Trong
nghiên cứu này, điều trị duy trì bằng
olaparib cải thiện rõ rệt PFS so với giả
dược. Bệnh nhân dùng olaparib không có
ảnh hưởng xấu về chất lượng cuộc sống so
với giả dược. Olaparib (so với giả dược)
cải thiện nhiều tiêu chí do bệnh nhân tự
đánh giá.32
Nghiên cứu niraparib, pha 3 (NOVA) thu
nhận và phân tầng bệnh nhân theo tình
trạng có hoặc không có đột biến BRCA
dạng germline (gBRCA).28 Trong nhóm có
đột biến gBRCA, điều trị niraparib cũng
cải thiện PFS dài hơn rõ rệt so với giả
dược.28 Thuốc ức chế PARP đang nổi lên
như một liệu pháp duy trì tiềm năng ở
những bệnh nhân UTBT đã đáp ứng với ít
nhất 2 bước hóa trị liệu có platinum trước
đó và đáp ứng (hoàn toàn hoặc một phần)
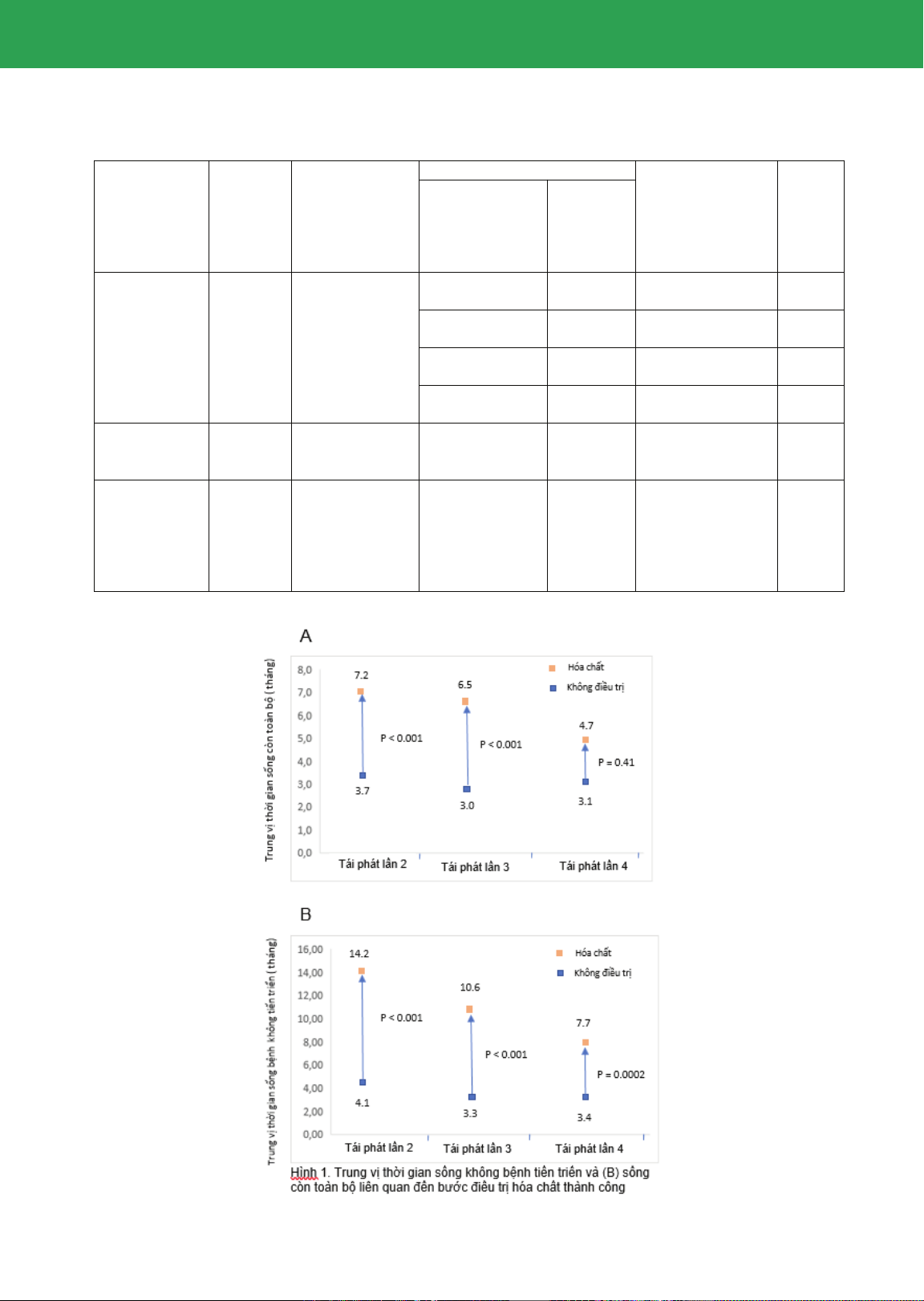
với liệu trình gần đây nhất.
(Bảng 1, Hình 1)
Bao nhiêu phần trăm bệnh nhân
UTBT tiến xa có đột biến BRCA?
Dữ liệu từ các nghiên cứu không lựa chọn
đặc điểm bệnh nhân UTBT cho thấy 5%-
18% trường hợp có đột biến gBRCA. Dữ
liệu hạn chế cho thấy có thêm 5%- 10%
phát sinh từ các đột biến BRCA sinh
dưỡng. Do đó, trong chẩn đoán ban đầu, tỷ
lệ bệnh nhân UTBT có liên quan tới đột
biến BRCA là khiêm tốn. Tuy nhiên,
những bệnh nhân mắc UTBT liên quan đến
đột biến BRCA có khả năng sống sót dài
hơn so với những người không mang đột
biến, một phần có thể do khả năng đáp ứng
tốt hơn với hóa trị liệu platinum. Do đó,
những bệnh nhân đã trải qua nhiều bước
hóa trị liệu có thể mang đột biến BRCA
nhiều hơn.
Triển vọng trong việc đáp ứng nhu
cầu điều trị của bệnh nhân nhận
nhiều hơn 3 bước điều trị?
Một số nghiên cứu đang thực hiện cho bệnh
nhân UTBT kháng platinum hoặc đã tiến
triển sau nhiều đợt điều trị, bao gồm đã hóa
trị nhiều hơn 3 bước. Nghiên cứu SOLO-3,
pha 3, đánh giá PFS giữa olaparib so với
hóa trị liệu không có platinum ở bệnh nhân
UTBT dạng thanh dịch, grade cao, nhạy
platinum hay ung thư dạng nội mạc tử cung
độ mô học cao, tiến triển sau > 6 tháng kể
từ khi ngừng liều điều trị platinum cuối
cùng, và đã nhận được 2 hoặc nhiều bước
hóa trị liệu có chứa platinum
(NCT02282020).
Để khẳng định độ nhạy và độ đặc hiệu của
xét nghiệm HRD và sự chính xác trong việc
tiên lượng đáp ứng với olaparib, nghiên
cứu LIGHT pha 2 (NCT02983799) đánh
giá hiệu quả và độ an toàn của olaparib ở
bệnh nhân UTBT tái phát nhạy cảm với
platinum, đã nhận được ≥2 bước hóa trị liệu
có chứa platinum. Bệnh nhân sẽ được phân
tầng bằng cách sử dụng các xét nghiệm di
truyền HRD khác nhau.
Kết luận
Hóa trị có chứa platinum được khuyến cáo
là điều trị bước một ở phụ nữ UTBMBT
tiến xa. Bevacizumab có thể có vai trò ở
một số đối tượng bệnh nhân UTBT chọn
lọc, bị tái phát, kết hợp với 5 phác đồ hóa
trị được phê duyệt. Đối với những bệnh
nhân có đáp ứng khách quan, khi điều trị
lại bằng hóa trị liệu chứa platinum, một
nghiên cứu giai đoạn 3 gần đây cho thấy
niraparib có thể kéo dài PFS khi được sử
dụng như đơn trị liệu duy trì.
38
THỜI SỰ Y HỌC, Chuyên đề SỨC KHỎE SINH SẢN, Tập 20, Số 1, Tháng 6 – 2020
Bảng 1. Nghiên cứu phase 3 của PARPi trong điều trị duy trì trên BN ung thư buồng trứng
tái phát nhạy với platinum
Số liệu
pháp
hóa
chất
trước
đó
Dấu ấn sinh
học
Trung vị PFS, tháng HR cho PFS
( 95% CI)
Giá trị
p
Liệu pháp so
sánh
Placebo
Niraparib
đơn trị
NOVA
≥2 Không có BN
được phân
tầng dựa trên
tinh trạng đột
biến gBRCA và
điểm HRD
gBRCA: 21,0 5,5 0,27 (0,17–0,41) <0,001
Non-gBRCA:
9,3
3,90,45 (0,34–0,61) <0,001
HRD-positive:
12,9
3,80,38 (0,24-0,59) <0,001
HRD-negative:
6,9
3,80,58 (0,36–0,92 0,02
Olaparib
đơn trị
SOLO-2
≥2
Đột biến
BRCA1/2
30,2 5,50,25 (0,18–0,35) <0,001
Rucaparib
đơn trị
ARIEL3
≥3 Không có BRCA
mutation: 16.6
HRD-positive:
13,6
ITT population:
10,8
5,4
5,4
5,4
0.23
0.32
0.36
<0.001
<0.001
<0.001

39
TỔNG QUAN Y VĂN
Nghiên cứu pha 3, SOLO-2 đã chứng minh
hiệu quả của viên nén olaparib đơn trị liệu
duy trì ở những bệnh nhân UTBT tái phát
nhạy với platinum, có đột biến gBRCA.
Hiện nay, lựa chọn điều trị cho những phụ
nữ bị UTBT tái phát thất bại từ > 2 bước
hóa trị rất hạn chế và nhiều bệnh nhân
không đủ điều kiện để nhận bevacizumab
hoặc thuốc ức chế PARP.29 Sự chấp thuận
nhanh chóng của FDA tạo cơ hội cho các
loại thuốc mới nhanh chóng được phê
duyệt để giải quyết các nhu cầu chưa được
đáp áp ứng trong điều
Dịch từ tài liệu:
Bringing new medicines to women
with epithelial ovarian cancer: what
is the unmet medical need? Thomas
J. Herzog and Bradley J. Monk,
Gynecologic Oncology Research
and Practice (2017) 4:13
Lời cảm ơn: Bài viết này được hỗ trợ từ
AstraZeneca cho mục đích giáo dục y khoa.
Từ viết tắt:
–UTBMBT: ung thư biểu mô buồng
trứng
–UTBT: Ung thư buồng trứng
–PARPi: thuốc ức chế enzyme Poly
(adenosine diphosphate-ribose)
polymerase
–gBRCA: Đột biến BRCA dòng mầm
–OS (overall survival): sống còn toàn bộ
–HRD (homologous recombination
deficiency): Thiếu hụt tái tổ hợp tương
đồng
–HR (hazard ratio): Tỷ số nguy cơ.
–HRQoL(health related quality of life):
Sức khỏe liên quan đến chất lượng
cuộc sống.
–95% CI (95% confident interval):
Khoảng tin cậy 95%.
–PFS (progression free survival): Thời
gian sống bệnh không tiến triển
–ITT (intent to treat): Có ý định điều trị.
–NR (not reported): Không báo cáo.
Tài liệu tham khảo
1) Korkmaz T, Seber S, Basaran G. Review of the
current role of targeted therapies as maintenance
therapies in first and second line treatment of
epithelial ovarian cancer; in the light of completed
trials. Crit Rev Oncol Hematol. 2016;98:180–8.
2) Markman M. Maintenance chemotherapy in the
management of epithelial ovarian cancer. Cancer
Metastasis Rev. 2015;34(1):11–7.
3) Burger RA, Brady MF, Bookman MA, Fleming GF,
Monk BJ, Huang H, et al. Incorporation of
bevacizumab in the primary treatment of ovarian
cancer. N Engl J Med. 2011;365(26):2473–83.
4) Perren TJ, Swart AM, Pfisterer J, Ledermann JA,
Pujade-Lauraine E, Kristensen G, et al. A phase 3
trial of bevacizumab in ovarian cancer. N Engl J
Med. 2011;365(26):2484–96.
5) Oza AM, Cook AD, Pfisterer J, Embleton A,
Ledermann JA, Pujade-Lauraine E, et al. Standard
chemotherapy with or without bevacizumab for
women with newly diagnosed ovarian cancer
(ICON7): overall survival results of a phase 3
randomised trial. Lancet Oncol. 2015;16(8):928–36.
6) Ray-Coquard IL, Harter P, Martin AG, Cropet C,
Pignata S, Fujiwara K, et al. PAOLA-1: An ENGOT/
GCIG phase III trial of olaparib versus placebo
combined with bevacizumab as
maintenancetreatment in patientswith advanced
ovarian cancer following first-lineplatinum-based
chemotherapy plus bevacizumab abstract and
poster presented at 2017 ASCO Annual Meeting. J
Clin Oncol. 2017;35(suppl):abstr TPS5605.
7) National Comprehensive Cancer Network. NCCN
Clinical Practice Guidelines in Oncology. Ovarian
Cancer Including Fallopian Tube Cancer and
Primary Peritoneal Cancer. Version 1.2016. https://
www.tri-kobe.org/nccn/guideline/
gynecological/english/ovarian.pdf. Accessed 15
March 2017.
8) Alberts DS, Liu PY, Wilczynski SP, Clouser MC,
Lopez AM, Michelin DP, et al. Randomized trial of
pegylated liposomal doxorubicin (PLD) plus
carboplatin versus carboplatin in platinum-sensitive
(PS) patients with recurrent epithelial ovarian or
peritoneal carcinoma after failure of initial
platinumbased chemotherapy (southwest oncology
group protocol S0200). Gynecol Oncol.
2008;108(1):90–4.
9) Parmar MK, Ledermann JA, Colombo N, du Bois A,
Delaloye JF, Kristensen GB, et al. Paclitaxel plus
platinum-based chemotherapy versus conventional
platinum-based chemotherapy in women with
relapsed ovarian cancer: the ICON4/AGO-OVAR-
2.2 Trial. Lancet. 2003;361(9375):2099–106.
10)
Pfisterer J, Plante M, Vergote I, du Bois A, Hirte H,
Lacave AJ, et al. Gemcitabine plus carboplatin
compared with carboplatin in patients with platinum-
sensitive recurrent ovarian cancer: an intergroup
trial of the AGO-OVAR, the NCIC CTG, and the
EORTC GCG. J Clin Oncol. 2006;24(29):4699–707.
11) Raja FA, Counsell N, Colombo N, Pfisterer J, du
Bois A, Parmar MK, et al. Platinum versus platinum-
combination chemotherapy in platinum-sensitive
recurrent ovarian cancer: a meta-analysis using
individual patient data. Ann Oncol.
2013;24(12):3028–34.
12) Pujade-Lauraine E, Combe P. Recurrent ovarian
cancer. Ann Oncol. 2016; 27(Suppl 1):i63–5.
13) Cannistra SA, Matulonis UA, Penson RT,
Hambleton J, Dupont J, Mackey H, et al. Phase II
study of bevacizumab in patients with platinum-
resistant ovarian cancer or peritoneal serous
cancer. J Clin Oncol. 2007;25(33):5180–6.












![Bài giảng Vi sinh vật: Đại cương về miễn dịch và ứng dụng [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20251124/royalnguyen223@gmail.com/135x160/49791764038504.jpg)