
TẠP CHÍ Y HỌC VIỆT NAM TẬP 490 - THÁNG 5 - SỐ 1 - 2020
229
HOÀN THIỆN KỸ THUẬT TÁCH DNA TỪ CÁC MẪU
BỆNH PHẨM SINH HỌC ĐỂ XÁC ĐỊNH ĐỘT BIẾN GEN BRAF V600E
Bùi Thị Lành*, Lê Anh Đức*, Bùi Minh Lý*, Đào Thị Luận*
Nguyễn Quang Trung*, Nguyễn Xuân Hậu*, Nguyễn Thị Trang*
TÓM TẮT59
BRAF là gen tổng hợp protein B-raf chịu trách
nhiệm kiểm soát hoạt động phát triển và phân chia
của nhiều loại tế bào trong cơ thể. Đột biến gen BRAF
làm cho các tế bào bất thường này nhân lên một cách
không kiểm soát và hình thành ung thư. Theo nhiều
nghiên cứu, đột biến tại codon 600 của exon 15
(V600E) là đột biến phổ biến nhất trên gen BRAF. Đột
biến này là nguyên nhân dẫn đến nhiều bệnh ung thư
trong đó có ung thư tuyến giáp. Mục tiêu: Hoàn
thiện kỹ thuật Realtime-PCR để xác định đột biến gen
BRAF V600E ở các mẫu bệnh phẩm bao gồm mẫu mô
phủ parafin, mẫu mô tươi, mẫu dịch hút tế bào và
mẫu máu của bệnh nhân theo dõi chẩn đoán ung thư
tuyến giáp. Đối tượng và phương pháp nghiên
cứu: 21 mẫu mô phủ parafin, 21 mẫu mô tươi, 22
mẫu dịch hút tế bào và 16 mẫu máu của bệnh nhân
theo dõi chẩn đoán ung thư tuyến giáp. Sử dụng kỹ
thuật Realtime-PCR để xác định đột biến gen BRAF
V600E từ các mẫu bệnh phẩm kể trên. Kết quả: Tỷ lệ
xuất hiện đột biến ở mẫu mô phủ parafin là 52,38%,;
mẫu mô tươi là 19,05%, mẫu dịch hút tế bào là
4,55%, mẫu máu là 0%. Kết luận: Hoàn thiện thành
công quy trình kỹ thuật Realtime-PCR để xác định đột
biến gen BRAFV600E từ các mẫu bệnh phẩm gồm
mẫu mô phủ parafin, mẫu mô tươi, mẫu dịch hút tế
bào và mẫu máu ở bệnh nhân theo dõi chẩn đoán ung
thư tuyến giáp.
Từ khóa:
Ung thư tuyến giáp, Realtime-PCR,
BRAF V600E.
SUMMARY
COMPLETE TECHNIQUES FOR DNA
EXTRACTION FROM BIOLOGICAL
SPECIMENS FOR DETERMINATION
MUTATION V600E OF GENE BRAF
Background: BRAF gene is known as a tumor
suppressor gene in Thyroid cancer (TC), which plays a
role in DNA repair. The mutation in BRAF have been
associated with different types of cancer. The present
study was aimed at studying the association between
BRAF V600E mutation and TC.Object: Complete the
Realtime-PCR technique to identify the BRAF V600E
gene mutation in patient samples including paraffin-
covered tissue samples, fresh tissue samples, fluid
aspirate samples and blood samples from patients
following diagnosis of thyroid cancer diagnosis.
Material and method:21 paraffin-covered tissue
*Trường Đại học Y Hà Nội
Chịu trách nhiệm chính: Nguyễn Thị Trang
Email: trangnguyen@hmu.edu.vn
Ngày nhận bài: 18.2.2020
Ngày phản biện khoa học: 13.4.2020
Ngày duyệt bài: 20.4.2020
samples were removed parafin by xylene, after that all
of samples extracted DNA by Qiagen kit. We analyzed
BRAFV600E mutation from 21 patients who had
anatomical diagnosis of papillary thyroid cancer, 21
fresh tissue samples were taken during surgery from
21 patients with cytologic results monitoring thyroid
cancer,22 fluid aspirated samplewere taken from 22
patients with suspected thyroid cancer who indicated
needle aspiration and 16 blood samples were taken
from 16 patients with other benign thyroid diseases
according to Realtime -PCR by BRAF V600E kit
(Rusian). Results: The prevalence of BRAF
V600Emutation was 52,38% , 19,05%, 4,55% and
0% fromparaffin-covered tissue sample,fresh tissue
sample, fluid aspirated sampleand blood sample
espectively. Conclusion: Complete techniques for
DNA extraction from biological specimens for
determination mutation V600E of gene BRAF.
Keywords:
Thyroid cancer, Realtime-PCR, BRAF
V600E.
I. ĐẶT VẤN ĐỀ
Ung thư tuyến giáp (UTTG) biệt hóa là ung
thư phổ biến nhất của hệ thống nội tiết. Trong
những thập kỷ gần đây, tỷ lệ mắc loại ung thư
này đã tăng gấp 3 lần [1,2]. Loại mô học phổ
biến nhất của ung thư tuyến giáp biệt hóa,
chiếm 80% -85% trong tất cả các trường hợp, là
ung thư tuyến giáp dạng nhú (PTC) [3]. PTC có
tiên lượng rất tốt và tỷ lệ sống 5 năm cao; tuy
nhiên, một số bệnh nhân không đáp ứng với
điều trị, cuối cùng dẫn đến tử vong. BRAF là một
phần của con đường tín hiệu tế bào MAPK, ngăn
chặn apoptosis và điều chỉnh sự tăng sinh cũng
như xâm lấn của khối u [3]. Trong các khuyến
nghị mới nhất của Hiệp hội Tuyến giáp Hoa Kỳ
(ATA), sự hiện diện của đột biến BRAF V600E là
một trong những yếu tố được tính đến trong
phân tầng nguy cơ của một nhóm lâm sàng PTC
tiên lượng xấu liên quan việc đáp ứng điều trị
I131 cũng như khả năng tái phát, di căn ở bệnh
nhân UTTG [4]. Đột biến này còn được biết đến
là một trong những dấu ấn phân tử giúp chẩn
đoán phát hiện UTTG với độ nhạy và độ đặc
hiệu tương ứng 80% và 99,7% khi kết hợp với
kỹ thuật chẩn đoán tế bào học[5] và hướng tới
cá thể hóa điều trị đích trong tương lai.Năm
2013, Cục Quản lý Dược phẩm và Thực phẩm
(FDA) của Hoa Kỳ đã phê chuẩn sorafenib (một
trong các thuốc ức chế BRAF) được phép chỉ
định điều trị cho nhóm BN UTTG thể biệt hóa, tái
phát, di căn thất bại với điều trị I131 [6,7]. Do

vietnam medical journal n01 - MAY - 2020
230
vậy kết quả sàng lọc nhằm phát hiện đột biến
BRAF V600E có tầm quan trọng, ảnh hưởng đến
việc theo dõibệnh nhân cũng như cá thể hóa
điều trị.
Mục đích nghiên cứu: Hoàn thiện kỹ thuật
Realtime-PCR xác định đột biến gen BRAF V600E
từ các mẫu bệnh phẩm bao gồm mẫu mô phủ
parafin, mẫu mô tươi, mẫu dịch hút tế bào và
mẫu máu ở bệnh nhân theo dõi chẩn đoán ung
thư tuyến giáp.
II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1 Đối tượng nghiên cứu
• Được chia thành 4 nhóm
- Nhóm I: 21 mẫu mô phủ parafin lấy từ 21
bệnh nhân đã có kết quả giải phẫu bệnh chẩn
đoán xác định ung thư tuyến giáp dạng nhú.
- Nhóm II: 21 mẫu mô tươi được lấy trong
quá trình phẫu thuật từ 21 bệnh nhân có kết quả
tế bào học theo dõi ung thư tuyến giáp
- Nhóm III: 22 mẫu dịch hút tế bào lấy từ 22
bệnh nhân nghi ngờ ung thư tuyến giáp có chỉ
định chọc hút tế bào bằng kim nhỏ.
- Nhóm IV: 16 mẫu máu lấy từ 16 bệnh nhân
có bệnh tuyến giáp lành tính khác.
• Thời gian nghiên cứu: Từ tháng 2/2019 đến
tháng 2 /2020.
• Địa điểm nghiên cứu: Trung tâm tư vấn di
truyền, Bệnh viện Đại học Y Hà Nội.
• Mẫu nghiên cứu: mẫu thuận tiện.
2.2 Phương pháp nghiên cứu
Phương pháp mô tả cắt ngang
2.2.1 Tách chiết DNA. Riêng mẫu mô phủ
parafin bước đầu tiên sử dụng xylen để loại bỏ
parafin, sau đó tất cả các mẫu dùng kit Qiagen
để tách chiết DNA.
2.2.2 Nhân đoạn gen bằng kỹ thuật
Realtime-PCR. DNA thu được với độ tinh sạch
đạt chuẩn được pha loãng đạt nồng độ phù hợp
sau đókhuếch đại bằng máy CFX96 (BioRad,
Mỹ)nhằm phát hiện đột biến BRAF V600E. Sự
hiện diện của đột biến BRAF V600E được xác
định bằng kỹ thuật Realtime-PCR với chất màu
huỳnh quang không SYBR Green (Synton, Nga).
Kích thước sản phẩm PCR là 136 bp. Cặp mồi
được sử dụng cho phản ứng PCR (B-raf-51 F và
B-raf-176R) đã được mô tả trước đây [8]. Tóm
lại, xét nghiệm PCR được thực hiện trên máy
CFX96 (Biorad, Mỹ) định lượng tương đối ddCT
thời gian thực với việc sử dụng các mồi dò BRAF-
đột biến FAM-TAGCTACAGAGAAATC và BRAF-
alen bình thường-HEX- CCTAGCTACAGTGAAATC
với chu trình luân nhiệt: 95oC - 3 phút, 40 chu kì
(95oC-15s, 63oC-40s).
2.3 Đạo đức nghiên cứu. Các số liệu và
thông tin nghiên cứu là hoàn toàn chính xác,
trung thực và khách quan đã được xác nhận và
chấp thuận bởi cơ sở nghiên cứu. Những thông
tin của bệnh nhân được giữ bí mật và chỉ phục
vụ công tác nghiên cứu.
III. KẾT QUẢ NGHIÊN CỨU
3.1 Kết quả tách chiết DNA. Chúng tôi cải
tiến trong bước loại bỏ parafin của mẫu mô bằng
cách dùng hóa chất là xylen. Tiến hành kiểm tra
độ tinh sạch đạt chuẩn thu được kết quả sau:
Bảng 3.1. Kết quả đo nồng độ và độ tinh
sạch DNA của 21 mẫu mô phủ parafin
Nồng độ
DNA
Nồng độ
DNA (Ng/µl)
Độ tinh
sạch
Thấp nhất
144,6
1,80
Cao nhất
748,1
2,05
Trung bình
338,55±81,75
1,91±0,05
Nhận xét:
Lượng DNA thu được từ các mẫu
tương đối cao và ổn định với nồng độ cao nhất
đạt 748,1 ng/µl, thấp nhất đạt 144,6ng/µl; độ
tinh sạch cao nhất là 2,05 thấp nhất là 1,80.
Bảng 3.2. Kết quả đo nồng độ và độ tinh
sạch DNA của 21 mẫu mô tươi
Nồng độ
DNA
Nồng độ DNA
(Ng/µl)
Độ tinh
sạch
Thấp nhất
168,9
1,83
Cao nhất
483,4
2
Trung bình
217,3±48,4
1,9±0,06
Nhận xét:
Lượng DNA thu được từ các mẫu
tương đối cao và ổn định với nồng độ cao nhất
đạt 483,4 ng/µl, thấp nhất đạt 168,9ng/µl; độ
tinh sạch cao nhất là 2, thấp nhất là 1,83.
Bảng 3.3. Kết quả đo nồng độ và độ tinh
sạch DNA của 22 mẫu dịch hút tế bào
Nồng độ
DNA
Nồng độ
DNA (Ng/µl)
Độ tinh
sạch
Thấp nhất
13,6
1,80
Cao nhất
59,8
2,04
Trung bình
25,8±11
1,92±0,12
Nhận xét:
Lượng DNA thu được từ các mẫu
tương đối cao và ổn định với nồng độ cao nhất
đạt 59,8ng/µl, thấp nhất đạt 13,6 ng/µl; độ tinh
sạch cao nhất là 2,04, thấp nhất là 1,80.
Bảng 3.4. Kết quả đo nồng độ và độ tinh
sạch DNA của 16 mẫu máu
Nồng độ
DNA
Nồng độ
DNA(Ng/µl)
Độ tinh
sạch
Thấp nhất
45,6
1,83
Cao nhất
135,3
1,97
Trung bình
50,1±4,5
1,93±0,04
Nhận xét:
Lượng DNA thu được từ các mẫu
tương đối cao và ổn định với nồng độ cao nhất
đạt 135,3ng/µl, thấp nhất đạt 46,5ng/µl; độ tinh
sạch cao nhất là 1,97 thấp nhất là 1,83.
TẠP CHÍ Y HỌC VIỆT NAM TẬP 490 - THÁNG 5 - SỐ 1 - 2020
231
3.2 Kết quả pha loãng DNA. Nồng độ DNA
thu được cao nhất ở hai nhóm mẫu mô phủ
parafin và mẫu mô tươi (144,6-748,1ng/µl), thấp
nhất ở nhóm mẫu dịch hút tế bào(13,6-
59,8ng/µl).
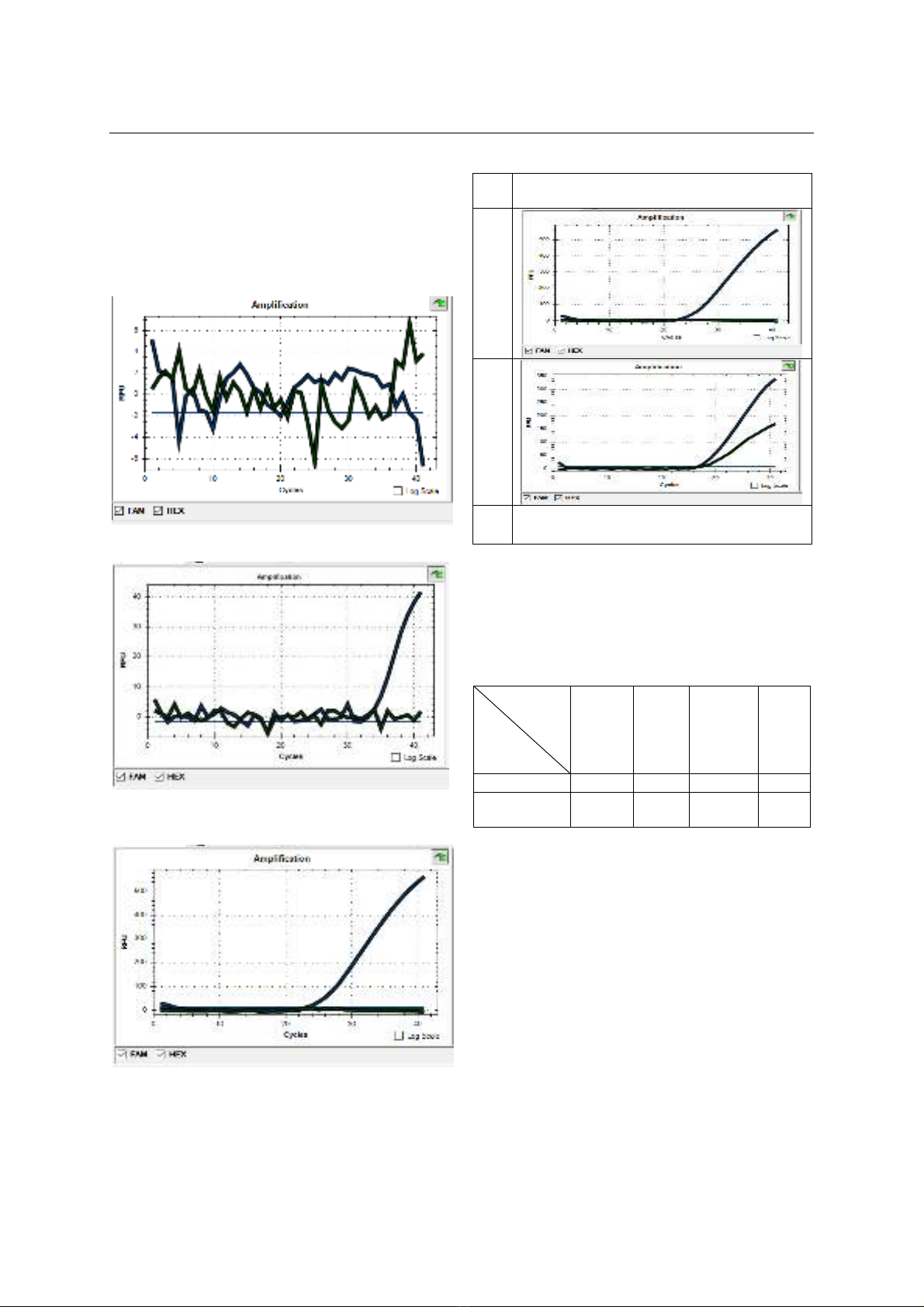
Khi tiến hành PCR, kết quả mẫu ức chế khi
nồng độ DNA >200ng/µl
Nồng độ DNA >200ng/µl
Hình 3.1: Hình ảnh kết quả mẫu ức chế
Nồng độ 100-200ng/µ
Hình 3.2. Hình ảnh kết quả nhiễu khi nồng
độ DNA cao.
Nồng độ <100ng/µl
Hình 3.3. Hình ảnh kết quả sau khi pha
loãng ở nồng độ thích hợp.
3.3 Kết quả REALTIME – PCR
Bảng 3.5: Kết quả REALTIME – PCR
Kiểu
gen
Kit REALTIME-PCR
Bình
thư
ờng
Dị
hợp
tử
đột
biến
Ghi chú: - Hex (xanh lá cây): Alen bình thường
- Fam (xanh nước biển): Alen đột biến
Nhận xét:
Hình ảnh sau khi chạy bằng kỹ
thuật REALTIME -PCR cho kết quả rõ nét, đảm
bảo yêu cầu, dù đã cải tiến ở bước xử lý mẫu
mô và tách chiết DNA.
3.3. Xác địnhđột biến gen BRAF
V600Ebằng kĩ thuật Realtime - PCR
Bảng 3.6. Kết quả xác định đột biến gen
bằng kỹ thuật Realtime -PCR
Loại
mẫu
Kết quả
Mẫu
mô
phủ
parafin
(N)
Mẫu
mô
tươi
(N)
Mẫu
dịch
hút tế
bào(N)
Mẫu
máu
(N)
Có đột biến
11
4
1
0
Không có
đột biến
10
17
21
16
Nhận xét: Khảo sát kiểu gen c.1799T>A
nhận thấy 21 mẫu mô phủ parafin có 11 trường
hợp có đột biến (chiếm 52,38%); 21 mẫu mô
tươi có 4 trường hợp có đột biến (chiếm
19,05%); 22 mẫu dịch hút tế bào có 1 trường
hợp có đột biến (chiếm 4,55%); 16 mẫu máu
không có trường hợp nào có đột biến.
IV. BÀN LUẬN
4.1. Loại bỏ parafin bằng xylen sau đó
tách chiết DNA bằng bộ kit Quiagen cải tiến.
Tách chiết DNA là công đoạn rất quan trọng
trong hầu hết các kỹ thuật sinh học phân tử. Để
các phản ứng tiếp theo được tối ưu và chính xác,
mẫu DNA cần đảm bảo đủ nồng độ, độ tinh
sạch, không bị đứt gãy trong quá trình tách
chiết. Do các mẫu mô đã được xử lý bằng

vietnam medical journal n01 - MAY - 2020
232
formalin và bọc trong parafin nên việc làm sạch
parafin trước khi tách DNA là vô cùng quan
trọng. Nó ảnh hưởng lớn tới độ tinh sạch của
DNA. Nghiên cứu sử dụng xylen là hóa chất dễ
tìm, giá thành phù hợp để loại bỏ parafin, sau đó
tách DNA bằng kit Quiagen giúp tiết kiệm tối đa
lượng hóa chất tách chiết cần thiết, góp phần
giẩm giá thành dịch vụ. Kết quả thu được vẫn
đảm bảo nồng độ DNA với độ OD đạt tiêu
chuẩn, cho phép tiến hành Realtime-PCR.
4.2. Pha loãng nồng độ DNA
Trong 4 loại mẫu: mẫu mô phủ parafin, mẫu
mô tươi, mẫu dịch hút tế bào và mẫu máu nồng
độ DNA thu được cao nhất ở nhóm mẫu mô phủ
parafin(748,1ng/µl), thấp nhất ở nhóm mẫu dịch
hút tế bào(13,6 ng/µl), ổn định nhất ở nhóm
mẫu máu(với độ lệch chuẩn 50,1±4,5 ng/µl).
Nồng độ DNA cao sẽ ức chế phản ứng. Sau
khi thu được DNA chúng tôi tiến hành pha loãng
để nồng độ DNA thu được dưới 100 ng/µl trước
khi tiến hành PCR. Chúng tôi nhận thấy rằng
nồng độ DNA trong khoảng 20-50 ng/µl cho hình
ảnh kết quả Realtime-PCR đẹp, ổn định nhất.
4.3. Kết quả xác định kiểu gen đột biến
bằng phương pháp Realtime– PCR
Ung thư biểu mô tuyến giáp thể nhú (PTC)
chiếm 80%-90% ung thư tuyến giáp và là ung
thư có tiên lượng tốt [3,4]. Mặc dù được xem là
có tiên lượng tốt song tỷ lệ di căn hạch chiếm
50% và di căn xa chiếm 10% [5]. Tỷ lệ mắc
ung thư tuyến giáp tăng nhanh ở cả nữ giới và
nam giới [6]. Do đó các phương pháp chẩn đoán
cũng như điều trị mới nên được nghiên cứu và
phát hiện. BRAF được biết đến như một gen tiền
ung thư, hoạt động như serine/threonin kinase
kích hoạt con đường truyền tín hiệu nội bào
MAPK [7]. Nhiều nghiên cứu đã chứng minh
rằng đột biến V600E nằm trong vùng kích hoạt
BRAF(CR3) làm tăng cường kích hoạt con đường
MAPK một cách liên tục, thúc đẩy các dòng tế
bào ung thư phát triển. Phát hiện đột biến gen
BRAF V600E là yêu cầu được đặt ra nhằm phục
vụ nhu cầu chẩn đoán và điều trị ung thư tuyến
giáp cũng như nhiều loại ung thư khác liên quan
đến đột biến này.
Nghiên cứu của chúng tôi tiến hành tìm đột
biến trên 4 loại mẫu: mẫu mô phủ parafin, mẫu
mô tươi, mẫu dịch hút tế bào và mẫu máu. Kết
quả phát hiện đột biến ghi nhận 11 trường hợp
mang đột biến trong 21 mẫu mô phủ parafin
(chiếm tỷ lệ 52,38%), 4 trường hợp mang đột
biến trong 21 mẫu mô tươi (chiếm tỷ lệ 19,05%),
1 trường hợp mang đột biến trong 22 mẫu dịch
hút tế bào (chiếm 4,55%) và không có trường
hợp nào mang đột biến trong 16 mẫu máu.
Chúng tôi hi vọng rằng những kỹ thuật này sẽ
được kiểm chứng trên cỡ mẫu lớn hơn để có độ
chính xác cao hơn trước khi ứng dụng trong lâm
sàng chẩn đoán và điều trị ung thư tuyến giáp.
V. KẾT LUẬN
- Hoàn thiện thành công kỹ thuật Realtime-
PCR để xác định đột biến gen BRAF V600E từ 4
loại mẫu bệnh phẩm: mẫu mô phủ parafin, mẫu
mô tươi, mẫu dịch hút tế bào, mẫu máu ở bệnh
nhân theo dõi chẩn đoán ung thư tuyến giáp
dạng nhú.
- Tỷ lệ xuất hiện đột biến gen ở mẫu máu là
0%; ở mẫu mô phủ parafin là 52,38%, ở mẫu mô
tươi là 19,05%, ở mẫu dịch hút tế bào là 4,55%.
Nhóm mẫu mô phủ parafin là nhóm bệnh nhân
đã có chẩn đoán xác định ung thư tuyến giáp
dạng nhú trong đó 7/11(63,63%) trường hợp
phát hiện đột biến có tình trạng di căn hạch,
2/11(18,18%) trường hợp tái phát sau 1 năm.
TÀI LIỆU THAM KHẢO
1. Chen AY, Jemal A, Ward EM. Increasing incidence
of differentiated thyroid cancer in the United States,
1988–2005. Cancer. 2009; 115(16): 3801–7.
2. Li N, Du XL, Reitzel LR, Xu L, Sturgis
EM. Impact of enhanced detection on the increase
in thyroid cancer incidence in the United States:
review of incidence trends by socioeconomic status
within the surveillance, epidemiology, and end
results registry, 1980–2008. Thyroid: official
journal of the American Thyroid Association.
2013;23(1):103–10.
3. Nikiforov YE, Nikiforova MN. Molecular
genetics and diagnosis of thyroid cancer. Nature
reviews Endocrinology. 2011;7(10):569–80.
4. Kowalska A, Walczyk A, Kowalik A et al
(2017), “Response to therapy of papillary thyroid
cancer of known BRAF status”, Clinical
Endocrinology, 87(1).
5. Pacini F, Castagna MG, Brilli L et al (2008),
“Differentiated thyroid cancer: European Society
for Medical Ocology clinical recommendation for
diagnosis, treament and follow-up”, Annals of
Oncology, (19), pp. 99 - 101.
6. Brose MS. Nutting CM, Sherman et al.
Rationale and design of DICISION: a doubleblind,
randomized, placebo-controlled phase III trial
evaluating the efficacy and safety of sorafenib in
patients with locally advanced or metastatic
radioactive iodine (RAI)-refractory, differentiated
thyroid cancer. BMC Cancer. 2011, 11, 349.
7. Ye X, Zhu Y, Cai J. Relationship between
toxicities and clinical benefits of newly approved
tyrosine kinase inhibitors in thyroid cancer: A
meta-analysis of literature. J Cancer Res Ther.
2015, 11, Suppl 2, pp.185-190.
8. Benlloch S, Paya A, Alenda C, et al. Detection
of BRAF V600E mutation in colorectal cancer:
comparison of automatic sequencing and real-time
chemistry methodology. J Mol Diagn 2006; 8(5):
540–543.


























