HOÁ VÔ CƠ
1. Tên học phần: HOÁ VÔ CƠ
2. Mã số:
3. Khối lượng: 4 (4.0.0.8)
Lý thuyết: 60 giờ.
Tự học: 120 giờ.
4. Đối tượng tham dự: Sinh viên năm thứ ba.
5. Điều kiện học phần:
Đã học Hóa học Đại cương.
6. Mục tiêu học phần:
Trang bị cho sinh viên các kiến thức cơ bản về các tính chất lý học, hóa học, nguyên tắc điều chế và
một số ứng dụng quan trọng nhất của các đơn chất và hợp chất vô cơ phổ biến nhất; các kiến thức
về quy luật biến thiên các tính chất quan trọng như tính axit-bazơ, tính oxy hóa- khử, tính bền và tính
tan của các đơn chất cũng như hợp chất của chúng trong nhóm và trong chu kỳ của bảng tuần hoàn;
Giải thích bản chất các tính chất và các quy luật biến thiên các tính chất dựa vào các kiến thức của
hóa học đại cương
7. Nội dung vắn tắt học phần:
Sự biến thiên tuần hoàn tính chất trong bảng tuần hoàn; Liên kết hóa học và cấu tạo phân tử; Chiền
của phản ứng hóa học vô cơ; Một số tính chất chung của các chất vô cơ; Các nguyên tố nhóm A và
hợp chất của chúng; Phức chất; Tính chất chung của các kim loại chuyển tiếp; Các nguyên tố nhóm
B và hợp chất của chúng.
8. Tài liệu học tập
Sách giáo khoa chính:
[1]. Lê Mậu Quyền: Hóa học vô cơ, Nhà Xuất Bản Khoa học & Kỹ thuật.
[2]. Lê Mậu Quyền: Bài tập hóa học vô cơ, Nhà Xuất Bản Khoa học & Kỹ thuật.
Sách tham khảo: Xem đề cương chi tiết.
9. Phương pháp học tập và nhiệm vụ của sinh viên:
Dự lớp: đầy đủ theo qui chế.
Thảo luận
Bài thu hoạch
Bài tập: hoàn thành các bài tập của học phần
10. Đánh giá kết quả:
Điểm môn học bao gồm 2 phần là: điểm thi cuối kỳ và điểm quá trình.
Điểm quá trình (bài tập của học phần + kiểm tra giữa kỳ): trọng số 0,3.
Thi cuối kỳ (tự luận + trắc nghiệm): trọng số 0,7.
11. Nội dung và kế hoạch học tập cụ thể
Tuần Nội dung SGK
chính
LT
1 CHƯƠNG 1- SỰ BIẾN THIÊN TUẦN HOÀN TÍNH CHẤT CÁC NGUYÊN
TỐ TRONG BẢNG TUẦN HOÀN (3LT)
1.1. Cấu tạo bảng tuần hoàn
- Các loại nguyên tố. Cấu trúc của bảng tuần hoàn dạng dài và nguyên
tắc sắp xếp các nguyên tố trong bảng. Họ các nguyên tố hiếm 4f và 5f.
1.2. Sự biến thiên tính chất của các nguyên tố trong bảng tuần hoàn
- Năng lượng của các obitan. Sự biến thiên năng lượng của các obitan
nguyên tử theo chiều tăng điện tích hạt nhân. Giản đồ EAO- Z. Sự biến
thiên năng lượng các obitan hóa trị của các nguyên tử theo nhóm và
chu kỳ.
[1]
- Năng lượng ion hóa I1. Sự biến thiên năng lượng ion hóa thứ nhất của
các nguyên tử theo chiều tăng của điện tích hạt nhân. Giản đồ I1- Z.
Giải thích sự biến thiên của I1. Giản đồ I1- Z. Giải thích sự biến thiên
của I1 theo chu kỳ và theo nhóm.
- Ái lực với electron, bán kính nguyên tử. Sự biến thiên theo chu kỳ và
nhóm. Sự co d và co f.
CHƯƠNG 2- CÁC KIẾN THỨC VỀ LIÊN KẾT HÓA HỌC VÀ CẤU TẠO
PHÂN TỬ (4 LT)
2.1. Các khái niệm
- Độ âm điện nguyên tố. Thang đo độ âm điện của Pauling. Ứng dụng
của độ âm điện. Năng lượng liên kết trong liên kết cộng hóa trị. Khái
niệm về năng lượng tạo liên kết và năng lượng phá vỡ liên kết, năng
lượng liên kết trung bình.
2 2.2. Cấu trúc phân tử.
- Công thức Lewis. Công thức cộng hưởng. Điện tích hình thức. Dự
đoán cấu hình không gian của phân tử. Mô hình sự đẩy của các cặp
electron hóa trị. Công thức Gillespie. Quan hệ giữa độ âm điện và góc
liên kết. Quan hệ giữa kiểu lai hóa và công thức hình học phân tử. Độ
phân cực của phân tử.
2.3. Các loại liên kết
- Liên kết ion. Năng lượng liên kết ion và năng lượng mạng lưới ion.
Công thức Born-Landé và Kapustinski. Các yếu tố ảnh hưởng đến
năng lượng mạng lưới ion. Liên kết cộng hóa trị. Các liên kết yếu: liên
kết hydro và lực Van der Waals.
CHƯƠNG 3- CHIỀU PHẢN ỨNG HÓA HỌC VÔ CƠ (2LT)
3.1. Phản ứng trao đổi
- Chất điện ly mạnh, chất điện ly yếu. Chiều phản ứng trao đổi.
[1]
3 3.2. Phản ứng oxy hóa khử
- Xác định số oxi hóa của một nguyên tố. Cân bằng phản ứng oxi hóa
khử. Thế khử và công thức tính thế khử của các cặp oxi hóa khử.
Chiều và giới hạn của phản ứng oxi hóa khử xảy ra trong dung dịch
nước. Giản đồ thế khử và ứng dụng. Mối quan hệ giữa thế khử và
năng lượng liên kết. Quan hệ giữa thế khử chuẩn của một cặp oxi hóa
-khử và các đại lượng thế đẳng áp nguyên tử hóa, ion hóa, hydrat hóa.
Ảnh hưởng của các phối tử tạo phức và các cấu tử tạo kết tủa đến thế
khử của một cặp oxi hóa khử.
CHƯƠNG 4- MỘT SỐ TÍNH CHẤT CHUNG CỦA CÁC CHẤT VÔ CƠ
(2LT)
4.1. Sự hòa tan
- Một số quy luật định tính về sự hòa tan của các chất trong dung môi
lỏng. Các yếu tố ảnh hưởng đến độ hòa tan của các hợp chất ion trong
nước.
4.2. Nhiệt độ chuyển pha của các chất
- Các yếu tố ảnh hưởng đến nhiệt độ chuyển pha của các chất. Tính
nhiệt độ chuyển pha của các chất. Ảnh hưởng của liên kết yếu đến
nhiệt độ chuyển pha của các chất.
4.3. Tính dẫn điện của các chất, thuyết vùng
- Cấu tạo của kim loại. Giải thích tính dẫn điện, tính bán dẫn và cách
điện của kim loại.
4.4. Tính chất từ của các chất
- Chất thuận từ và chất nghịch từ. Nguyên nhân sự khác nhau về tính
chất từ của hai loại chất này. Momen từ của chất thuận từ
[1]
CHƯƠNG 5- HYDRO VÀ NƯỚC (2LT)
5.1. Hydro
- Cấu tạo và lý tính. Tính chất hóa học của hydro. Hydro mới sinh.
Phương pháp điều chế và ứng dụng của hydro.
4 5.2. Các hydrua
- Hydrua cộng hóa trị. Hydrua ion. Hydrua kiểu kim loại.
5.3. Nước
- Cấu tạo và tính chất lý học của nước. Tính chất bất thường của nước.
Tính chất hóa học của nước. Giản đồ thế khử của nước.
CHƯƠNG 6- CÁC HALOGEN (4LT)
6.1. Đặc tính chung của nhóm
- Cấu tạo và số oxi hóa. Tính chất lý học.
6.2. Tính chất hóa học
- Tính oxi hóa. Tính khử. Các phương pháp điều chế. Ứng dụng.
[1]
5 6.3. Các hợp chất
- Hợp chất hydro halogenua: tính chất lý học, hóa học, phương pháp
điều chế. Hợp chất halogen chứa oxi: hợp chất HXO, HXO3, HXO4.
CHƯƠNG 7- CÁC NGUYÊN TỐ NHÓM VIA (4LT)
7.1. Đặc tính chung của nhóm
7.2. Oxi
- Đơn chất oxi và ozon: cấu tạo phân tử, tính chất lý học, hóa học, trạng
thái tự nhiên, phương pháp điều chế và ứng dụng. Hợp chất. Các oxit:
điều kiện tạo thành, phân loại oxit. Các hydroxit: phân loại, các yếu tố
ảnh hưởng đến lực axit và bazơ của các hydroxit. Hydro peoxit: cấu
tạo phân tử, tính chất lý học, hóa học, phương pháp điều chế và ứng
dụng.
7.3. Lưu huỳnh
- Đơn chất. Các dạng thù hình. Cấu tạo phân tử, tính chất lý học, hóa
học, trạng thái thiên nhiên. Phương pháp điều chế và ứng dụng. Hợp
chất. Đihydrosunfua, SO2, H2SO3, SO32-, H2SO4 và muối của chúng:
cấu tạo phân tử, tính chất lý học, hóa học, phương pháp điều chế và
ứng dụng. Một số hợp chất khác của lưu huỳnh: axit thiosunfuric, axit
peoxidisunfuric và các muối của chúng: phương pháp điều chế, tính
chất lý học, hóa học và ứng dụng.
[1]
6 7.4. Selen, Telu và poloni
- Đơn chất. Các dạng thù hình. Tính chất lý học, hóa học. Trạng thái
thiên nhiên. Phương pháp điều chế và ứng dụng của selen. Hợp chất.
Hợp chất H2X, XO2, H2XO3, XO3, các axit X(VI) và các muối tương
ứng. Cấu tạo phân tử, so sánh tính chất lý học, hóa học với các hợp
chất tương ứng của lưu huỳnh.
CHƯƠNG 8- CÁC NGUYÊN TỐ NHÓM VA (4LT)
8.1. Đặc tính chung của nhóm.
- Hóa trị và số oxi hóa. Tính trơ của cặp electron ns.
8.2. Nitơ
- Đơn chất. Cấu tạo phân tử. Tính chất lý học, hóa học. Trạng thái tự
nhiên. Phương pháp điều chế và ứng dụng. Hợp chất. Amoniac và
muối amoni: cấu tạo phân tử, tính chất lý học, hóa học, phương pháp
điều chế và ứng dụng. Các oxit quan trọng của nitơ, axit nitrơ và muối
của nó: điều kiện tạo thành, cấu tạo phân tử, tính chất lý học, hóa học.
[1]
Axit nitric và muối của nó: cấu tạo phân tử, tính chất lý học, hóa học.
Nước cường toan và tính chất của nó. Phương pháp điều chế và ứng
dụng của axit nitric.
8.3. Phốtpho
- Đơn chất. Các dạng thù hình. Tính chất lý học, hóa học. Trạng thái tự
nhiên. Phương pháp điều chế và ứng dụng. Hợp chất. Các oxit quan
trọng: điều kiện tạo thành, cấu tạo phân tử, tính chất lý học, hóa học và
ứng dụng. Axit photphorơ, axit photphoric và muối của chúng: cấu tạo
phân tử, tính chất lý học, hóa học. Phương pháp điều chế và ứng dụng
của axit photphoric.
7 8.4. Asen, antimon và bitmut
- Đơn chất. Các dạng thù hình. Tính chất lý học, hóa học so sánh với
nitơ và photpho. Hợp chất. Hợp chất XH3: điều kiện tạo thành, cấu tạo
phân tử, tính chất lý học, hóa học so sánh với NH3 và PH3.
- Các oxit. Hydroxit và muối của chúng chứa nguyên tố với số oxi hóa
+III, +V: điều kiện tạo thành, cấu tạo phân tử, tính chất lý học, hóa học
so sánh với các hợp chất của photpho.
CHƯƠNG 9- CÁC NGUYÊN TỐ NHÓM IVA (3LT)
9.1. Đặc tính chung của nhóm.
- Hóa trị và số oxi hóa. Tính trơ của cặp electron ns
9.2. Cácbon
- Đơn chất. Các dạng thù hình. Tính chất lý học, hóa học, phương pháp
điều chế và ứng dụn. Hợp chất. Các bon oxit, CO2, H2CO3 và muối của
nó: công thức cấu tạo, tính chất lý học, hóa học, phương pháp điều
chế và ứng dụng.
9.3. Silic
- Đơn chất. Cấu trúc tinh thể, tính chất lý học, hóa học, trạng thái tự
nhiên, phương pháp điều chế và ứng dụng. Hợp chất. Silan: điều kiện
tạo thành, tính chất lý học, hóa học, ứng dụng. SiO2, các axit và muối
tương ứng: tính chất lý học, hóa học, phương pháp điều chế và ứng
dụng.
9.4. Gecmani, thiếc, chì
- Đơn chất. Các dạng thù hình của thiếc, tính chất lý học, hóa học, trạng
thái tự nhiên, phương pháp điều chế và ứng dụng. Hợp chất. Các oxit,
hydroxit và muối tương ứng: tính chất lý học, hóa học so sánh với các
hợp chất của silic. Phương pháp điều chế và ứng dụng.
[1]
8 CHƯƠNG 10- CÁC NGUYÊN TỐ NHÓM IIIA (2LT)
10.1. Đặc tính chung của nhóm.
- Hóa trị và số oxi hóa. Tính trơ của cặp electron ns
10.2. Bo
- Đơn chất. Các dạng thù hình. Tính chất lý học, hóa học, trạng thái tự
nhiên, phương pháp điều chế. Hợp chất. Oxit, axit và muối của Bo:
công thức cấu tạo, tính chất lý học, hóa học, phương pháp điều chế và
ứng dụng.
10.3. Nhôm
- Đơn chất. Tính chất lý học, hóa học, trạng thái tự nhiên, phương pháp
điều chế và ứng dụng. Hợp chất. Oxit, hydroxit và muối của nó: tính
chất lý học, hóa học, phương pháp điều chế và ứng dụng.
10.4. Gali, Indi và Tali
- Đơn chất. Tính chất lý học, hóa học so sánh với nhôm. Trạng thái tự
nhiên, phương pháp điều chế và ứng dụng. Hợp chất. Oxit, hydroxit và
muối của nó: điều kiện tạo thành, tính chất lý học, hóa học so sánh với
[1]
các hợp chất tương ứng của nhôm.
CHƯƠNG 11- CÁC NGUYÊN TỐ NHÓM IIA (2LT)
11.1. Đặc tính chung của nhóm
- Electron hóa trị và số oxi hóa. Sự biến thiên một số tính chất của
nguyên tử: bán kính kim loại, bán kính ion M2+, năng lượng ion hóa.
11.2. Đơn chất
- Tính chất lý học, hóa học, trạng thái tự nhiên, phương pháp điều chế.
11.3. Hợp chất
- Oxit, hydroxit và muối của chúng: tính chất lý học, hóa học, phương
pháp điều chế và ứng dụng.
- Bari peoxit: tính chất lý học, hóa học, phưong pháp điều chế và ứng
dụng.
9 CHƯƠNG 12- CÁC KIM LOẠI KIỀM (2LT)
12.1. Đặc tính chung của nhóm
- Electron hóa trị và số oxi hóa. Sự biến thiên một số tính chất của
nguyên tử: bán kính kim loại, bán kính ion M+, năng lượng ion hóa.
12.2. Đơn chất
- Tính chất lý học, hóa học, trạng thái tự nhiên, phương pháp điều chế
và ứng dụng.
12.3. Hợp chất
- Oxit, peoxit, supeoxit, ozonit, hydroxit và muối: tính chất lý học, hóa
học. Phương pháp điều chế và ứng dụng của Na2O2.
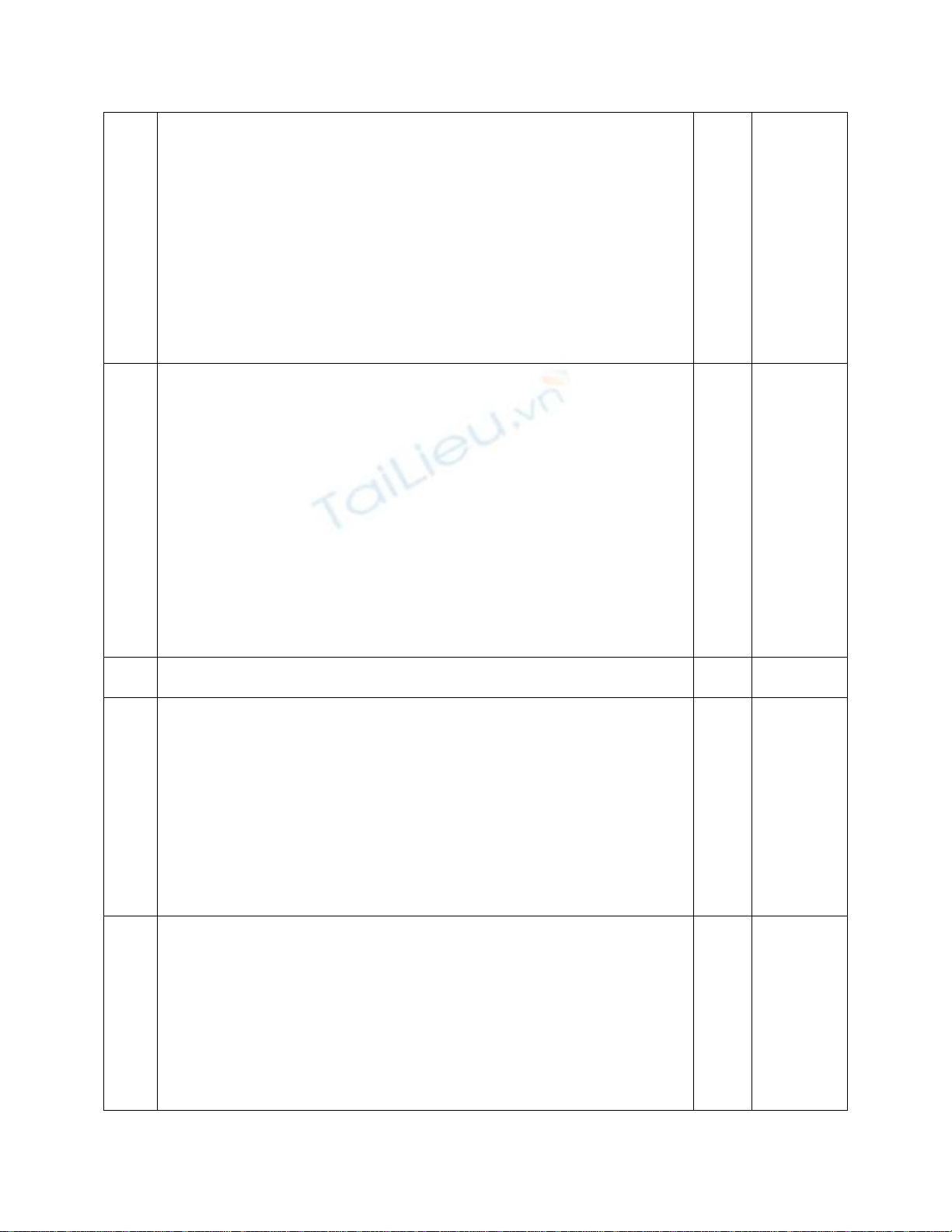
CHƯƠNG 13- PHỨC CHẤT (9LT)
13.1. Một số khái niệm
- Phức chất, dung lượng phối trí của phối tử, số phối trí của nhân trung
tâm.
[1]
10 13.2. Liên kết hóa học trong phức chất
- Thuyết liên kết hóa trị, thuyết trường tinh thể, thuyết obitan phân tử.
[1]
11 13.3. Phức chất trong dung dịch nước
- Hằng số điện ly, hằng số bền của ion phức và các yếu tố ảnh hưởng.
CHƯƠNG 14- TÍNH CHẤT CHUNG CỦA CÁC NGUYÊN TỐ CHUYỂN
TIẾP D (1LT)
14.1. Đặc điểm cấu hình electron hóa trị
- Số electron hóa trị. Sự biến thiên năng lượng các obitan hóa trị theo
chu kỳ và theo nhóm.
14.2. Tính chất chung
- Tính kim loại, số oxi hóa, khả năng tạo phức, tính chất từ, nhiệt độ
nóng chảy, nhiệt độ sôi và sự biến thiên theo chu kỳ và theo nhóm.
[1]
12 CHƯƠNG 15- CÁC NGUYÊN TỐ NHÓM VIB (3LT)
15.1. Đặc tính chung của nhóm
- Electron hóa trị, số oxi hóa. Sự biến thiên tính kim loại, năng lượng ion
hóa.
15.2. Đơn chất
- Tính chất lý học, hóa học, trạng thái tự nhiên, phương pháp điều chế
và ứng dụng.
15.3. Hợp chất
- Các hợp chất chứa nguyên tố với các số oxi hóa 0, +II, +III, +IV, +VI,
chủ yếu là các hợp chất của crôm: tính chất lý học, hóa học, phương
[1]



![Tính chất hóa học chung của các chất Vô cơ [chuẩn SEO]](https://cdn.tailieu.vn/images/document/thumbnail/2016/20161006/bins100/135x160/9881475804057.jpg)





![Dung môi: Khái niệm và các loại dung môi thường dùng [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2011/20111116/abcdef_50/135x160/khai_niem_dung_moi_va_cac_loai_dung_moi_thuong_dung_6143.jpg)









![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



