
Trường Đại học Khoa học Tự nhiên
Khoa Hóa – Bộ môn Hóa Học Hữu cơ
HA HU CƠ 1
1
Cycloalkane và alkane mạch hở có tính chất hóa học khá giống nhau: có tính
không phân cực và tương đối trơ. Sự khác biệt là cycloalkane có tính kém uyển
chuyển, linh động so với các alkane mạch hở.
Vòng cycloalkane càng lớn thì sự xoay chuyển càng dễ dàng hơn, Vòng lớn (từ
25C trở lên) thì sự xoay chuyển dễ dàng, gần giống alkane mạch thẳng.
2
Chương 4: Cycloalkane và hóa học lập thể của cycloalkane
1. Đồng phân cis – trans trong cycloalkane
Đồng phân cis: hai nhóm thế ở cùng phía mặt phẳng của vòng.
Đồng phân trans: hai nhóm thế ở hai phía đối diện mặt phẳng của vòng.
Đồng phân cis, trans là hai đồng phân lập thể.
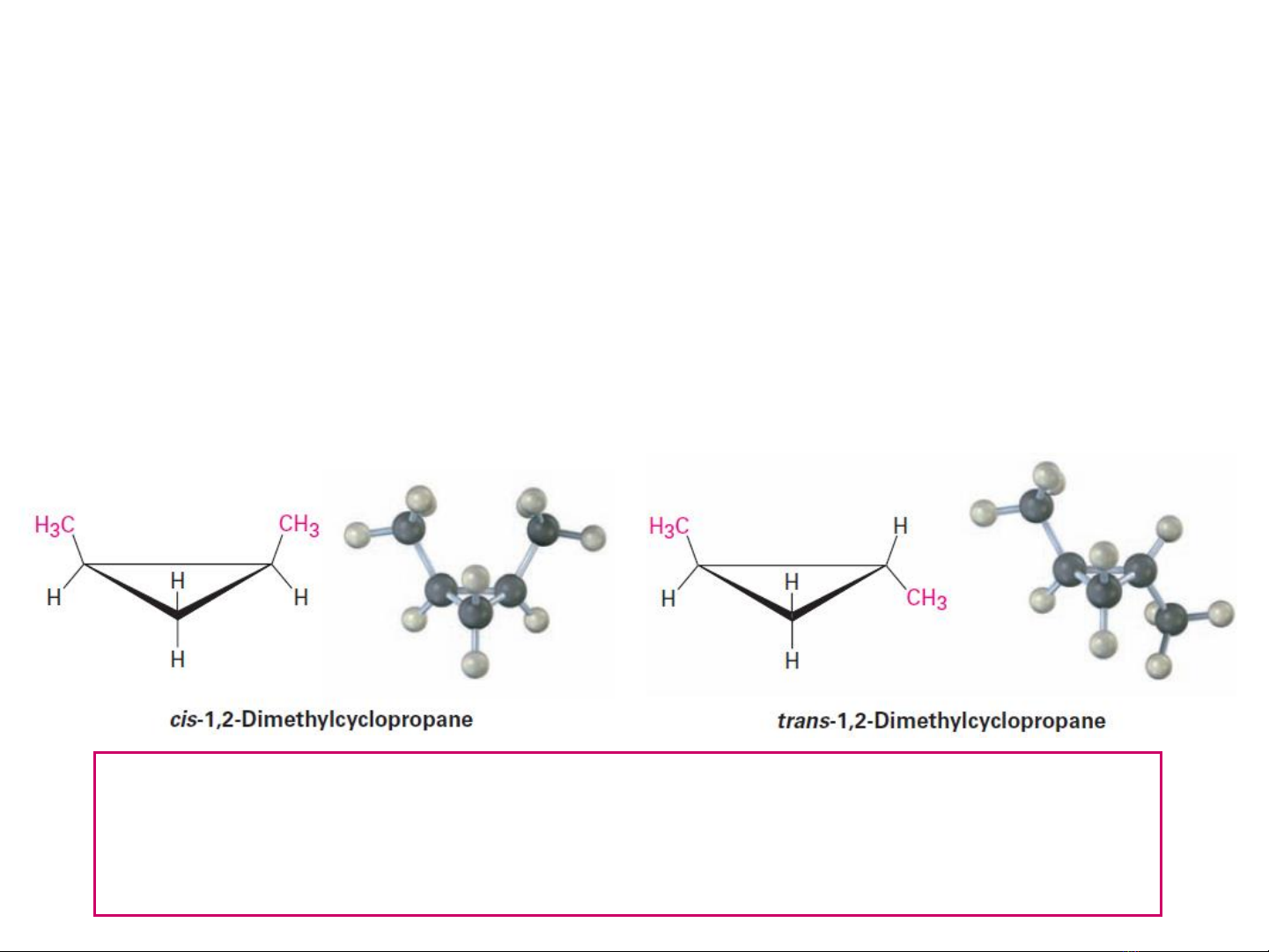
Đồng phân cis-trans trong cycloalkane mang hai nhóm thế
3
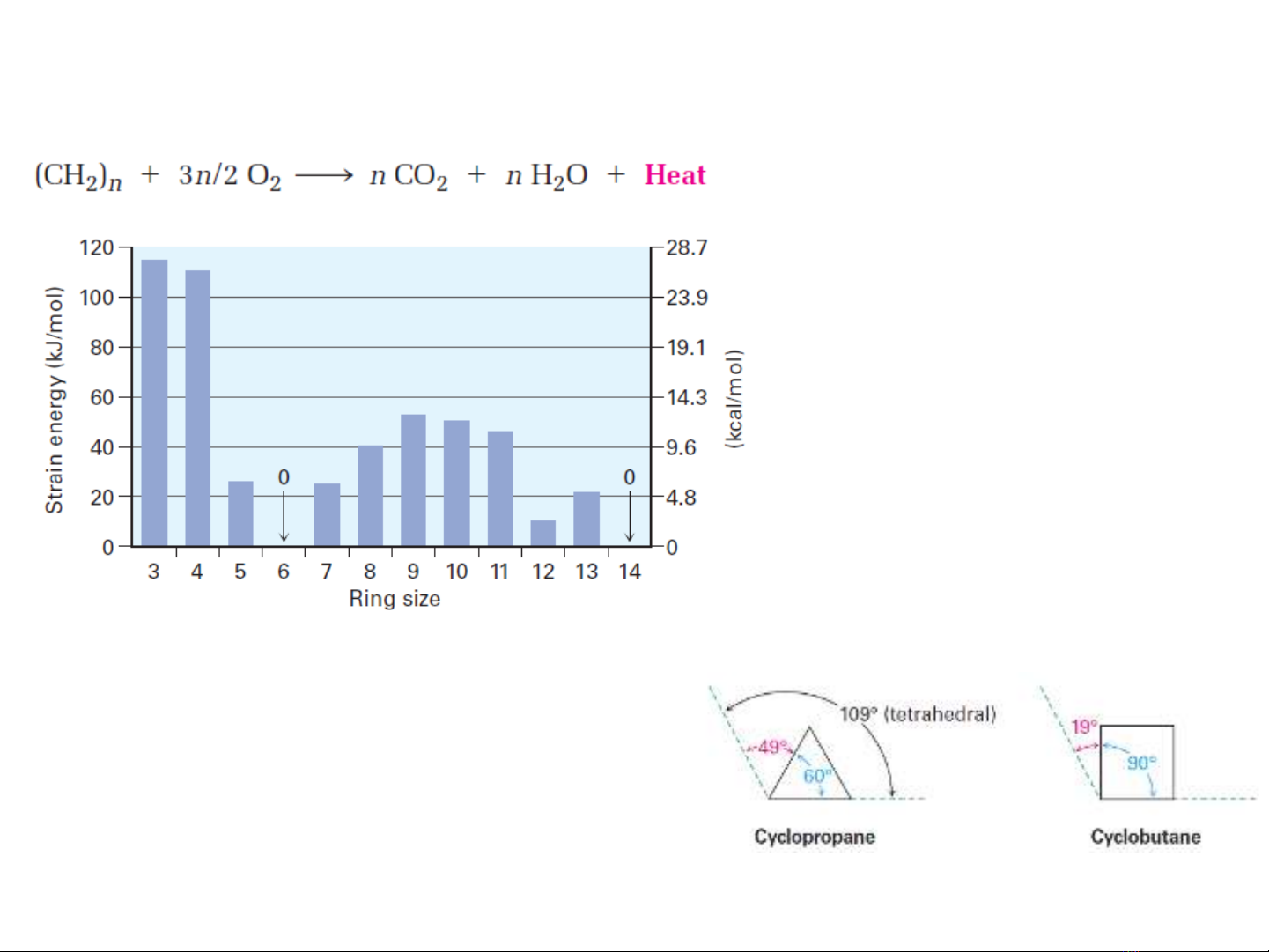
2. Tính bền của cycloalkane: sức căng vòng (ring strain)
Các vòng cyclopropane và
cyclobutane có sức căng vòng
rất lớn vì các vòng này nhỏ, ko
có sự linh hoạt.
Các vòng kích thước trung
bình có sức căng vòng vừa
phải.
Vòng 6C và vòng 14C
không có sức căng vòng.
Năng lượng sức căng vòng của một số cycloalkane
Sức căng góc (angle strain): là sức
căng tạo ra trong phân tử khi các góc nối
trong phân tử bị buộc phải ép nhỏ lại so
với giá trị góc tứ diện lý tưởng là 109.5o.
4
2. Tính bền của cycloalkane: sức căng vòng (ring strain)
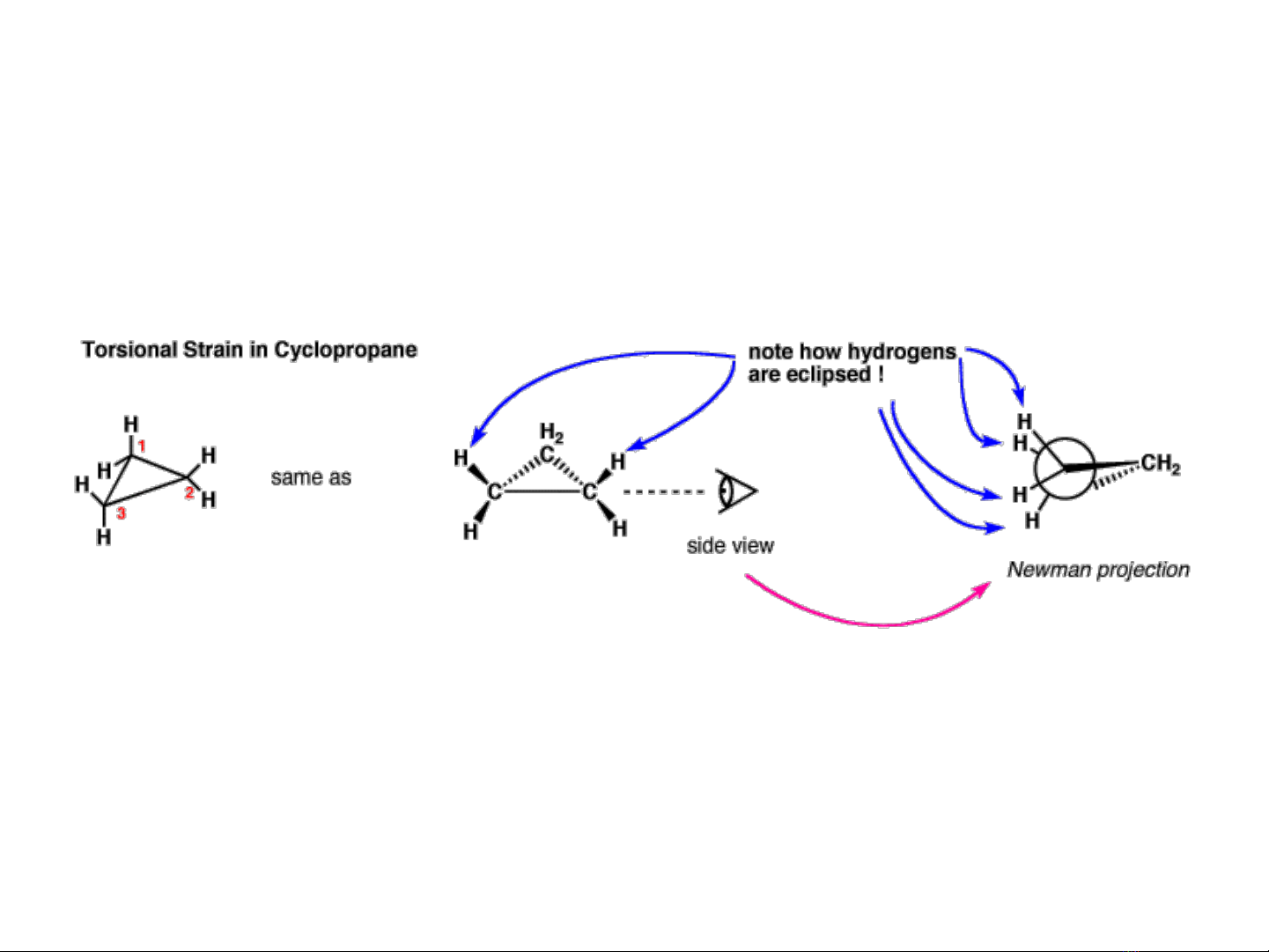
Lực xoắn (torsional strain): lực gây ra do sự che chắn của các nối gắn vào các
nguyên tử kề bên nhau.
Lực do cản trở lập thể (steric strain): lực gây ra do sự tương tác xô đẩy nhau khi
hai nguyên tử đến quá gần nhau.
Với hầu hết các vòng, nhất là các vòng kích thước trung bình (C7-C11), lực
xoắn gây ra bởi sự tương tác che khuất HH trên các carbon liền kề và lực lập thể
gây ra do sự xô đẩy giữa các nguyên tử không nối ở quá gần nhau.
3. Cấu trạng của các cycloalkane
•Cyclopropane là vòng căng nhất, do sức căng góc gây ra bởi góc 60 o.
•Cyclopropane chịu lực xoắn do các nối C-H trên các C kề nhau che chắn nhau.
Cyclopropane rất căng, phản ứng mở vòng tạo alkane mạch thẳng dễ xảy ra.
5
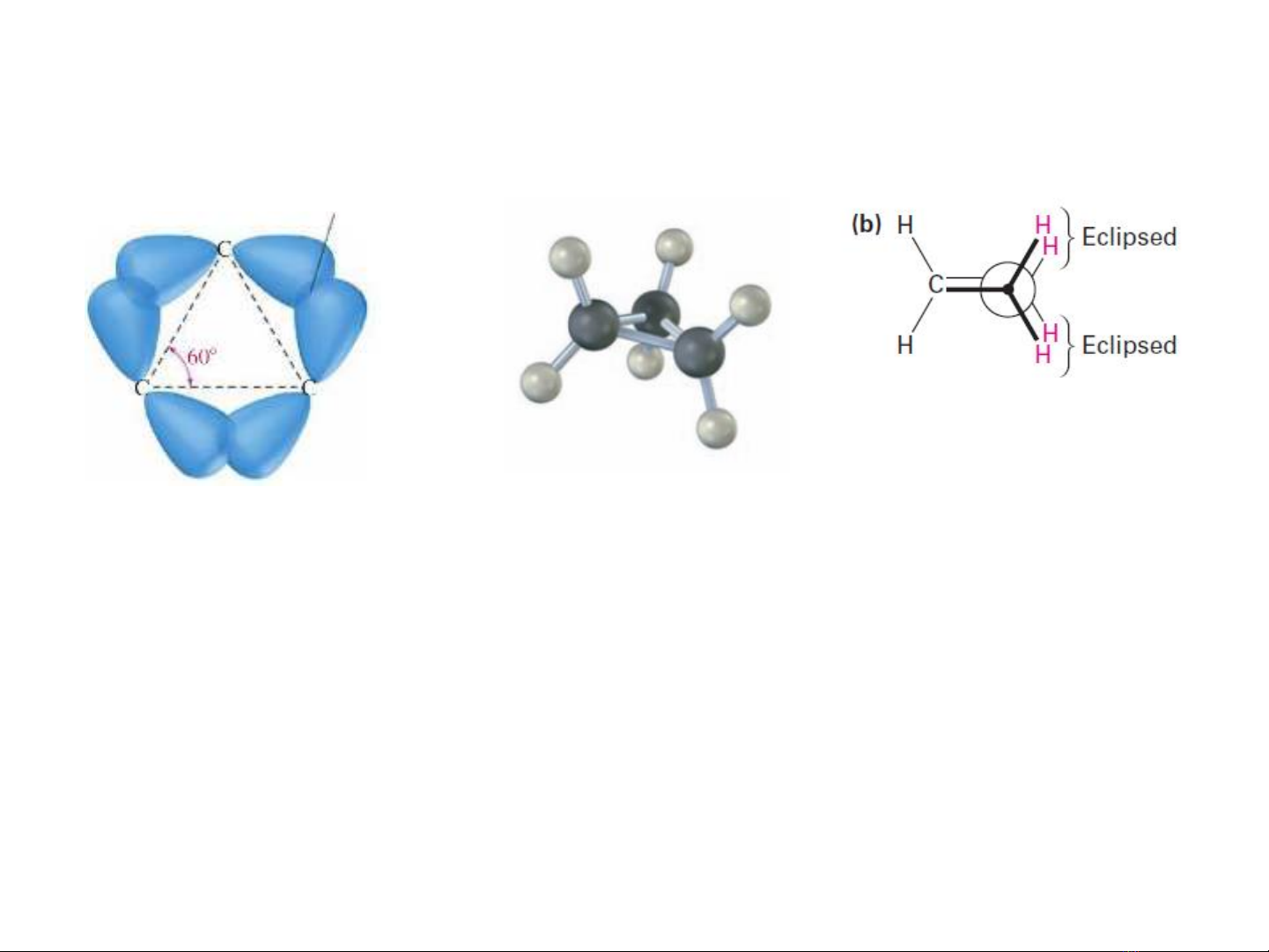
Cyclopropane
Xen phủ vân đạo kém















![Đề thi kết thúc học phần Nguyên lí Hóa học 2 [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20251014/anhinhduyet000/135x160/69761760428591.jpg)










