
Tìm hiểu bảng hệ thống tuần hoàn
Bảng tuần hoàn các nguyên tố hóa học, hay bảng tuần hoàn
Mendeleev, hay ngắn gọn bảng tuần hoàn, là một phương pháp liệt kê
các nguyên tố hóa học thành bảng, liên quan mật thiết với định luật
tuần hoàn.
Các nguyên tố được sắp xếp theo cấu trúc electron. Do cấu trúc
electron là yếu tố quyết định các tính chất hóa học của các nguyên tố,
việc sắp xếp này tạo nên sự thay đổi đều đặn của các tính chất hóa học
theo các hàng và cột.
Mỗi nguyên tố được liệt kê bởi số nguyên tử và ký hiệu hóa học. Bảng
tuần hoàn tiêu chuẩn cho biết các dữ liệu cơ bản nhất. Còn có nhiều các
trình bày khác cho từng mục đích cụ thể hơn.
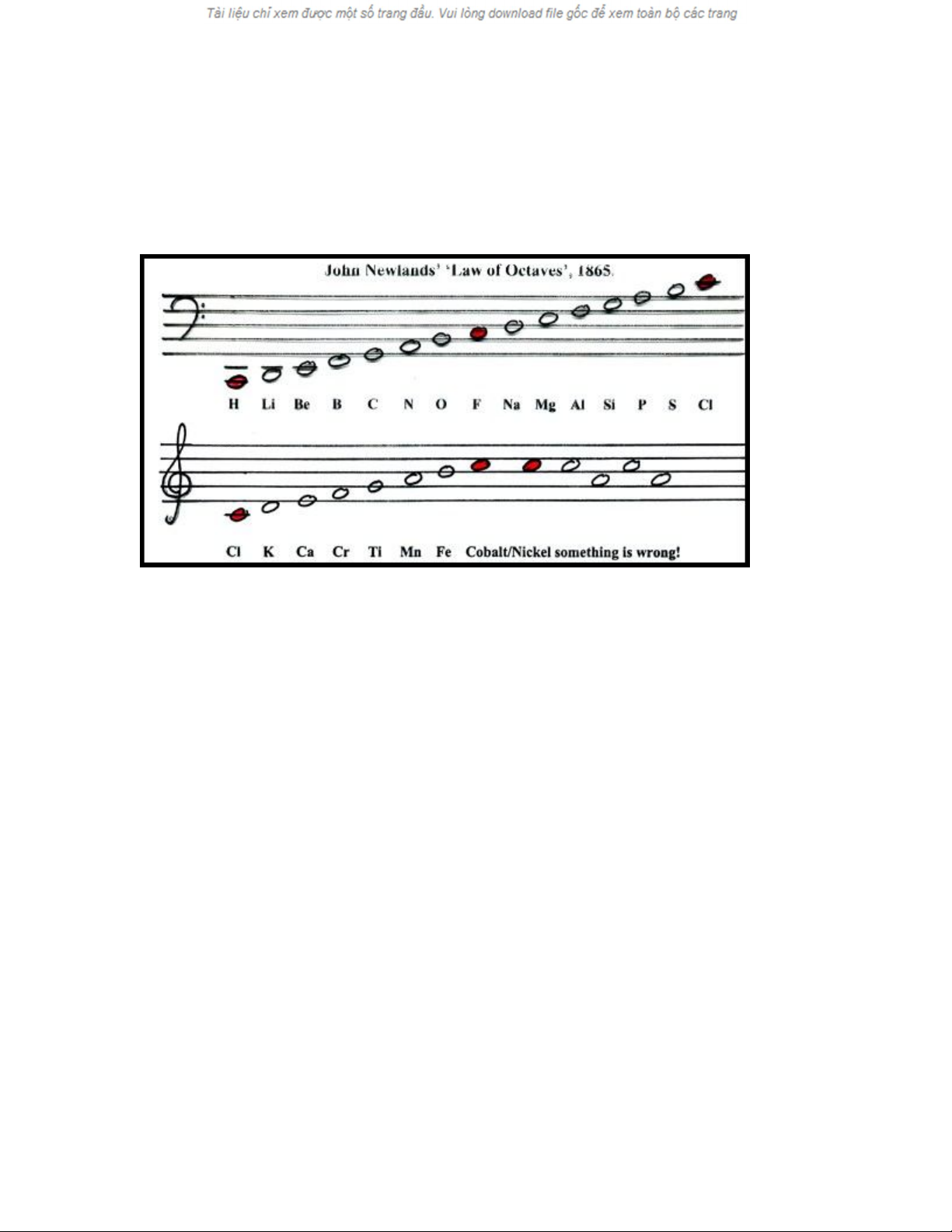
Các cố gắng ban đầu để liệt kê các nguyên tố nhằm thể hiện quan hệ
giữa chúng thông thường là sắp xếp theo trật tự của nguyên tử lượng.
Sự hiểu biết sâu sắc cơ bản của Mendeleev trong phát minh ra bảng
tuần hoàn là sắp đặt các nguyên tố để minh họa sự tuần hoàn của các
tính chất hóa học (thậm chí nếu như điều đó có nghĩa là một số nguyên
tố nhất định không theo trật tự khối lượng, ví dụ Argon có nguyên tử
lượng là 39,948(1) trong khi Kali là nguyên tố xếp sau nó lại chỉ có
nguyên tử lượng là 39,0983(1).), và để lại các lỗ hổng cho các nguyên
tố “bị bỏ sót” (chưa tìm thấy vào thời kỳ đó). Mendeleev sử dụng bảng
của mình để dự đoán các tính chất của các “nguyên tố bị bỏ sót” này,

và nhiều trong số chúng sau này đã được phát hiện ra là phù hợp khá
tốt với các dự đoán.
Với sự phát triển của các học thuyết về cấu trúc nguyên tử (ví dụ thuyết
của Henry Moseley) nó trở thành rõ ràng là Mendeleev đã sắp xếp các
nguyên tố theo trật tự tăng của số nguyên tử (tức là số lượng proton
trong hạt nhân). Trật tự này gần như là đồng nhất với kết quả thu được
từ trật tự tăng của nguyên tử lượng.
Nhằm minh họa các thuộc tính tuần hoàn, Mendeleev đã bắt đầu các
hàng mới trong bảng của mình sao cho các nguyên tố với các tính chất
tương tự nhau nằm trong cùng một cột đứng (“nhóm”).
Với sự phát triển của các lý thuyết trong cơ học lượng tử hiện đại về
cấu hình electron trong phạm vi nguyên tử, nó trở thành rõ ràng là mỗi
hàng ngang (“chu kỳ”) trong bảng tuần hoàn tương ứng với sự điền đầy
lớp lượng tử của các electron. Trong bảng ban đầu của Mendeleev, mỗi
chu kỳ đều có độ dài như nhau. Các bảng ngày nay có các chu kỳ dài
hơn tăng dần lên về phía cuối bảng, và nhóm các nguyên tố trong các
khối s, p, d và f để thể hiện sự hiểu biết của con người về cấu hình
electron của chúng.
Trong các bảng in ra, mỗi nguyên tố thường được thể hiện bằng ký hiệu
nguyên tố và số nguyên tử; nhiều phiên bản còn liệt kê cả nguyên tử
lượng và các thông tin khác, như cấu hình electron vắn tắt của chúng,
độ âm điện và các hóa trị phổ biến nhất. Vào thời điểm năm 2005, bảng
tuần hoàn chứa 116 nguyên tố hóa học mà sự phát hiện ra chúng đã
được xác nhận. Trong số đó, 94 nguyên tố được tìm thấy trong tự nhiên
trên Trái Đất, phần còn lại là các nguyên tố tổng hợp đã được tạo ra
một cách nhân tạo trong các máy gia tốc hạt.
Tính tuần hoàn của các tính chất hóa học
Giá trị chính của bảng tuần hoàn là khả năng dự đoán các tính chất hóa
học của nguyên tố, dựa trên vị trí của nó trong bảng tuần hoàn. Cũng
cần lưu ý là các tính chất hóa học đó thay đổi đáng kể khi chuyển từ cột
này sang cột kia hơn là khi thay đổi từ hàng này sang hàng kia.
Nhóm và chu kỳ
Nhóm
Một nhóm, còn gọi là một họ, là một cột thẳng đứng trong bảng tuần
hoàn.





![Bài tập so sánh hơn và so sánh nhất của tính từ [kèm đáp án/mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250808/nhatlinhluong27@gmail.com/135x160/77671754900604.jpg)
![Tài liệu tham khảo Tiếng Anh lớp 8 [mới nhất/hay nhất/chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250806/anhvan.knndl.htc@gmail.com/135x160/54311754535084.jpg)




![Tài liệu Lý thuyết và Bài tập Tiếng Anh lớp 6 [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250802/hoihoangdang@gmail.com/135x160/18041754292798.jpg)




