
TNU Journal of Science and Technology
230(05): 346 - 352
http://jst.tnu.edu.vn 346 Email: jst@tnu.edu.vn
ASSESSMENT OF HEMOLYTIC TOXICITY OF
CHLORHEXIDINE DIGLUCONATE AND 1200 µg/mL CHLORHEXIDINE
DIGLUCONATE MOUTHWASH SOLUTION
Nguyen Khac Tiep, Nguyen Ngoc Anh, Nguyen Duc Thien*
Ha Noi University of Pharmacy
ARTICLE INFO
ABSTRACT
Received:
15/8/2024
Chlorhexidine digluconate is an active ingredient that can kill many
strains of microorganisms, it can destroy red blood cells causing
hemolysis. The erythrocyte ability of chlorhexidine digluconate is
concentration-dependent, at a concentration of 20 µg/mL it is capable of
disrupting the red blood cell membrane. When chlorhexidine
digluconate solution was at a concentration of 1200 µg/mL, the
hemolysis rate increased to 84.7%, at 2000 µg/mL, the hemolysis rate
was 97.45%. Combining PEG400, PEG4000 and PEG6000 with a
sample solution containing chlorhexidine digluconate 1200 µg/mL, the
% of hemolysis decreases. The concentration of PEG400 is 15% in the
chlorhexidine digluconate 1200 µg/mL sample and does not cause
hemolysis. With PEG4000 at 3% concentration or PEG6000 at 4%
concentration in chlorhexidine digluconate solution at 1200 µg/mL, the
percentage of hemolysis was reduced to less than 5%, the test mixture
was less toxic to red blood cells. The excipients that create flavor, color
and taste in the mouthwash did not cause hemolysis and did not affect
the antibacterial and lytic properties of chlorhexidine digluconate. The
addition of PEG in mouthwashes using the antibacterial agent
chlorhexidine digluconate is necessary to reduce its hemolytic effect.
Revised:
06/02/2025
Published:
07/02/2025
KEYWORDS
Chlorhexidine
PEG
Mouthwash
Cytotoxicity
Hemolytic
KHẢO SÁT ĐỘC TÍNH ĐỐI VỚI MÀNG TẾ BÀO HỒNG CẦU CỦA
DUNG DỊCH CHLORHEXIDINE DIGLUCONATE VÀ
DUNG DỊCH NƯỚC SÚC MIỆNG CHLORHEXIDINE DIGLUCONATE 1200 µg/mL
Nguyễn Khắc Tiệp, Nguyễn Ngọc Ánh, Nguyễn Đức Thiện*
Trường Đại học Dược Hà Nội
THÔNG TIN BÀI BÁO
TÓM TẮT
Ngày nhận bài:
15/8/2024
Chlorhexidine digluconate là hoạt chất có khả năng diệt nhiều chủng vi sinh
vật, nó có thể phá hủy hồng cầu gây ra tan máu. Khả năng phá hủy hồng
cầu của chlorhexidine digluconate phụ thuộc vào nồng độ. Ở nồng độ 20
µg/mL nó đã có khả năng phá vỡ màng tế bào hồng cầu. Khi dung dịch
chlorhexidine digluconate ở nồng độ 1200 µg/mL thì tỷ lệ tan máu tăng lên
84,7%, ở 2000 µg/mL thì tỷ lệ tan máu là 97,45%. Phối hợp PEG400,
PEG4000 và PEG6000 với dung dịch mẫu thử chứa chlorhexidine
digluconate 1200 µg/mL thì tỷ lệ tan máu giảm. Nồng độ PEG400 là 15%
trong mẫu thử chlorhexidine digluconate 1200 µg/mL thì không gây ra tan
máu. Với PEG4000 nồng độ 3% hoặc PEG6000 nồng độ 4% trong dung
dịch chlorhexidine digluconate 1200 µg/mL thì tỷ lệ tan máu giảm xuống
dưới 5%, hỗn hợp thử ít gây độc tính lên tế bào hồng cầu. Các tá dược tạo
mùi, màu và vị trong nước súc miệng không gây tan máu và không ảnh
hưởng đến đặc tính kháng khuẩn và gây tan máu của chlorhexidine
digluconate. Việc bổ sung PEG trong nước súc miệng sử dụng chất kháng
khuẩn chlorhexidine digluconate là cần thiết để giảm khả năng tan máu.
Ngày hoàn thiện:
06/02/2025
Ngày đăng:
07/02/2025
TỪ KHÓA
Chlorhexidine
PEG
Nước súc miệng
Độc tính trên tế bào
Tan máu
DOI: https://doi.org/10.34238/tnu-jst.10947
* Corresponding author. Email: thiennd@hup.edu.vn

TNU Journal of Science and Technology
230(05): 346 - 352
http://jst.tnu.edu.vn 347 Email: jst@tnu.edu.vn
1. Giới thiệu
Hiện nay, các bệnh lý răng miệng như sâu răng, viêm lợi và viêm nha chu đang ngày càng trở
nên phổ biến. Theo Tổ chức Y tế Thế giới, đến năm 2023 có khoảng 3,5 tỷ người trên toàn thế
giới bị ảnh hưởng bởi các bệnh lý răng miệng, trong đó sâu răng và viêm nha chu là hai bệnh
phổ biến nhất, đặc biệt ở trẻ em và người lớn tuổi [1]. Trong bối cảnh đó, các chất sát khuẩn có
nguồn gốc hóa học đã được nghiên cứu và phát triển nhằm hỗ trợ việc kiểm soát và ngăn ngừa
vi khuẩn gây bệnh trong khoang miệng [2]. Chlorhexidine (CHX) là một trong những chất sát
khuẩn được sử dụng rộng rãi và được coi là hóa chất vàng trong việc điều trị và phòng ngừa các
bệnh lý răng miệng.
CHX là một bis- guanide sát khuẩn và khử khuẩn, có hiệu quả trên phạm vi rộng đối với các vi
khuẩn Gram dương và Gram âm, nấm men, nấm da và các virus ưa lipid [3]. In vitro, tác dụng
kháng khuẩn của CHX liên quan đến khả năng làm thay đổi tính thấm của màng tế bào [4]. Ở nồng
độ thấp (0,02%- 0,06%) CHX gây ra sự dịch chuyển ion Ca2+, Mg2+ và mất K+ khỏi thành tế bào,
dẫn đến tác dụng kìm khuẩn [5]. Ở nồng độ cao (> 0,1%), CHX gây rò rỉ tất cả các thành phần nội
bào chính ra khỏi tế bào, dẫn đến tác dụng diệt khuẩn. Tác dụng trên virus của CHX tương tự như
đối với vi khuẩn. CHX có thể vô hiệu hóa các loại virus có vỏ bọc, chẳng hạn như herpes virus, tác
nhân gây ra bệnh nhiễm trùng ngoài da. Tuy nhiên, CHX ít có tác dụng đối với các loại virus không
có vỏ bọc, bao gồm virus gây u nhú ở người (HPV) [6]. Đối với vi nấm, ngoài khả năng làm thay
đổi tính thấm của màng tế bào, tác dụng chống nấm của CHX còn liên quan đến việc ngăn ngừa sự
hình thành biofilm trên cả bề mặt sinh học và phi sinh học [7].
Với tác dụng vượt trội trên, CHX thường được sản xuất ở nhiều dạng bào chế khác nhau như:
nước súc miệng, gel, vecni, v.v. và được sử dụng rộng rãi để điều trị và phòng ngừa các vấn đề liên
quan tới răng miệng. Đi kèm với tác dụng đó, hoạt chất này có thể gây ra độc tính trên các tế bào
tại vị trí sử dụng như độc tính trên tế bào ngà răng [8]. Tuy nhiên, hiện nay có rất ít nghiên cứu
hướng tới đánh giá độc tính của hoạt chất này trên các tế bào.
Xác định tính chất tan máu trong ống nghiệm là một phương pháp phổ biến và quan trọng để
đánh giá sơ bộ độc tính của hóa chất, thuốc hoặc bất kỳ thiết bị hoặc vật liệu y tế nào tiếp xúc với
máu. Đánh giá mức độ mà hợp chất gây ra sự phá vỡ màng hồng cầu, do đó gây ra sự giải phóng
năng lượng tế bào, đây là bước đầu tiên trong các đánh giá độc tính tế bào [9].
Trong nghiên cứu này, chúng tôi sử dụng phương pháp xác định tính chất tan máu từ đó đánh
giá sơ bộ độc tính của dung dịch CHX- D trên tế bào động vật, đại diện ở đây là tế bào hồng cầu.
Đồng thời tiến hành xác định độc tính của một số dun4g dịch nước súc miệng có chứa CHX-D
1200 µg/mL được pha chế tại phòng thí nghiệm khoa Khoa học cơ bản – Trường Đại học Dược
Hà Nội và một chế phẩm chứa CHX 1200 µg/mL có sẵn trên thị trường. Từ đó xác định nồng độ
và loại tá dược pha thêm vào để có thể khử đặc tính tan máu của CHX- D trong nước súc miệng.
2. Nguyên liệu và phương pháp nghiên cứu
2.1. Nguyên liệu
CHX-D 20% hãng Evonik, Đức. Các tá dược NaF, sulcralose, sorbitol, isopropanol, xanh
patent, PEG400, PEG4000 và PEG6000 có nguồn gốc từ Trung Quốc.
Các chủng VSV E. coli ATCC 25922, S. aureus ATCC 33591, C. albicans ATCC 10231, S.
mutans ATCC 25175 được cung cấp bởi phòng nghiên cứu dược lý phân tử và tế bào (FACM) -
Đại học công giáo Louvain, Vương quốc Bỉ và Viện Kiểm nghiệm thuốc Trung ương.
Các dung dịch nước súc miệng chứa CHX - D 1200 µg/mL được bào chế và bảo quản tại phòng
thí nghiệm Khoa Khoa học cơ bản, Trường Đại học Dược Hà Nội. Dung dịch X là chế phẩm có
sẵn trên thị trường và chứa CHX-D nồng độ 1200 µg/mL
Máu chuột được lấy từ chuột bạch từ Viện Vệ sinh dịch tễ Trung ương dùng trong thí nghiệm
xác định độc tính đối với màng tế bào hồng cầu.
TNU Journal of Science and Technology
230(05): 346 - 352
http://jst.tnu.edu.vn 348 Email: jst@tnu.edu.vn
2.2. Phương pháp nghiên cứu
Thử nghiệm tan máu được phát triển từ phương pháp trong công bố của Nguyễn Thu Hằng và
cộng sự [10]. Cụ thể, mẫu máu được lấy và đựng trong ống có chứa Heparin để tránh hiện tượng
đông máu. Cách xử lý máu để loại bỏ hết các thành phần gây đông máu như sau: thêm một thể tích
NaCl 0,9% bằng thể tích máu thu được sau đó đem ly tâm ở tốc độ 4000 vòng/phút, nhiệt độ 4 oC
trong vòng 5 phút trên máy ly tâm lạnh Sigma 3-18K Sartorius. Loại bỏ phần dịch trong nổi ở phía
trên. Lặp lại bước rửa 3 lần. Sau đó pha loãng cặn hồng cầu thu được theo tỉ lệ 1: 100 trong NaCl
0,9% để thu được hỗn dịch hồng cầu 1%.
Chuẩn bị mẫu thử ở nồng độ gấp 10 lần nồng độ cần khảo sát.
Mẫu chứng dương là dung dịch Triton 1%. Mẫu chứng âm là dung dịch NaCl 0,9%.
Sử dụng Eppendorf 2mL, trộn 80 µl với 100 µl hỗn dịch máu thu được ở trên và 20 µl tất cả các
mẫu thử sau đó ủ ở nhiệt độ phòng 20 phút. Đem các mẫu đi ly tâm ở 6000 vòng/phút, nhiệt độ 4
oC trong vòng 2 phút để tách tế bào hồng cầu và thu dịch ly tâm có chứa hemoglobin (nếu tế bào
hồng cầu bị ly giải). Dịch ly tâm thu được chuyển sang đĩa 96 giếng, đo độ hấp thụ A tại bước sóng
405 nm bằng máy đọc vi đĩa 96 giếng huỳnh quang - UV Varioskan Lux. Làm tương tự với mẫu
chứng dương và chứng âm.
Tỷ lệ phần trăn tan máu (HR(%)) được tính theo công thức sau:
𝐻𝑅(%) = 𝐴 𝑚ẫ𝑢 𝑡ℎử − 𝐴 𝑐ℎứ𝑛𝑔 â𝑚
𝐴 𝑐ℎứ𝑛𝑔 𝑑ươ𝑛𝑔 − 𝐴 𝑐ℎứ𝑛𝑔 â𝑚
3. Kết quả và bàn luận
3.1. Độc tính trên tế bào hồng cầu của dung dịch CHX-D
Tiến hành khảo sát độc tính của CHX-D được đánh giá qua khả năng gây ly giải tế bào hồng
cầu với dãy nồng độ tăng dần 20 - 50 – 100 – 200 – 400 – 800 – 1200 - 2000 µg/mL, bắt đầu từ
nồng độ tạo nên tác dụng diệt vi sinh vật. Kết quả được thể hiện dưới dạng đường cong nồng độ
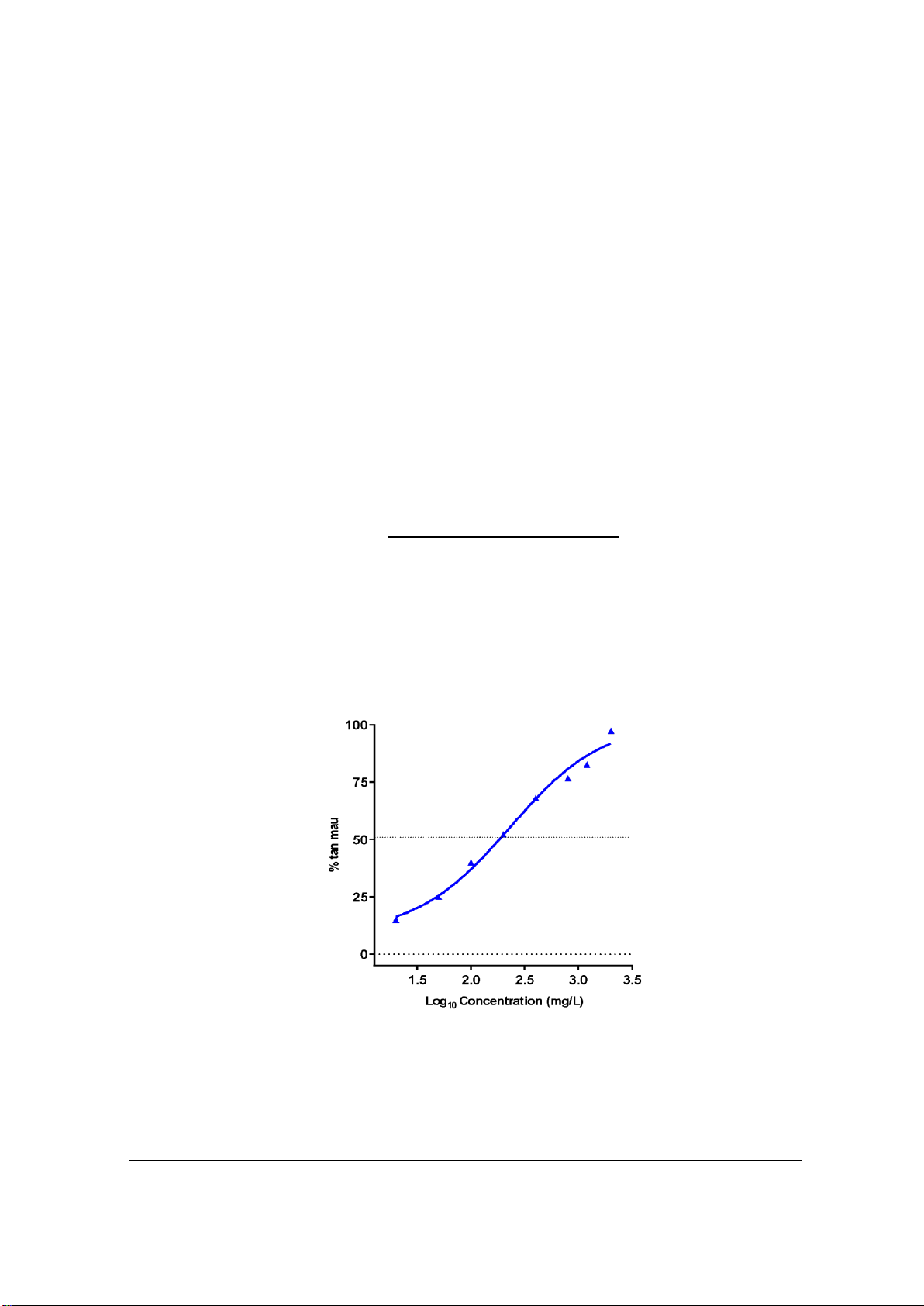
(log10 C – µg/L) - đáp ứng (sự ly giải tế bào hồng cầu - %tan máu) như Hình 1 dưới đây.
Hình 1. Đồ thị HR (%) theo log10 nồng độ dung dịch CHX-D
Trong nhiều nghiên cứu, CHX-D được chứng minh có tác dụng trên vi khuẩn Gram âm, Gram
dương và vi nấm với MIC (nồng độ tối thiểu ức chế vi sinh vật) ở trong khoảng từ 1-6 µg/mL và
MBC/MFC (nồng độ tối thiểu diệt khuẩn/diệt nấm) trong khoảng từ 6-20 µg/mL. Theo Hình 1,
ngay từ các nồng độ gần với giá trị MBC đối với các VSV ở dạng tự do (20 µg/mL), CHX-D có
khả năng làm màng tế bào hồng cầu bị phá vỡ, giải phóng thành phần hemoglobin ra dịch ngoại
TNU Journal of Science and Technology
230(05): 346 - 352
http://jst.tnu.edu.vn 349 Email: jst@tnu.edu.vn
bào, gây ra tan máu. Khả năng phá hủy hồng cầu của CHX-D phụ thuộc vào nồng độ. Khi tăng
nồng độ chất thử, HR tăng. Khi nồng độ CHX-D đạt 1200 µg/mL (0,12%), HR tăng lên 84,7%. Ở
nồng độ 2000 µg/mL (0,2%), CHX-D gây tan máu tương đương với chứng dương là dung dịch
Triton 1% có HR là 97,45%.
CHX-D đã được chứng minh là có khả năng phá hủy hồng cầu ở phạm vi nồng độ tương tự như
nồng độ cần thiết để tạo ra tác dụng kháng khuẩn. Điều này có thể do cách thức CHX-D tác động
lên VSV và gây ra trên tế bào hồng cầu là tương tự nhau [11]. Theo in vitro, tác dụng chống vi
khuẩn của CHX-D đều liên quan đến sự thay đổi tính thấm của màng tế bào. Ở nồng độ thấp (200-
600 µg/mL) CHX-D tạo tác dụng kìm khuẩn. Ở nồng độ cao (>0,1%) CHX-D gây rò rỉ tất cả các
thành phần chính của nội bào ra khỏi tế bào, dẫn đến tác dụng diệt khuẩn [12].
3.2. Độc tính trên tế bào hồng cầu của dung dịch CHX-D phối hợp với PEG
Do tác dụng phá hủy màng hồng cầu cho nên việc sử dụng các dung dịch nước súc miệng (NSM)
có chứa thành phần CHX-D trên các vùng da tổn thương tại niêm mạc miệng có thể ảnh hưởng đến
quá trình chữa lành vết thương.
Trong các công thức NSM có chứa CHX-D, PEG là một tá dược phổ biến, giúp điều chỉnh độ
nhớt của chế phẩm mà không gây kích ứng niêm mạc. Ngoài ra, PEG còn có khả năng làm giảm
tình trạng tan máu của các hợp chất phenolic [13]. Theo Howard C. Ansel, với dung dịch chứa
CHX, khi bổ sung PEG, hoạt tính tan máu của dung dịch sẽ giảm. Nhờ sự có mặt của PEG, quá
trình hấp phụ của CHX lên màng tế bào hồng cầu sẽ bị cản trở, giúp các tế bào trên tồn tại ở trạng
thái nguyên vẹn, không bị phá vỡ [14].
Phối hợp CHX-D 1200 µg/mL với PEG400, PEG4000 và PEG6000 ở các nồng độ khác nhau,
sau đó khảo sát độc tính của các mẫu thử trên thông qua đánh giá khả năng làm ly giải hồng cầu
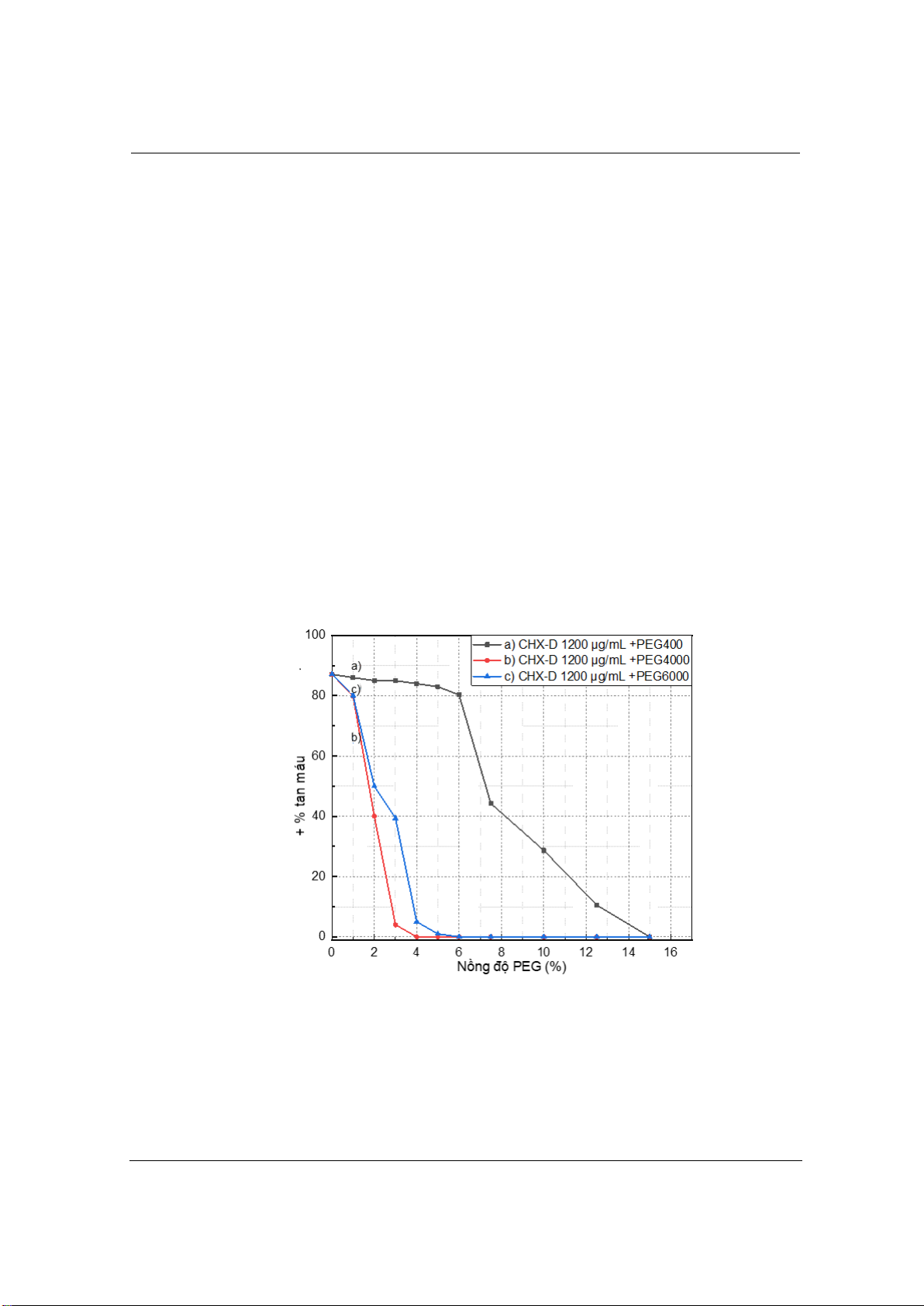
trong máu chuột. Kết quả HR của CHX-D với PEG được thể hiện ở Hình 2.
Hình 2. Đồ thị HR của dung dịch CHX-D 1200 µg/mL khi kết hợp với: a) PEG400, b) PEG4000 và c) PEG6000
Từ kết quả ở Hình 2 cho thấy cả PEG400, PEG4000 và PEG6000 đều có tác dụng làm giảm
độc tính của mẫu thử chứa CHX-D 1200 µg/mL. Nói chung khi nồng độ PEG càng tăng trong mẫu
thử chứa CHX-D 1200 µg/mL thì mức độ tan máu của dung dịch thử càng giảm.
Hình 2a cho thấy dung dịch phối hợp PEG400 ở nồng độ thấp dưới 6% thì tỷ lệ tan máu trên
80%, chưa tạo đáp ứng trên tế bào hồng cầu. Để ngăn chặn hoàn toàn tác động của CHX-D lên tế
bào hồng cầu, nồng độ PEG400 phải tăng đến 15%. Tuy vậy, chế phẩm NSM chứa nồng độ
PEG400 15% sẽ làm ảnh hưởng tới thể chất của dung dịch, gây bất tiện cho người sử dụng.

TNU Journal of Science and Technology
230(05): 346 - 352
http://jst.tnu.edu.vn 350 Email: jst@tnu.edu.vn
Với PEG4000 và PEG6000 phối hợp với dung dịch cho đáp ứng trên tế bào hồng cầu ngay từ
nồng độ thấp ở Hình 2b và 2c. Khi dung dịch thử CHX-D 1200 µg/mL được phối hợp với 1%
PEG4000 hoặc PEG6000, tỷ lệ tan máu của hỗn hợp là 80%. Khi phối hợp dung dịch CHX-D 1200
µg/mL với PEG4000 nồng độ 3% hoặc PEG6000 nồng độ 4%, mức độ ly giải hồng cầu của dung
dịch thử giảm xuống dưới 5%, hỗn hợp thử ít gây độc tính lên tế bào hồng cầu.
Cả 3 loại PEG đều có tác dụng làm giảm độc tính tan máu của dung dịch CHX-D. Phối hợp
PEG400 nồng độ 12,5%, PEG4000 nồng độ 3% hoặc PEG6000 nồng độ 4%, dung dịch CHX 1200
µg/mL ít/ gần như không gây tan máu. Như vậy, PEG có khả năng tác động lên màng tế bào hồng
cầu, ngăn chặn độc tính của CHX-D lên màng tế bào này.
Khảo sát khả năng ảnh hưởng của PEG lên tính chất kháng khuẩn của CHX-D các thí nghiệm
xác định MIC của dung dịch CHX-D khi phối hợp với PEG và MIC của CHX-D nguyên chất. Ở
đây chúng tôi lựa chọn 4 VSV là E. coli, S. aureus, C. albicans, S. mutans có nhiều trong khoang
miệng để khảo sát MIC. Kết quả MIC của dung dịch CHX-D phối hợp với PEG và CHX-D biểu
thị ở Bảng 1.
Bảng 1. MIC của CHX-D và dung dịch CHX-D khi kết hợp với PEG
Dung dịch CHX-D có MIC trong khoảng 1,5-3 µg/mL. Khi bổ sung PEG400 nồng độ 12,5%,
PEG4000 nồng độ 3% hoặc PEG6000 nồng độ 4%, MIC của CHX-D gần như không đổi, dao động
trong khoảng 0,75-6 µg/mL. Phối hợp 3 loại PEG vào dung dịch CHX-D 1200 µg/mL không làm
thay đổi MIC của chất thử. Do vậy, có thể kết luận rằng PEG có tác dụng làm giảm độc tính trên
tế bào hồng cầu của dung dịch CHX-D, tuy nhiên không làm ảnh hưởng tới tác dụng trên VSV của
chất thử.
3.3. Độc tính trên tế bào hồng cầu của dung dịch NSM chứa CHX-D 1200 µg/mL
Trong chế phẩm NSM thường gồm nhiều thành phần có tác dụng hỗ trợ để có sản phẩm thương
mại phù hợp với thị hiếu người tiêu dùng. Cho nên, chúng tôi tiến hành nghiên cứu ảnh hưởng của
các tá dược trong công thức NSM lên tế bào hồng cầu. Ở đây, tỷ lệ khối lượng của các tá dược
thường được sử dụng trong công thức NSM được khảo sát, kết quả tác động lên màng tế bào hồng
cầu ở trong bảng 2.
Bảng 2. Ảnh hưởng của các tá dược trong NSM lên màng tế bào hồng cầu
STT
Thành phần
Hàm lượng
(%)
Tác động lên màng tế bào hồng cầu
1
CHX-D 20%
0,12
Gây độc tính trên tế bào hồng cầu từ nồng độ 20 µg/mL (0,002%)
2
Natri Floride
0,1
Không ảnh hưởng
3
PEG
400
12,5
Không ảnh hưởng
4000
3
Không ảnh hưởng
6000
4
Không ảnh hưởng
4
Sulcralose
0,08
Không ảnh hưởng
5
Sorbitol
4
Không ảnh hưởng
6
Tinh dầu bạc hà
0,015
Không ảnh hưởng
7
Isopropanol
4
Không ảnh hưởng
8
Xanh patent
0,45
Không ảnh hưởng
9
Nước cất 2 lần
Vừa đủ
Không ảnh hưởng
Chủng VSV
MIC (µg/mL CHX-D)
CHX-D
CHX-D 1200 µg/mL +
12,5% PEG400
CHX-D 1200 µg/mL
+ 3% PEG400
CHX-D 1200 µg/mL
+ 4% PEG400
E. coli ATCC 25922
1,5
3
1,5
3
S. aureus ATCC 33591
1,5
1,5
3
3
C. albicans ATCC
10231
1,5
3
1,5
0,75
S. mutans ATCC 25175
3
3
1,5
6























![Giáo trình Bệnh học nội khoa - Trường Cao đẳng Y dược Hà Nội [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20251209/laphong0906/135x160/51721770719192.jpg)


