
Bài giảng quan trắc - khảo sát môi trường 2
lượt xem 26
download
 Download
Vui lòng tải xuống để xem tài liệu đầy đủ
Download
Vui lòng tải xuống để xem tài liệu đầy đủ
Thuỷ quyển là một trong các thành phần cơ bản của môi trường nước, bao gồm toàn bộ các đại dương, sông suối, ao, nước ngầm, băng tuyết, hơi ẩm trong đất và trong không khí. Khối lượng các loại nguồn nước rất khác nhau (94% nước trên trái đất là nước mặn).
Bình luận(0) Đăng nhập để gửi bình luận!
Nội dung Text: Bài giảng quan trắc - khảo sát môi trường 2
- BÀI GIẢNG Môn học: QUAN TRẮC- KHẢO SÁT MÔI TRƯỜNG II (QTKSMT NƯỚC - ĐẤT) 1
- Chương 1: Môi trường nước - Sự ô nhiễm và đánh giá lượng nguồn nước 1.1. Tài nguyên thiên nhiên 1.1.1. Khái quát chung về tài nguyên nước - Thuỷ quyển - một trong các thành phần cơ bản của môi trường nước, bao gồm toàn bộ các đại dương, sông suối, ao, nước ngầm, băng tuyết, hơi ẩm trong đất và trong không khí. - Khối lượng các loại nguồn nước rất khác nhau (94% nước trên trái đất là nước mặn) - Tầm quan trọng: + Là môi trường sống + Điều hoà khí hậu - Chu trình nước tuần hoàn: nước trên trái đất được tuần hoàn theo chu trình, tuỳ theo loại nguồn nước mà thời gian luân hồi cơ thể rất ngắn (một vài tuần hoặc kéo dài hàng ngàn năm). - Thực trạng chung của nguồn tài nguyên nước: + Trử lượng: dồi dào, phong phú. Việt Nam là một trong những quốc gia có trử lượng nước hàng đầu thế giới. + Chất lượng: thiếu nguồn nước sạch ( nước có thể uống được). + Xu thế biến đổi: Có dấu hiệu bị ô nhiễm ở các khu đô thị, khu công nghiệp,… 1.1.2. Thành phần hoá học của nguồn nước - Các hợp chất vô cơ, hữu cơ trong nước tự nhiên có thể tồn tại ở dạng ion hoà tan, khí hoà tan, dạng rắn hoặc lỏng. - Chính sự phân bố các chất này quyết định bản chất của nướ tự nhiên: ngọt, mặn, giàu hoặc nghèo dinh dưỡng, cứng hoặc mềm, bị ô nhiễm nặng hoặc nhẹ,… 2
- 1.1.2.1. Các ion hoà tan - Trong nước tự nhiên có các ion hoà tan: Cl-, Na+, SO42- ,Mg2+,Ca2+,HCO3-,… - Hàm lượng các nguyên tố hoá học phân bố phụ thuộc vào + Đặc điểm khí hậu + Địa chất, địa hình + Độ dốc của lưu vực + Nguồn thải chất ô nhiễm - Để xác định các ion hoà tan trong nước: dùng chỉ số TDS (tổng chất rắn hoà tan = Total dislove sodid) 1.1.2.2. Các khí hoà tan - Hầu hết các khí đều hoà tan hoặc phản ứng với nước (trừ metan): O2, CO2, NH3, H2S,… - O2: Độ bảo hoà phụ thuộc chủ yếu vào nhiệt độ nước, áp suất khí quyển trên bề mặt và một phần vào độ mặn. - NH3, H2S: do sự phân huỷ các hợp chất hữu cơ. 1.1.2.3. Các chất rắn Bao gồm vô cơ, hữu cơ và sinh vật: - Chúng được phân thành 02 loại, phụ thuộc vào kích thước + Loại chất rắn có thể lọc được d ≤ 10 - 6m: • Dạng keo: 10-9 - 10-6m • Dạng hoà tan: < 10-9m + Loại chất rắn không lọc được: • d ≥ 10-6m → tảo • d: 10-5 - 10-6m → hạt bùn (lơ lửng) • d > 10-5m → cát, sạn (lắng được) - Chất rắn có thể phân loại theo độ bay hơi ở nhiệt độ sấy (1030C – 1050C) + Chất rắn bay hơi + Chất rắn không bay hơi 3
- 1.1.2.4. Chất hữu cơ - Chất hữu cơ dễ bị phân huỷ sinh học: đường, chất héo,prôtêin,… - Chất hữu cơ khó bị phân huỷ sinh học: PCB, Dioxin,… 1.1.3. Thành phần sinh học của nguồn nước tự nhiên - Chỉ thị cho độc tính sinh thái của nguồn nước - Một số loài sinh vật gây ô nhiễm hoặc làm sạch nguồn nước tự nhiên * Vi khuẩn và nấm * Siêu vi trùng(vi rút) * Tảo * Các loại thực vật và sinh vật khác 1.2. Các thông số đánh giá chất lượng nguồn nước 1.2.1. Các chỉ tiêu vật lý 1.2.1.1. Nhiệt độ Nhiệt độ của nước thải sinh hoạt thường cao hơn nhiệt độ của nước cấp do việc xả các dòng nước nóng hoặc ấm từ các hoạt động sinh hoạt, thương mại hay công nghiệp và nhiệt độ của nước thải thwongf thấp hơn nhiệt độ của không khí. Nhiệt độ của nước thải là một trong những thông số quan trọng bởi vì phần lớn các sơ đồ công nghệ xử lý nước thải đều ứng dụng các quá trình xử lý sinh học mà các quá trình đó thường bị ảnh hưởng mạnh bởi nhiệt độ. Nhiệt độ của nước thải ảnh hưởng đến đời sống của thủy sinh vật, đến sự hòa tan oxy trong nước. Nhiệt độ còn là một trong những thông số công nghệ quan trọng liên qun đến quá trình lắng các hạt cặn. Nhiệt độ của nước thải thường thay đổi theo mùa và vị trí địa lý. Ở những vùng khí hậu lạnh, nhiệt độ của nước thải có thể thay đổi từ 7 ÷ 180C, trong khi đó ở những vùng có khí hậu ấm hơn, nhiệt độ của nước thải có thể thay đổi từ 13 đến 240C. - Phụ thuộc vào nhiệt độ của môi trường (nước mặt) - Nhiệt độ nước ngầm ít thay đổi 4
- - Xác định nhiệt độ bằng nhiệt độ bằng nhiệt kế 1.2.1.2. Màu Màu của nước thải là do các chất thải sinh hoạt, công nghiệp, thuốc nhuộm hoặc do các sản phẩm được tạo ra từ các quá trình phân hủy các chất hữu cơ. Độ màu là thông số thường mang tính chất định tính, có thể đwocj sử dụng để đánh giá trạng thái chung của nước thải. Nước thải sinh hoạt để chưa quá 6h thường có màu nâu nhạt. Màu xám nhạt đến trung bình là đặc trưng của các loại nước thải đã bị phân hủy một phần. Nếu xuất hiện màu xám sẫm hoặc đen, nước thải coi như đã bị phân hủy hoàn toàn bởi các vi khuẩn trong điều kiện yếm khí. Hiện tượng nước thải ngả màu đen thường là do sự tạo thành các sulfide khác nhau, đặc biệt là sulfide sắt. Điều này xảy ra khi khi hydro sulfua được sản sinh ra dưới điều kiện yếm khí kết hợp với một kim loại hóa trị 2 có trong nước. - Phụ thuộc vào các chất hoà tan trong môi trường nước - Phụ thuộc vào sự phát triển của các thực vật trong nước, vi sinh vật trong nước - Xác định màu → so với thang màu chuẩn: Pt - Co;Cr - Co Điển hình: * Nước có sắt Fe3+ → có màu nâu đỏ * Các hchc dạng humic → màu vàng * Tảo lam → xanh * Nước thải SH, CN: màu xám → màu đen 1.2.1.3. Mùi Việc xác định mùi của nước thải ngày càng trở nên quan trọng, đặc biệt là các phản ứng gây gắt của dân chúng đối với các công trình xử lý nước thải không được vận hành tốt. Mùi của nước thải còn mới thường không gây ra các cảm giác khó chịu nhưng một loạt các hợp chất gây mùi khó chị sẽ được tỏa ra khi nước thải bị phân hủy sinh học dưới điều kiện yếm khí. 5
- - Phụ thuộc vào sản phẩm phân huỷ các chất hữu cơ Ví dụ: + H2S → mùi trứng thối + NH3 → mùi khai,… - Phụ thuộc sự phát triển hệ động thực vật trong nước - Phương pháp xác định: + Ở nhiệt độ thường: lắc mạnh, mỡ nhanh nút → dùng khứu giác để xác định + Đun nóng 40 - 500C, sau khi lắc nhẹ → dùng khứu giác để xác định Chú ý: Chỉ xác định đối với những nguồn nước không có dấu hiệu ô nhiễm 1.2.1.4. Độ đục Đọ đục của nước là do các chất lơ lửng và các chất dạng keo chứa trong nước thải tạo nên. Đơn vị đo độ đục thông dụng là NTU. Giữa độ dục và hàm lượng chất lơ lửng trong nước thải ban đầu (chưa xử lý) chưa có mối quan hệ đáng kể nào, tuy nhiên mối quan hệ này thể hiện rõ ở nước sau khi ra khỏi bể lắng 2 và được tính bằng công thức: Chất lơ lững, SS (mg/l) = (2.3 ÷ 2.4)* độ đục (NTU) Phụ thuộc vào khả năng xuyên suốt của ánh sáng 1.2.1.5. Độ dẫn Phụ thuộc vào hàm lượng các ion hoà tan trong nước 1.2.2. Các chỉ tiêu hoá học 1.2.2.1. DO - Rất quan trọng đối với nước mặt - Sơ bộ đánh giá được chất lượng nguồn nước: * Do cao → nguồn nước sạch * DO thấp → nguồn nước bị ô nhiễm - Với hệ thống xử lý nước thải → dùng giá trị DO để kiểm tra, đánh giá hiệu quả quá trình làm sạch - Sự phụ thuộc của DO vào các yếu tố: 6
- * Nhiệt độ: nhiệt độ cao → DO thấp * Áp suất * Diện tích bề mặt * Nồng độ muối (nồng độ muối cao → DO giảm) * Sự phát triển của hệ động thực vật (DO biến thiên theo thời gian) * Hàm lượng các chất hữu cơ - Phương pháp xác định: * Phương pháp Winkler * Đo bằng điện lực 1.2.2.2. Fe - Tiêu chuẩn: * Nước cấp sinh hoạt : 0,3mg/l (tiêu chuẩn cũ), 0,5mg/l (tiêu chuẩn mới) * Nước mặt: 1mg/l * Nước ngầm: 1-5mg/l - Sự phụ thuộc hàm lượng Fe: Trong nước ngầm tồn tại ở dạng Fe2+ nhưng khi ra ngoài không khí tồn tại ở dạng Fe3+. Nồng độ Fe phụ thuộc vào nguồn nước 1.2.2.3. Mn - Đối với nguồn thải người ta thường ít quan tâm. - Quan tâm ở nguồn nước cấp - Tiêu chuẩn: [Mn] ≤ 0.1mg/l (tiêu chuẩn cũ) ≤ 0,5mg/l (tiêu chuẩn mới) 1.2.2.4. Ca - Mg - Trong nước mặt, thông thường hàm lượng Ca, Mg tương đương với tiêu chuẩn cho phép - Trong nước ngầm giá trị (Hàm lượng) Ca, Mg thay đổi tuỳ thuộc vào địa chất, vùng. 1.2.2.5. NH3 - NH4+ - Cần khảo sát, phân tích đối với nước ngầm 7
- - Đối với trạm xử lý cần phải khử các muối ammôni - Phụ thuộc vào giá trị pH. Với các khoảng pH khác nhau thì thông thường chúng tồn tại ở các dạng khác nhau ( hoặc là NH3 hoặc là NH4+). 1.2.2.6. NO2-,NO3- - Là sản phẩm trung gian của quá trình của quá trình oxi hoá các hợp chất ammoni - Theo tiêu chuẩn: * Nước cấp sinh hoạt: NO3- ≤ 30mg/l (tiêu chuẩn cũ) ≤ 50mg/l (tiêu chuẩn mới) NO2- = 0 (tiêu chuẩn cũ) ≤ 0,1 mg/l (tiêu chuẩn mới) * Chất lượng nước mặt: N - NO3- : 10 - 15mg/l N - NO2- : 0,01 - 0,05mg/l 1.2.2.7. PO43- - Đối với nước ngầm thì không cần quan tâm, thông thường giá trị của nó rất nhỏ. Thông qua thông số (chỉ tiêu) PO43- để đánh giá sự phú dưỡng nguồn - nước - Trong công nghệ xử lý nước thải: N,P là nguyên tố dinh dưỡng 1.2.3. Các chỉ tiêu sinh học - Nhóm coliform đặc trưng là Escherichia E.Coli: Chọn E.Coli vì nó phổ biến, đặc trưng cho nguồn nước có bị ô nhiễm phân không, có khả năng tồn tại cao trong các môi trường. - Các loại rong tảo: đặc trưng cho sự nhiễm bẩn các chất hữu cơ, sự phú dưỡng nguồn nước ( Eutrofication) 8
- 1.3. Các nguồn gây ô nhiễm môi trường nước 1.3.1. Nước thải đô thị - Nguồn gốc: từ hoạt động sinh hoạt và dịch vụ hàng ngày của con người - Đặc điểm nguồn thải: nguồn thải nhỏ, phân tán - Lưu lượng thải * Phụ thuộc vào tập quán sinh hoạt * Phụ thuộc vào thiết bị vệ sinh * Phụ thuộc vào tiêu chuẩn cấp nước - Chế độ thải: không ổn định - Tích chất, thành phần: * Tính chất: Có màu từ trắng đục đến xám đen Có mùi hôi. * Thành phần: Chứa nhiều hợp chất hữư cơ không bền vững, dễ bị phân huỷ sinh học (cacbon hydrat, pr, mỡ, thức ăn dư thừa,…) → gây mùi hôi, màu. Chứa các chất dinh dưỡng N, P Chứa các vi trùng, vi khuẩn gây bệnh. 1.3.2. Nước thải công nghiệp - Nguồn gốc: Nước thải từ các nhà máy, xí nghiệp, cơ sở sản xuất,.. - Đặc điểm thải: tập trung - Lưu lượng thải và chế độ thải: phụ thuộc vào qui trình công nghệ - Tính chất, thành phần: phụ thuộc vào qui trình công nghệ, đặc thù của từng nhà máy, xí nghiệp hay cơ sở sản xuất. 1.3.3. Nước mưa chảy tràn - Nguồn gốc: do nước mưa chảy tràn trên mặt đất - Đặc điểm nguồn thải: phụ trhuộc vào mùa, lượng mưa. - Tính chất, thành phần: Chứa chất rắn (Vô cơ, hữu cơ), thuốc trừ sâu, phân bón, dầu mỡ, hoá chất, vi trùng, vi khuẩn,… 9
- 1.3.4. Hoạt động tàu thuyền và các hoạt động khác - Nước thải từ các hoạt động sinh hoạt - Nước thải từ các hoạt động khác: nước mưa, từ các vùng xử lý CTR. 1.4. Các chất gây ô nhiễm nước và phương pháp xác định 1.4.1. Các phương pháp phân tích thường gặp trong việc xác định nồng độ các chất gây ô nhiễm môi trường nước 1.4.1.1. Phương pháp chuẩn độ 1.4.1.2. Phương pháp trọng lượng 1.4.1.3. Phương pháp cực phổ 1.4.1.4. Phương pháp đo quang (trắc quang) 1.4.2. Các chất gây ô nhiễm môi trường nước và phương pháp xác định 1.4.2.1. Các chất lơ lững SS (Suspend Solid) - Nguồn gốc: + Xói mòn, rửa trôi + Cọ xát dòng chảy, lắng đọng bụi + Do sự phát triển của hệ thống động thực vật trong nước + Do hoạt động của con nghười - Ảnh hưởng đến chất lượng nguồn nước + Làm giảm giá trị sử dụng nguồn nước + Làm tăng độ đục, khả năng truyền ánh sáng kém → ảnh hưởng đến sự sinh trưởng và phát triển của hệ động thực vật trong nước + Tăng chi phí xử lý nước cấp cho sinh hoạt. - Phương pháp xác định: phương pháp cân trọng lượng 1.4.2.2. Các chất hữu cơ (COD, BOD) Gồm 02 loại: + Chất hữu cơ dễ phân huỷ sinh học + Chất hữu cơ khó phân huỷ sinh học 10
- 1. Chất hữu cơ dễ phân huỷ sinh học - Khái niệm: là các chất hữu cơ trong điều kiện tự nhiên có khả năng (dễ) chuyển hoá thành các dạng khác (đặc trưng bởi thông số BOD5) - Sự chuyển hoá: Các quá trình sinh hoá + Quá trình oxy hoá sinh học hiếu khí CHC + O2 → CO2 + H2O + Quá trình oxy hoá sinh hoạt sinh hoạt yếm khí - Mức độ tác động: khi môi trường nước bị ô nhiễm bởi các chất hữu cơ dễ phân huỷ sinh học → xảy ra các quá trình sinh học hiếm khí → làm giảm lượng O2 hoà tan trong nước: + Ảnh hưởng đến hệ động vật nước (O2 thấp trong thời gian dài) + Tạo thuận lợi cho quá trình sinh học yếm khí – gây mùi hôi thối - giảm giá trị sử dụng nhiều nước. - Phương pháp xác định: xác định gián tiếp thông qua quá trình tiêu thụ O2 trong quá trình sinh hoá. 2. Chất hữu cơ khó phân huỷ sinh học ( hchc bền vững) Gồm 02 loại: + Độc + Không độc (ít độc) a. Không độc (ít độc): dầu, mỡ động vật… - Khó và chậm phân huỷ trong thời gian dài - Các hợp chất này tạo thành lớp màn trên bề mặt môi trường nước → DO giảm → huỷ diệt hệ sinh vật trong môi trường nước. - Các hợp chất dầu mỡ dễ phân tán vào môi trường nước bao bọc quanh sinh vật phù du, thức ăn, chất bẩn → sinh vật sử dụng chúng làm thức ăn → không chuyển hoá được thức ăn → sinh vật bị chết. b. Độc: - Thuốc trừ sâu, thuốc diệt cỏ: Nồng độ lớn gây chết sinh vật trong nước, con người 11
- Ví dụ: DDT gây tiệt chủng các loại động vật bậc cao. c. Phương pháp xác định: - Xác định gián tiếp, xác định lượng O2 tiêu thụ bằng các chất oxy hoá các chất hữu cơ khó phân huỷ ( dùng KMnO4, K2Cr2O7) - CODMn, CODcr. Việc giám sát và quản lý các chất có độc tính cao được qui đinh chặt chẽ trong các tiêu chuẩn nhà nước và các tổ chức thế giới cho từng loại nguồn nước và cho từng mục đích sử dụng khác nhau. Để đánh giá tổng hợp các chất trong nước, người ta dung các thông số sau: 1. Tổng cacbon hữu cơ ( TOC): là tỷ lệ giữa khối lượng cacbon so với khối lượng hợp chất. TOC được tính dựa trên công thức của hợp chất bằng gam hoặc miligam cacbon theo thể tích (mg/m3, mg/l) 2. Nhu cầu oxy lý thuyết ( ThOD): là lượng oxy cần thiết để oxy hoá một đơn chất. ThOD được tính bằng gam hoặc miligam oxy theo thể tích dựa theo các phương trình phản ứng giữa các hchc và oxy (mg/m3, mg/l) 3. Nhu cầu oxy sinh hoá (BOD): là lượng oxy cần thiết để phân huỷ các hchc bằng vi sinh vật. Thông số này rất quan trọng, nó là thông số cơ bản đánh giá mức độ ô nhiễm, BOD càng lớn thì mức độ ô nhiễm càng cao. Đơn vị mg/l, g/m3 4. Nhu cầu oxy hoá học (COD): là lượng oxy cần thiết để oxy hoá hoá học các hợp chất hữu cơ 1.4.2.3. Các kim loại nặng: pb, Hg, As, Cd, Cr, Ni,… - pb: Có độc tính với não, có thể gây nhiễm độc nặng. Chúng có khả năng tích luỹ lâu dài trong cơ thể. + Trong nước sông - hồ có lượng vết: 0.05 - 40mg/l + Nước biển không bị ô nhiễm, [pb] = 0.03mg/l - Hg: rất độc đối với người và thuỷ sinh. [Hg] cho phép trong nước uống: 0.001mg/l [Hg] cho phép trong nước nuôi trồng thuỷ sản: 0.005mg/l - As: là chất độc, khả năng gây ung thư cao 12
- + Nước tự nhiên có chứa vết As với nồng độ khoảng 0.01mg/l + Tiêu chuẩn nước uống là 0.05mg/l, nước nuôi cá là 0.025mg/l 1.4.2.4. Các chất dinh dưỡng (hợp chất N,P) - Sự tự ô nhiễm → phú dưỡng nguồn nước. Các thực vật sống trong môi trường này phát triển rất mạnh - Một số chất tiêu biểu 1. Ammôni (NH4+): Trong nước tự nhiên không ô nhiễm có vết ammôni ( dưới 0.05 ppm). Nồng độ ammôni trong nước ngầm cao hơn. Lượng ammôni trong nước thải sinh hoạt và công nghiệp hoá chất, chế biến thực phẩm có thể lên tới 100mg/l. Nếu lượng ammôni trên 5mg/l nguồn nước dược xem là ô nhiễm nặng. 2. Nitrat (NO3-): là sản phẩm cuối cùng của sự phân huỷ các chất có Nitơ chứa trong chất thải của người và động vật. Trong nước tự nhiên, nồng độ nỉtat thường dưới 5mg/l. Ở vùng bị ô nhiễm nồng độ nitrat cao trên 10mg/l. Nitrat trong nước uống không được quá 10mg/l. Đây là chất dinh dưỡng của rong, tảo. 3. Phôtphat (PO43-): có nhiều trong nước thải, phân người, súc vật và trong nước thải của các nước thải của các ngành sản xuất phân lân, thực phẩm. Đây cũng là chất dinh dưỡng cho rong tảo phát triển. Nồng độ phôtphat trong nước không ô nhiễm thường nhỏ hơn 0.01mg/l. Hàm lượng trong nước uống tối đa là 6mg/l. 1.4.2.5. Các vi sinh vật Nguồn gốc: Nước thải bệnh viện, các nước thải từ các lò giết mổ gia súc,… 1.5. Đánh giá mức độ ô nhiễm nguồn nước Bảng đánh giá tổng hợp chất lượng nguồn nước mặt ( Bảng phân loại Kolvits Marson) 13
- Trạng % NH4+ NO3- PO43- thái COD BOD STT pH Oxy bảo nguồn mg/l mg/l mg/l mg/l mg/l hoà nước 1 Nước rất sạch 7-8 < 0.05 < 0.1 < 0.01 100 8 > 0.3 100 > 10 1.6. Các tiêu chuẩn liên quan đến chất lượng nước Tuỳ theo nguồn nước khác nhau → sử dụng các tiêu chuẩn tương ứng để đánh giá chất lượng nguồn nước Vd: TCVN 5942:1995: Cln – T/c chất lượng nước mặt TCVN 5943: 1995: Cln – T/c chất lượng nước biển ven bờ TCVN 5944: 1995: Cln – T/c chất lượng nước ngầm 14
- Chương 2: Mẫu nước thải - Lấy mẫu- bảo quản và vận chuyển 2.1. Lựa chọn vị trí lấy mẫu Tuỳ vào mục đích (đánh giá hiện trạng, đánh giá tác động của nguồn thải) mà người ta lựa chọn các vị trí lấy mẫu khác nhau và sử dụng một số phương pháp lấy mẫu nước thải khác nhau. Tuy nhiên dù vị trí lấy mẫu hay phương pháp lấy mẫu khác nhau nhưng mẫu lấy phải đại diện cho nguồn nước cần được xem xét, đánh giá. 2.1.1. Sự phân bố các chất ô nhiễm Sự phân bố các chất ô nhiễm trong các vùng khác nhau: - Theo diện tích: ở các vị trí khác nhau nồng độ các chất ô nhiễm khác nhau. - Theo chiều sâu: Trên bề mặt xảy ra quá trình oxy hóa sinh hóa hiếu khí → chất lượng nước sạch hơn. - Vùng giáp ranh. 2.1.2. Các yếu tố liên quan Cần xem xét ảnh hưởng của một số yếu tố đến sự pha loãng các chất ô nhiễm trong lưu vực đang xem xét. - Vận tốc dòng chảy: liên quan đến lượng oxy hòa tan → ảnh hưởng đến hàm lượng chất hữu cơ trong môi trường nước. - Thành phần địa chất trong lưu vực: lưu ý đến khi số liệu khảo sát bất thường. 2.1.3. Các số liệu đặc trưng cơ bản - Các số liệu về lòng dẫn: chiều dài, diện tích. - Lưu lượng - Các nguồn gây ô nhiễm : * Xác định số điểm lấy mẫu 15
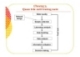
- * Làm cơ sở giải thích kết quả đo * Xác định các chỉ tiêu cần phân tích Riêng đối với nước thải công nghiệp phải xem xét chế độ thải 2.2. Các dạng mẫu Có 02 loại mẫu: Mẫu đơn và mẫu tổ hợp 2.2.1. Mẫu đơn - Loại mẫu được lấy tại 1 điểm, ở thời điểm cụ thể, chỉ đại diện cho thành phần của nguồn tại thời điểm và địa điểm đó. - Có thể đại diện cho chất lượng nguồn nước ở lưu vực nếu ở khu vực đó có sự xáo trộn mảnh liệt theo diện tích, theo chiều sâu được coi là đồng nhất. Lấy mẫu đơn là cách đơn giản nhất để quan trắc các dòng thải. Tuy nhiên phương pháp này chỉ đưa ra một bức tranh riêng lẻ và tức thời về đối tượng quan trắc. Phương pháp lấy mẫu này chỉ thích hợp ở một số điều kiện nhất định khi các đặc trưng của dòng thải không biến đổi trong một khoảng thời gian dài. 2.2.2. Mẫu tổ hợp Mẫu tổ hợp cung cấp thông tin chính xác hơn mẫu đơn vì đặc tính của dòng thải thường dao động và rất khó dự đoán. Có 03 loại mẫu tổ hợp: • Tổ hợp theo không gian • Tổ hợp theo thời gian • Tổ hợp theo lưu lượng 2.2.2.1. Mẫu tổ hợp theo không gian Bao gồm các mẫu đơn có thể tích bằng nhau và được lấy đồng thời tại các địa điểm khác nhau. Thường sử dụng để lấy giá trị trung bình cho các mặt cắt ngang hoặc mặt cắt dọc của dòng nước. 16
- Mẫu đại diện cho chất lượng nước tại mặt cắt đó, được lấy ở thời điểm nước đứng, dòng chảy ổn định. Ví d ụ : Mẫu tổ hợp A Mặt cắt dọc 1 2 Mẫu tổ hợp A B 1 2 Mặt cắt ngang 3 B Chú ý: Khi sử dụng mặt cắt trong quá trình khảo sát, phân tích cần phải thu gọp các điểm lấy mẫu lại để tiết kiệm chi phí cho quá trình khảo sát, phân tích. Cần sử dụng mặt cắt ở các nơi khác biệt. 2.2.2.2. Mẫu tổ hợp theo thời gian Bao gồm những mẫu đơn có thể tích bằng nhau và được lấy ở các khoảng thời gian bằng nhau trong một chu kỳ. Lấy mẫu tổ hợp theo thời gian thường được áp dụng để nghiên cứu chất lượng trung bình của nguồn nước theo chu kỳ (ngày đêm, chu kỳ triều,…) 2.2.2.3. Mẫu tổ hợp theo lưu lượng - Khi lưu lượng thay đổi thì chất lượng nước thay đổi. - Bao gồm các mẫu đơn ở các khoảng thời gian bằng nhau nhưng theo tỷ lệ lưu lượng dòng thải 17
- - Dùng để khảo sát dòng thải công nghiệp Chú ý: Đối với mẫu tổ hợp, từng mẫu đơn cần lấy với thể tích ≥ 50ml. Thường chọn khoảng 200 – 300ml. Tất cả các mẫu đơn phải được lấy với thể tích 1 – 2 lít Mẫu tổ hợp từ n mẫu thường được lấy 1 – 2 lít/n. 2.3. Kỹ thuật lấy mẫu Tùy theo mục đích chúng ta có thể lựa chọn vị trí lấy mẫu, thời điểm lấy mẫu, thời gian lấy mẫu để tránh sự khác biệt của các thành phần trong mẫu nước. 2.3.1. Lấy mẫu nước sông - Điểm lấy mẫu thường là các địa danh dễ nhớ, hoặc thuận tiện cho việc lấy mẫu. - Điểm lấy mẫu chọn nơi dòng chảy có sự xáo trộn mạnh nhất (chọn vị trí giữa dòng đối với dòng chảy nhỏ) * Đối với dòng chảy hẹp: 01 vị trí * Đối với dòng chảy rộng: 03 vị trí (trái, phải, giữa dòng: tại các vị trí này có trường vận tốc khác nhau). - Nếu dòng chảy không có gì đặc biệt, mẫu được lấy cách mặt nước 20 ÷ 30 cm, là các mẫu đơn hay mẫu tổ hợp. - Khi lấy mẫu nước sông cần chú ý: * Nếu Sông đồng nhất → mẫu được lấy cách bề mặt 30 ÷ 40 cm * Nếu Sông không đồng nhất → cần lấy mẫu theo độ sâu: H ≤ 1m → chọn 1 điểm lấy mẫu H = 1 – 2m → chọn 2 điểm lấy mẫu H ≥ 3m → chọn 3 điểm lấy mẫu Việc xác định tính đồng nhất hay không đồng nhất dựa và sự biến thiên nhiệt độ. Đây là thông số điều khiển tất cả các quá trình trong tự nhiên. Khi 18
- nhiệt độ khác nhau thì các quá trình xảy ra cũng khác nhau dẫn đến giá trị các thông số cũng khác nhau. - Khi nghiên cứu tác động của dòng nhánh, nguồn thải tới chất lượng nước trong dòng chính thì xác định 02 điểm : thượng lưu và hạ lưu. Điểm hạ lưu phải đủ xa để có sự xáo trộn hoàn toàn, L khoảng 1km. Điểm thượng lưu phải đủ xa để nguồn thải không ảnh hưởng đến địa điểm đo. Q1 L = 1000 m M1: thượng lưu M2: Hạ lưu - Đối với sông chịu ảnh hưởng của thủy triều (cửa sông). Khi xác định điểm lấy mẫu cần có bảng thủy triều để xác định thời điểm lấy mẫu 2.3.2. Lấy mẫu nước ao, hồ (các nguồn nước đứng) Tùy theo độ sâu, hình dáng, tùy theo điều kiện cụ thể mà lấy mẫu đơn hay mẫu tổ hợp. Khi lấy mẫu tổ hợp → có sự thay đổi theo độ sâu: • Điểm 1: cách mặt nước 10 ÷ 30cm. • Điểm 2: cách đáy 100cm. Nếu lấy mẫu theo độ sâu cần xác định độ giảm nhiệt: • Ở bề mặt → lấy mẫu • Ở tầng suy nhiệt → lấy mẫu • Ở tầng đáy → lấy mẫu 19
- Tầng mặt Tầng đáy 2.3.3. Lấy mẫu nước ngầm (nước giếng) - Lấy mẫu bằng bơm: lấy sau khi bơm 20 ÷ 30 phút. - Lấy theo chiều sâu: tương tự như lấy mẫu theo các độ sâu khác. 2.3.4. Lấy mẫu nước thải Địa điểm phải đại diện cho dòng thải cần khảo sát Có 02 loại nước thải: • Nước thải công nghiệp • Nước thải đô thị. Với nước thải công nghiệp: cần phải xem xét qui trình công nghệ → xác định thời gian lấy mẫu, lựa chọn thời điểm lấy mẫu. Với nước thải đô thị: các khoảng thời gian lấy mẫu khác nhau. Có 02 vị trí lấy mẫu thường chọn: • Lấy mẫu tại các cống thải, kênh thải và hố ga • Lấy mẫu tại đầu vào của trạm xử lý. Các lưu ýkhi lấy mẫu tại hiện trường 1. Lưu ý khi lấy mẫu đại diện: Chương trình lấy mẫu, lựa chọn vị trí lấy mẫu thích hợp và lên kế hoạch chi tiết cho việc lấy mẫu là hết sức quan trọng nhằm lấy được mẫu đại diện. Các yêu cầu tối thiểu khi lấy mẫu đại diện: 20

CÓ THỂ BẠN MUỐN DOWNLOAD
-

Báo cáo thực hành quan trắc
 16 p |
16 p |  489
|
489
|  104
104
-
Bài giảng Quan trắc môi trường - Chương 3: Quan trắc môi trường nước
 33 p |
33 p |  1269
|
1269
|  76
76
-

Bài giảng Quản trắc môi trường
 125 p |
125 p |  227
|
227
|  60
60
-

Bài giảng Quản lý môi trường: Chương 5
 67 p |
67 p |  191
|
191
|  40
40
-

Quan trắc môi trường
 62 p |
62 p |  224
|
224
|  38
38
-

Bài giảng Kiểm soát ô nhiễm môi trường nước do nước thải: Chuyên đề 3 - Quản lý, giám sát và quan trắc tài nguyên - môi trường nước, nước thải
 73 p |
73 p |  210
|
210
|  37
37
-

Bài giảng Tổng quan hoạt động quan trắc môi trường
 49 p |
49 p |  211
|
211
|  37
37
-

Bài giảng Giới thiệu TCVN ISO/IEC 17025 và định hướng áp dụng đối với hệ thống quan trắc môi trường
 62 p |
62 p |  252
|
252
|  32
32
-

Bài giảng Quan trắc môi trường: Bài 5 - Thái Vũ Bình
 62 p |
62 p |  122
|
122
|  26
26
-

Bài giảng Quan trắc môi trường: Bài 6 - Thái Vũ Bình
 47 p |
47 p |  138
|
138
|  26
26
-

Bài giảng Quản lý chất lượng môi trường trong nuôi trồng thủy sản: Phần 2
 152 p |
152 p |  143
|
143
|  21
21
-

Bài giảng Hệ thống quan trắc môi trường quốc gia
 47 p |
47 p |  130
|
130
|  14
14
-

Bài giảng Hệ thống văn bản, tài liệu liên quan đến hoạt động quan trắc môi trường
 23 p |
23 p |  113
|
113
|  8
8
-

Bài giảng Vật lý đại cương 1 (Trọn bộ công thức, bài tập trắc nghiệm, tự luận và đề thi)
 117 p |
117 p |  34
|
34
|  3
3
-

Bài giảng Quan trắc và đánh giá chất lượng nước và không khí: Chương 1 - Phạm Khắc Liệu
 37 p |
37 p |  32
|
32
|  2
2
-

Bài giảng Quan trắc và đánh giá chất lượng nước và không khí: Chương 2 - Phạm Khắc Liệu
 54 p |
54 p |  30
|
30
|  2
2
-

Bài giảng Quan trắc và đánh giá chất lượng nước và không khí: Chương 3 - Phạm Khắc Liệu
 90 p |
90 p |  32
|
32
|  2
2
-

Bài giảng Quan trắc và đánh giá chất lượng nước và không khí: Chương 4 - Phạm Khắc Liệu
 74 p |
74 p |  20
|
20
|  2
2
Chịu trách nhiệm nội dung:
Nguyễn Công Hà - Giám đốc Công ty TNHH TÀI LIỆU TRỰC TUYẾN VI NA
LIÊN HỆ
Địa chỉ: P402, 54A Nơ Trang Long, Phường 14, Q.Bình Thạnh, TP.HCM
Hotline: 093 303 0098
Email: support@tailieu.vn









