1
MỞ ĐẦU
1. Lý do chọn đề tài
Hiện nay vấn đề ô nhiễm không khí ở các thành phố lớn gây ra bởi các phương tiện giao thông chạy bằng
nhiên liệu hoá thạch ngày một trầm trọng do đó việc thay thế các phương tiện giao thông gây ô nhiễm bằng
các phương tiện thân thiện môi trường như xe điện (Evs), xe điện hybride (HEVs)... là rất cần thiết. Để có thể
sử dụng được trong xe điện, thì pin phải đáp ứng được những yêu cầu khắt khe như dung lượng lớn, thời gian
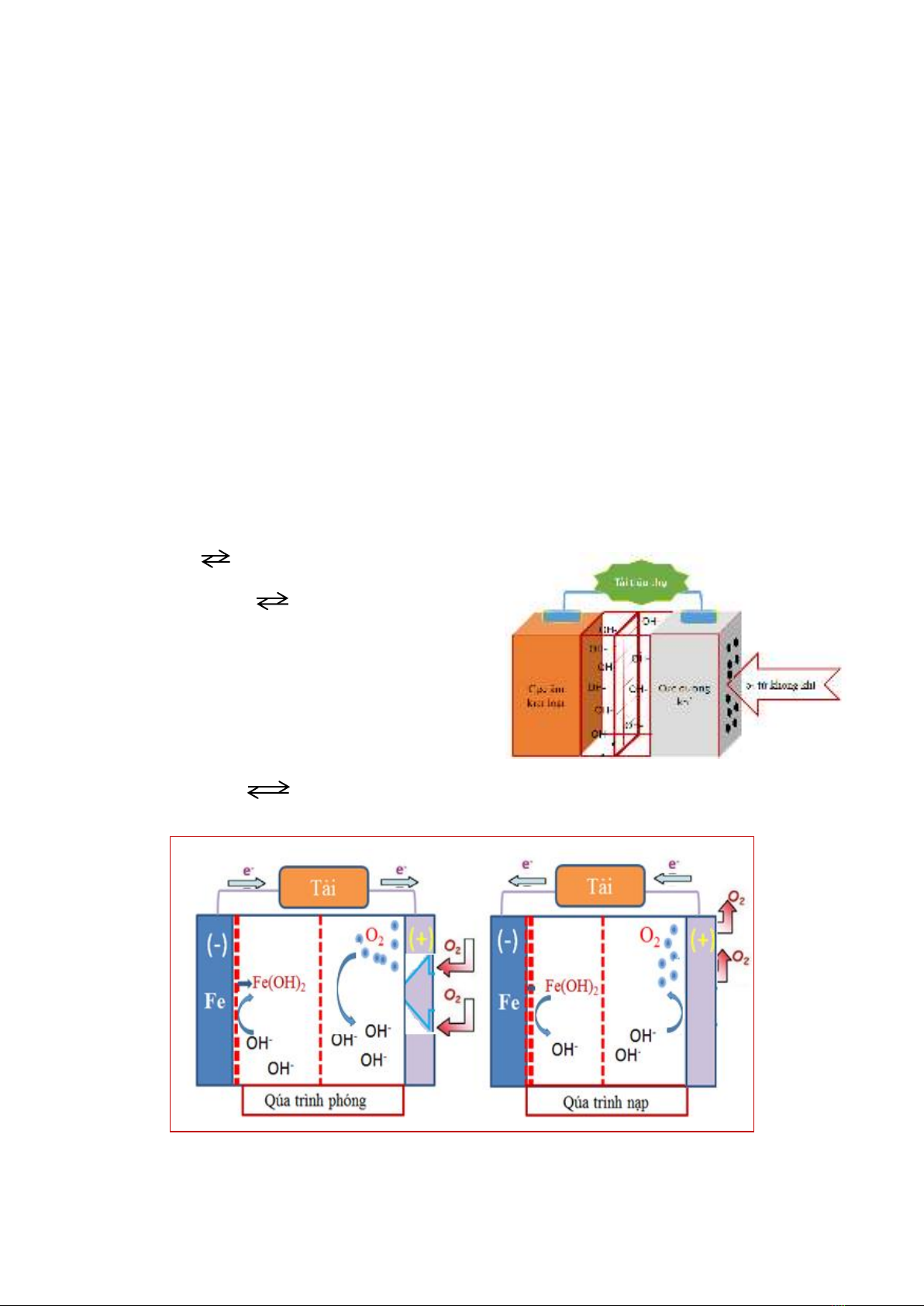
sống dài, sạc nhanh, nhỏ gọn, giá thành thấp, an toàn khi sử dụng, thân thiện môi trường… Pin Fe - khí là một
trong những loại pin tiềm năng nhất có thể đáp ứng được những yêu cầu nêu trên của xe điện do chúng nhiều
ưu điểm vượt trội như dung lượng và năng lượng lý thuyết cao, kim loại sắt có nhiều trên trái đất, an toàn khi
sử dụng, giá thành thấp. Do vậy trong khuôn khổ đề tài này chúng tôi đã tiến hành: “Nghiên cứu chế tạo vật
liệu composit oxit sắt/các bon định hướng ứng dụng trong tích trữ năng lượng” nhằm góp phần hạn chế của
loại pin này.
2. Mục tiêu của luận án
Tìm ra quy trình phù hợp nhất chế tạo vật liệu composit chứa ôxit sắt và các bon bằng phương pháp hóa
học và nghiền cơ học. So sánh vật liệu chế tạo bằng phương pháp hóa học và nghiền cơ học để tìm ra vật liệu
phù hợp nhất có thể ứng dụng trong pin Fe - khí.
Khảo sát các yếu tố ảnh hưởng đến đặc trưng điện hóa của điện cực composit Fe2O3/AB như tỷ lệ thành
phần Fe2O3 và các bon, hàm lượng chất kết dính, cấu trúc, hình thái học và kích thước hạt Fe2O3… từ đó tìm
ra được thành phần tối ưu, cấu trúc, hình thái học phù hợp nhất của Fe2O3 cho điện cực composit Fe2O3/AB.
Nghiên cứu chi tiết vai trò của chất phụ gia điện cực và phụ gia trong dung dịch điện ly để nâng cao
dung lượng, hiệu suất của điện cực composit Fe2O3/AB trong pin Fe - khí.
Tìm hiểu cơ chế của sự suy giảm dung lượng của điện cực Fe2O3/AB để từ đó tìm biện pháp khắc phục.
3. Phương pháp nghiên cứu
Tổng hợp vật liệu Fe2O3 có kích thước, hình thái học khác nhau bằng quy trình thủy nhiệt một bước và chế
tạo composit Fe2O3/AB bằng quy trình thủy nhiệt hai bước. Chế tạo vật liệu composit Fe2O3/AB bằng phương
pháp nghiền trộn sử dụng vật liệu thương mại để so sánh với vật liệu composit Fe2O3/AB chế tạo bằng quy
trình thủy nhiệt hai bước. Khảo sát cấu trúc, hình thái học của vật liệu chế tạo được bằng các phương pháp
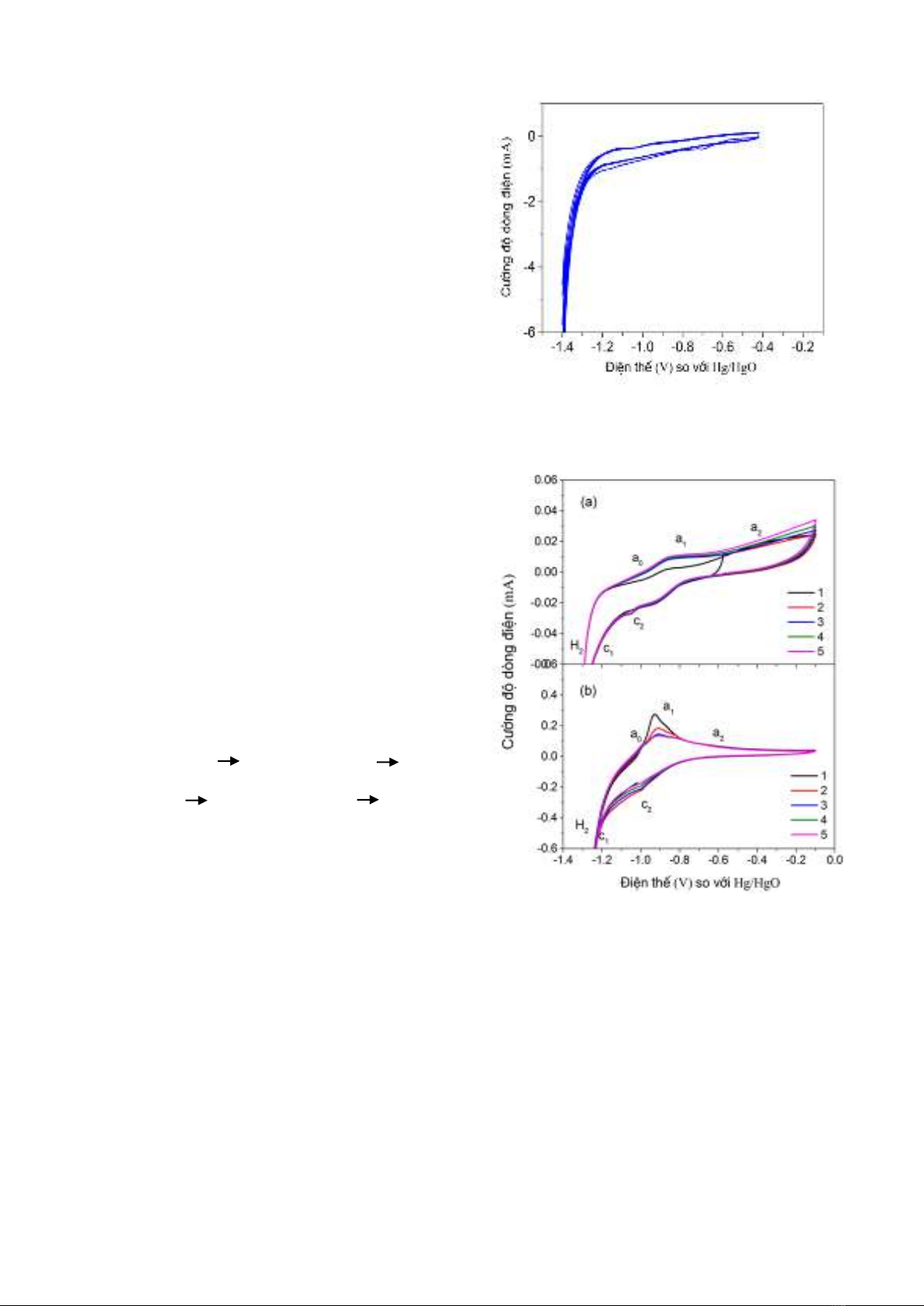
XRD, SEM, TEM, EDS. Khảo sát đặc trưng điện hóa của điện cực bằng các phép đo CV, phép đo đặc trưng
phóng - nạp (Galvanostatic cycling).
4. Các đóng góp của luận án
Tìm được quy trình tối ưu để chế tạo vật liệu Fe2O3 có thể điều khiển được kích thước, hình dạng
mong muốn để cho đặc trưng điện hóa tốt nhất.
Hoàn thiện quy trình chế tạo vật liệu composit chứa ôxit sắt và các bon với các tỉ lệ thành phần ôxit
sắt, các bon, chất kết dính, chất phụ gia tối ưu nhất.
Tìm được hàm lượng chất phụ gia điện cực, chất phụ gia dung dịch điện ly phù hợp nhất để điện cực
composit Fe2O3/AB cho dung lượng, hiệu suất cao nhất.