1
SỞ GIÁO DỤC VÀ
ĐÀO TẠO
QUẢNG NGÃI
KÌ THI CHỌN HỌC SINH GIỎI
CẤP TỈNH
MÔN HÓA HỌC LỚP 12 THPT
NĂM HỌC 2008-2009
(Đề gồm có 02 trang; thí sinh được sử dụng Bảng tuần hoàn
và máy tính cầm tay)
Câu 1. (4,0 điểm)
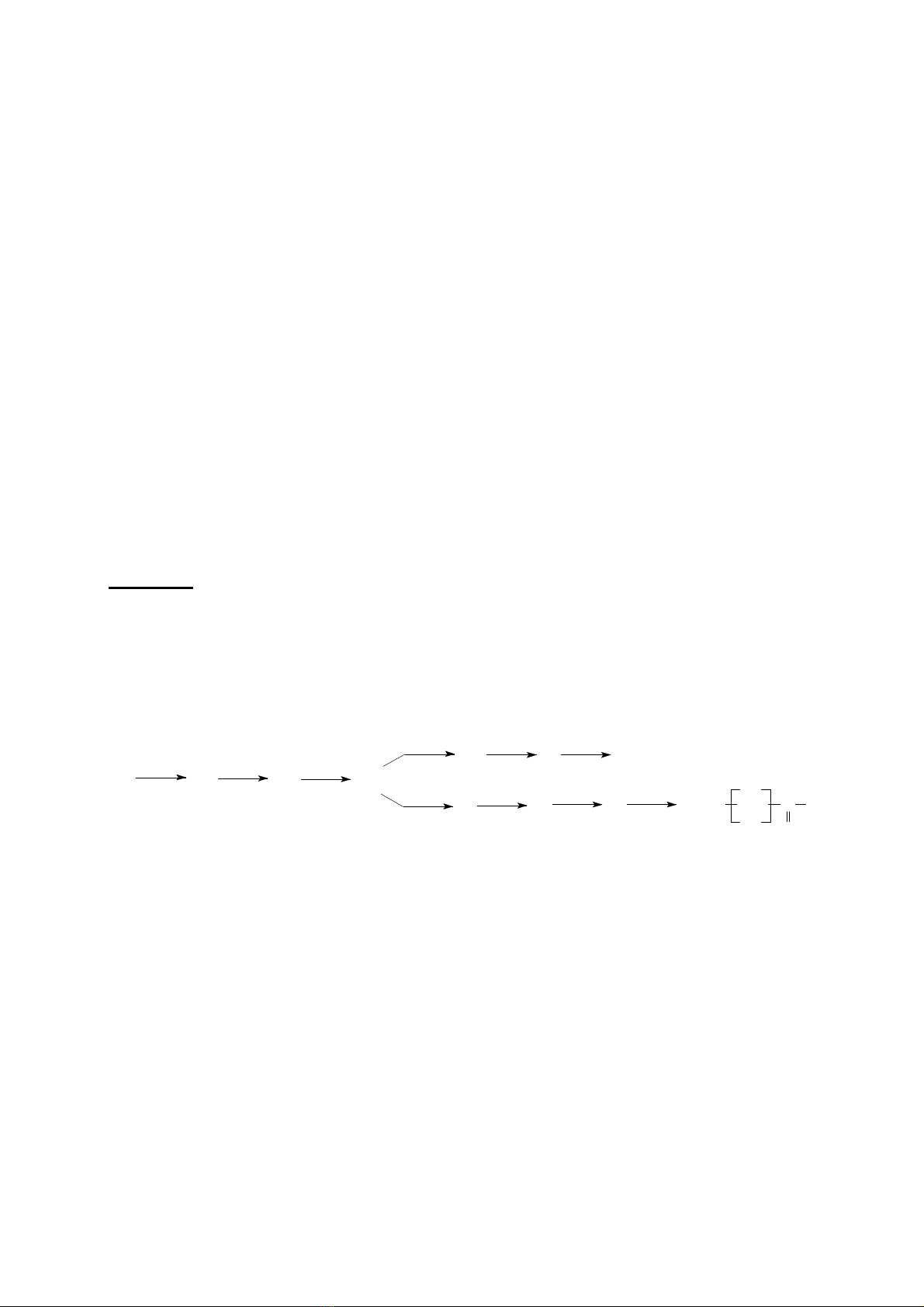
1. Viết phương trình phản ứng theo sơ đồ sau (các chất được
viết dưới dạng công thức cấu tạo).
XA B C
DEF
GH K O=HC CH2C
O
COOH
Cl2 (1 1)
:
(askt)
H2O
OH-
K2Cr2O7
H+
C6H5MgCl HNO3
HCN H2SO4O3
Zn/CH3COOH
H2O
H+
H2O
H+t04
2. Khi clo hoá C5H12 ở 100oC có chiếu sáng thu được các sản
phẩm với tỉ lệ % như sau:
2-clo-2-metylbutan: 28,4%; 1-clo-2-metylbutan:
24,4%;

2
3-clo-2-metylbutan: 35,0% ; 4-clo-2-metylbutan:
12,2%.
a. Viết phương trình phản ứng (dùng công thức cấu tạo)
và trình bày cơ chế phản ứng tạo ra một trong số các sản phẩm
trên.
b. Nếu thay clo bằng brom thì các tỉ lệ % trên biến đổi
như thế nào? Giải thích.
c. Tính khả năng phản ứng tương đối của H ở các nguyên
tử cacbon có bậc khác nhau.
3. So sánh lực bazơ của các chất trong dãy sau. Giải thích.
N
N
H
(X) CH3CH2CH2NH2. (Y) CH C - C
O
NH2
(Z) (T)
Câu 2. (3,0 điểm)
1. Chất X có công thức phân tử là C9H18O. X có phản ứng
iodofom; không có phản ứng cộng H2. Khi đun nóng X với
H2SO4 đặc ở 170oC thu được 2 chất hữu cơ Y, Z là đồng phân
của nhau và có công thức phân tử là C9H16. Y không có đồng
phân hình học. Oxi hoá Y bằng dung dịch KMnO4 đặc, đun
nóng rồi thực hiện phản ứng đề cacboxyl hoá thu được

3
etylxiclopentan. Z có thể tham gia phản ứng cộng với Br2
trong dung dịch theo tỉ lệ mol 1:1. Oxi hoá Z bằng dung dịch
KMnO4 đặc thấy có tạo thành CH3CH2CO[CH2]4COCH3.
Lập luận (không cần viết phương trình) để xác định công
thức cấu tạo của X, Y, Z và trình bày cơ chế tạo Y, Z từ X.
2. Một hợp chất hữu cơ A có công thức phân tử là C5H12O2 khi
oxi hóa cho một sản phẩm B là C5H8O2. Chất B có phản ứng
với hidroxylamin cho dioxim; tác dụng với I2 trong môi
trường kiềm cho iodofom và phản ứng được với thuốc thử Sip.
Lập luận (không cần viết phương trình) để suy ra công thức
cấu tạo của A.
Câu 3. (3,0 điểm)
1. Viết phương trình phản ứng khi cho axit aminoaxetic lần
lượt tác dụng với: Dung dịch NaOH, dung dịch H2SO4, CH3I,
metanol/HCl bão hòa, CH3COCl, NaNO2/dung dịch HCl,
Cu(OH)2.
2. Viết phương trình phản ứng xảy ra khi nhiệt phân các amino
axit mạch không phân nhánh có công thức phân tử là
C4H9O2N.

4
3. Trộn một hidrocacbon là chất khí ở điều kiện thường (A)
với O2 theo tỉ lệ thể tích VA : VO2 = 1 : 9 (cùng điều kiện) rồi
cho vào bình kín thấy áp suất trong bình là 1 atm ở 0oC. Bật
tia lửa điện để A cháy hết, hỗn hợp khí và hơi sau phản ứng có
áp suất là 1,575 atm ở 136,5oC. Xem thể tích bình không đổi.
a. Tìm công thức phân tử của A.
b. Chọn cấu dạng A ở trên cho phù hợp để từ A và các
chất vô cơ cần thiết điều chế chất C có công thức cấu tạo:
Câu 4. (3,0 điểm)
1. Trộn các dung dịch sau đây với thể tích bằng nhau: CuSO4
1,5M; FeSO4 0,075M; Fe2(SO4)3 0,375M; thu được dung dịch
A (xem thể tích dung dịch không đổi). Thêm vào dung dịch A
một ít mảnh kim loại Cu.
a. Cho biết chiều của phản ứng. Tính hằng số cân bằng
của phản ứng.
b. Tính tỉ lệ 3
2
Fe
Fe
để phản ứng đổi chiều.

5
Cho 2
0
/
0,34( )
Cu Cu
E V
; 3 2
0
/
0,77( )
Fe Fe
E V
.
2. Nêu hiện tượng xảy ra và viết các phương trình phản ứng
(nếu có) khi:
a) Cho Fe3O4 tác dụng với dung dịch HI dư.
b) Cho kim loại Al vào dung dịch hỗn hợp gồm KNO3 và
KOH.
c) Cho dung dịch H2SO4 loãng vào dung dịch Fe(NO3)2.
d) Cho muối natri axetat vào dung dịch K2Cr2O7.
Câu 5. (3,0 điểm)
Hợp chất A có dạng M3X2. Khi cho A vào nước, thu được kết
tủa trắng B và khí C là một chất độc. Kết tủa B tan được trong
dung dịch NaOH và dung dịch NH3. Đốt cháy hoàn toàn khí C
rồi cho sản phẩm vào nước dư, thu được dung dịch axit D.
Cho D từ từ vào dung dịch KOH, phản ứng xong thu được
dung dịch E chứa 2 muối. Dung dịch E phản ứng với dung
dịch AgNO3 cho kết tủa màu vàng F tan trong axit mạnh.








![Đề thi học sinh giỏi Quốc gia THPT môn Hoá học năm 2021-2022 có đáp án [Kèm đề thi]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230215/bapnuong09/135x160/2931676452944.jpg)













![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



