
A.HIÑROÂCACBONNO
I)Ankan(Parafin) CnH2n+2 (n
1)
1)Caùch goïi teân: soá chæ vò trí-teân nhaùnh + teân maïch chính + an.
Löu yù: Ñaùnh soá thöù töï phaûi ñaùnh töø vò trí coù gaàn noái ñoâi nhaát.
Ví duï
1 2 3 4
3 2 3
|
3
CH CH CH CH
CH
2- metylbutan (isopentan)
3
|
1 2 3 4 5
3 2 2 3
|
3
CH
CH CH CH CH CH
CH
2,2- ñimetyl pentan (neoheptan)
2)Tính chaát hoaù hoïc.
*Phaûn öùng theá:
CH4 + Cl2 askt
CH3Cl + HCl
*Phaûn öùng taùch H2
2CH4 0
1500 C
lln
C2H2 + 2H2
* Phaûn öùng oxi hoaù
CnH2n+2 +
3n 1
2
O2 0
t
nCO2 + (n+1)H2O
+Phaûn öùng oxi hoaù khoâng hoaøn toaøn: CH4 + O2 0
t ,xt
HCHO + H2O
II)Xicloankan CnH2n (n
3)
CH3
| CH3
1,2,4-Trimetylxiclohexan
|
CH3
*Tính chaát hoaù hoïc
a) phaûn öùng coäng môû voøng.
+ H2 0
Ni,80 C
C3H8
+ Br2
Br
CH2
CH2
CH2
Br (1,3-ñibrompropan)
+ HBr
CH3
CH2
CH2
Br
+ H2 0
Ni,120 C
C4H10 (Butan)
b)Phaûn öùng theá Br
+ Br2 0
t
+ HBr
c) Phaûn öùng oxi hoaù
Haõy hoïc vì
töông
lai cuûa moãi chuùng
ta vàconchúngta.

2 | Nguyễn Hoàng Linh Tel:01689107184
CnH2n +
3n
2
O2 0
t
nCO2 + nH2O
* Ñieàu cheá
CH3
CH2
CH2
CH2
CH2
CH3 0
t ,xt
+ H2
0
t ,xt
C6H6 + 3H2
B.Hidrocacbon khoâng no
I)Anken (olefin) coù ñoàng phaân hình hoïc [cis(cuøng), trans( khaùc)]
1)Danh phaùp CnH2n (n
2)
Soá chæ vò trí –teân nhaùnh + teân maïch chính – soá vò trí noái 2 – en
Vd:
1 2 3 4
2 2 3
|
3
CH C CH CH
CH
2–metylbut–1–en
2) Tính chất hoá học
a) Phản ứng cộng.
CH2=CH2+H2 0
t ,xt
CH3
CH3
2 2 2 2 2
| |
CH CH Cl CH CH
Cl
Cl
1,2- đicloetan
2 2
| |
2 2 2
CH CH
CH CH Br
BrBr
1,2- đibrometan
C2H4+HCl 0
t ,xt
CH3CH2Cl
C2H4+H-OH 0
t ,xt
CH3CH2OH
b)Phản ứng trùng hợp
n
2 2 3
|
3
CH C CH CH
CH
0
t ,xt,P
2 2 3
|
3
CH C CH CH
CH
n
c)Phản ứng oxi hoá không hoàn toàn.
3CH2=CH2+ 2KMnO4 + 4H2O
3
2 2
| |
CH CH
OHOH
+ 2KOH + 2MnO2
3
2 2 3
|
3
CH C CH CH
CH
+ 2KMnO4 + 4H2O
3
2 2 3
| |
CH C CH CH
OHOH
+ 2KOH + 2MnO2
3)Điều chế
CH3CH2OH 0
2 4
H SO ,170 C
C2H4+H-OH
II)Ankadien (CnH2n-2) có hai liên kết đôi trong phân tử.
1) Phân loại+ankađienliênhợpcáchnhaumộtliênkếtđơn.
+ankađiencáchnhauhainốiđôitrởlên.
2) Phản ứng hoá học
a. Phản ứng cộng
CnH2n-2 + 2H2 0
t ,Ni
CnH2n+2
0
80 C
2
+Br
2 2
CH CH CH CH | |
BrBr
2 2
CH CH CH CH
Haõy hoïc vì
töông lai cuûa
moãi chuùng ta và
conchúngta.
3 | Nguyễn Hoàng Linh Tel:01689107184
0
80 C
+HBr
2 2
CH CH CH CH | |
HBr
2 2
CH CH CH CH
b. Phản ứng trùng hợp
0
t ,xt,p
n
n C C
2 2 2 2
CH CH CH CH H H CH CH
n
2 2
|
3
CH C CH CH
CH
02 2
t ,xt,p |
3
n
CH C CH CH
CH
3) Điều chế ứng dụng của butađien & isopropen
TrongCNhiệnnaybutađien&isopropenđượcđiềuchếbằngcáchtáchH2từankan
CH3−CH2−CH2−CH3 0
t ,xt,P
2 2
CH CH CH CH
+ 2H2
2 2 2
|
3
CH CH CH CH
CH
0
t ,xt,P
2 2
|
3
CH C CH CH
CH
+ 2H2
III. Ankin CnH2n-2 (n
2)
1. Danh pháp: cũnggọinhưankenchỉthayđuôienthànhđuôiin.
2. Tính chất hoá học.
a. Phản ứng cộng:
Cộng H2
C2H2+H2 0
t ,Ni
C2H6
C2H2+H2 3
Pd,PbCO
C2H4
Cộng Br2
CH3CCCH3+Br2 0
20 C
3 3
CH C C CH
BrBr
| |
CH3CCCH3+Br2
3 3
BrBr
CH C C CH
BrBr
| |
| |
Cộng H2O
CHCH+HOH 4 2 4
0
HgSO ,H SO
80 C
CH3CHO
Cộng HCl
CHCH+HCl 2
0
HgCl
t
CH2=CHCl(Vinylclorua)
b. Phản ứng đime hoá và phản ứng trime hoá:
CHCH 0
t ,xt
CH2=CHCCH(Vinylaxetilen)
CHCH 0
600 C,BôtC
C6H6 ( Benzen)
c. Phản ứng thế bằng ion kim loại (đây là phản ứng để nhận biết ankin có nối ≡
đầu mạch):
CHCH+2AgNO3+2NH3
AgCCAg(vàng) + 2NH4NO3
(Bạcaxetilua)
d. Phản ứng oxi hoá:đốt cháy và làm mất màu thuốc tím (KMnO4)
CnH2n-2 +
3n 1
2
O2 0
t
n CO2 + (n-1)H2O
Haõy hoïc vì töông
lai cuûa moãi
chuùng ta vàcon
chúngta.
4 | Nguyễn Hoàng Linh Tel:01689107184
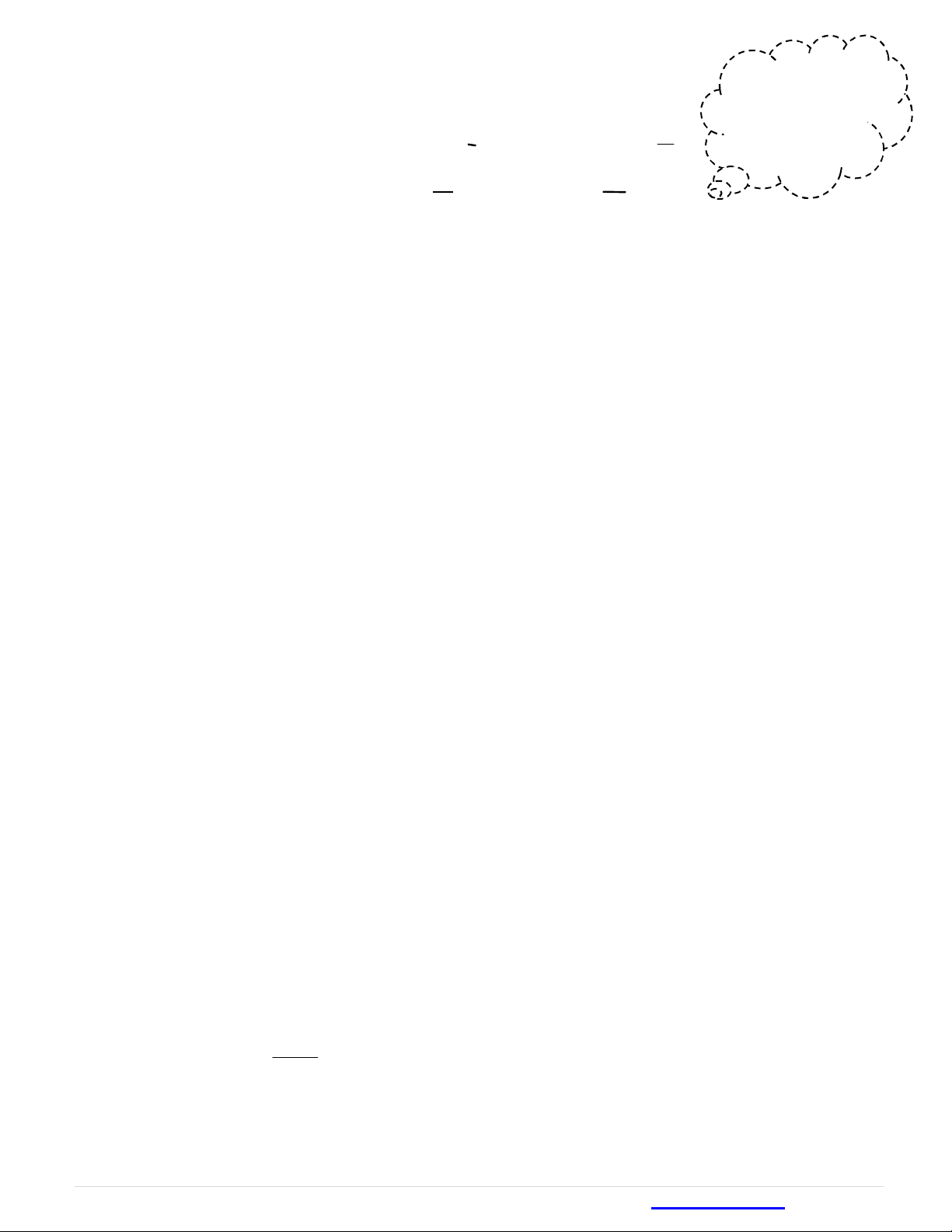
C. Hiđrôcacbon thơm
I) Benzen và ankyl benzen
1)Đặc trưngcómạchvòngcó6cạnhcó3liênkếtđơnxenkẻ3liênkếtđôi.
CTTQ CnH2n-6 (n6)
2) Tính chất hoá học
a) Phản ứng thế Br
+ Br2 bôtFe
+ HBr
C6H5CH3 + Br2 bôtFe
C6H5BrCH3 + HBr
C6H5CH3 + Br2 áskt
C6H5CH2Br + HBr
C6H6 + HNO3 2 4
H SO
đ C6H5NO2 + H2O
b) Phản ứng cộng .
C6H6 + H2 0
t ,Ni
C6H12
C6H6 + Cl2 áskt
C6H6Cl6
c) Phản ứng oxi hoá.
C6H5CH3 + 2KMnO4 0
t
C6H5COOK + 2MnO2 + KOH + H2O
CnH2n-6 + 3n
3
2
O2 0
t
nCO2 + (n-3)H2O
3) Điều chế
CHCH 0
600 C,BôtC
C6H6 ( Benzen)
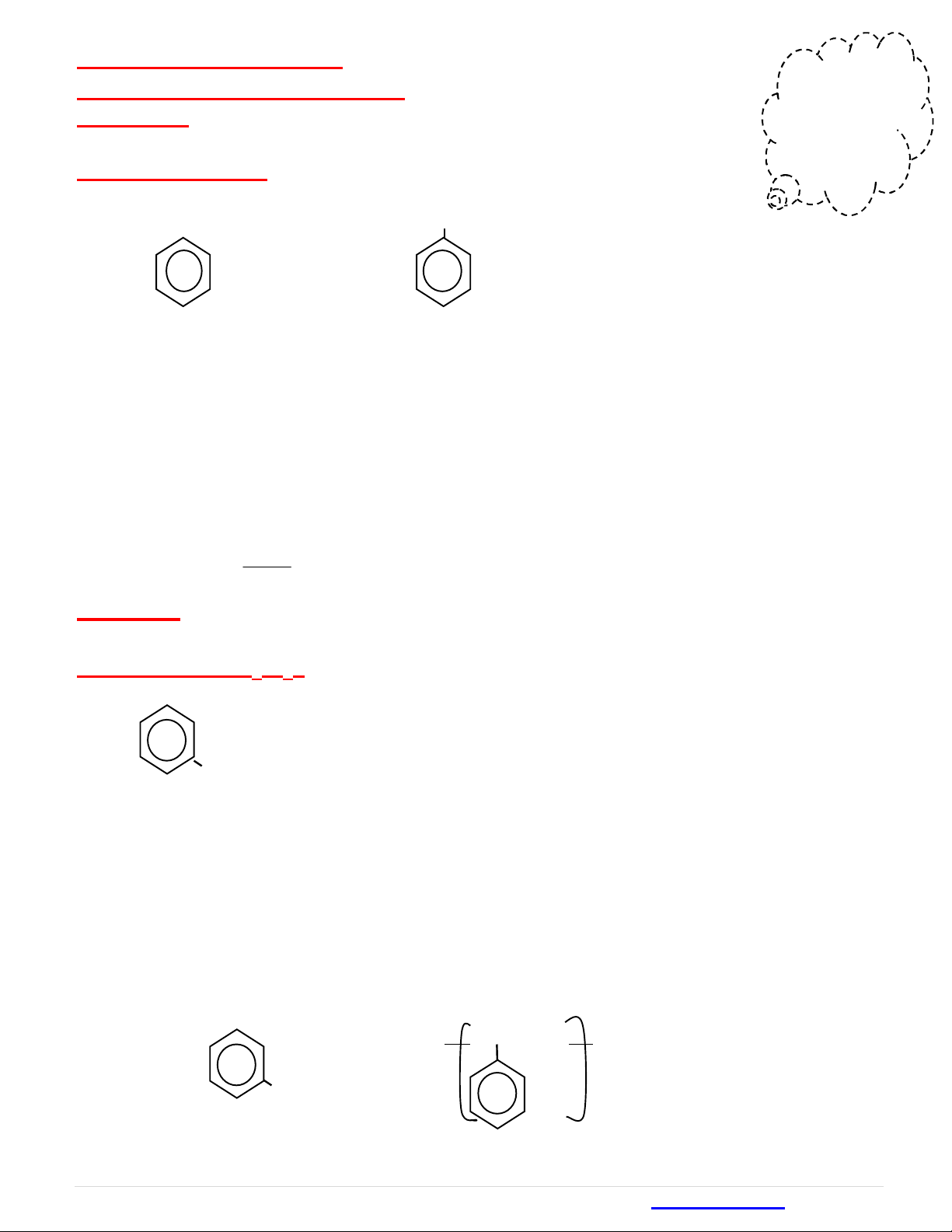
II) STIREN (C8H8)
1) Đặc trưng: cómộtvòngbenzenliênkếtvớinhómvinyl(CH=CH2)
CH=CH2
2) TÍNH CHẤT HOÁ HỌC
a. Phản ứng cộng
C6H5CH=CH2 + Br2
6 5 2
| |
C H CH CH
Br Br
C6H5CH=CH2 + HCl
6 5 3
|
C H CH CH
Cl
C6H5CH=CH2 + H2 0
t ,xt,p
6 5 2 3
C H CH CH
C6H5CH=CH2 + 4H2 0
t ,xt,p
6 2 3
C H CH CH
11
b. Phản ứng trùng hợp
CH-CH2
n 0
t ,xt,p
(polistiren)
CH=CH2
n
c. Phản ứng oxi hoá
Haõy hoïc vì
töông lai cuûa
moãi chuùng ta
vàconchúng
ta.
5 | Nguyễn Hoàng Linh Tel:01689107184
CH=CH2CH(OH)-CH2(OH)
+2KMnO4+4H2O
+2MnO2 (đen) + 2KOH
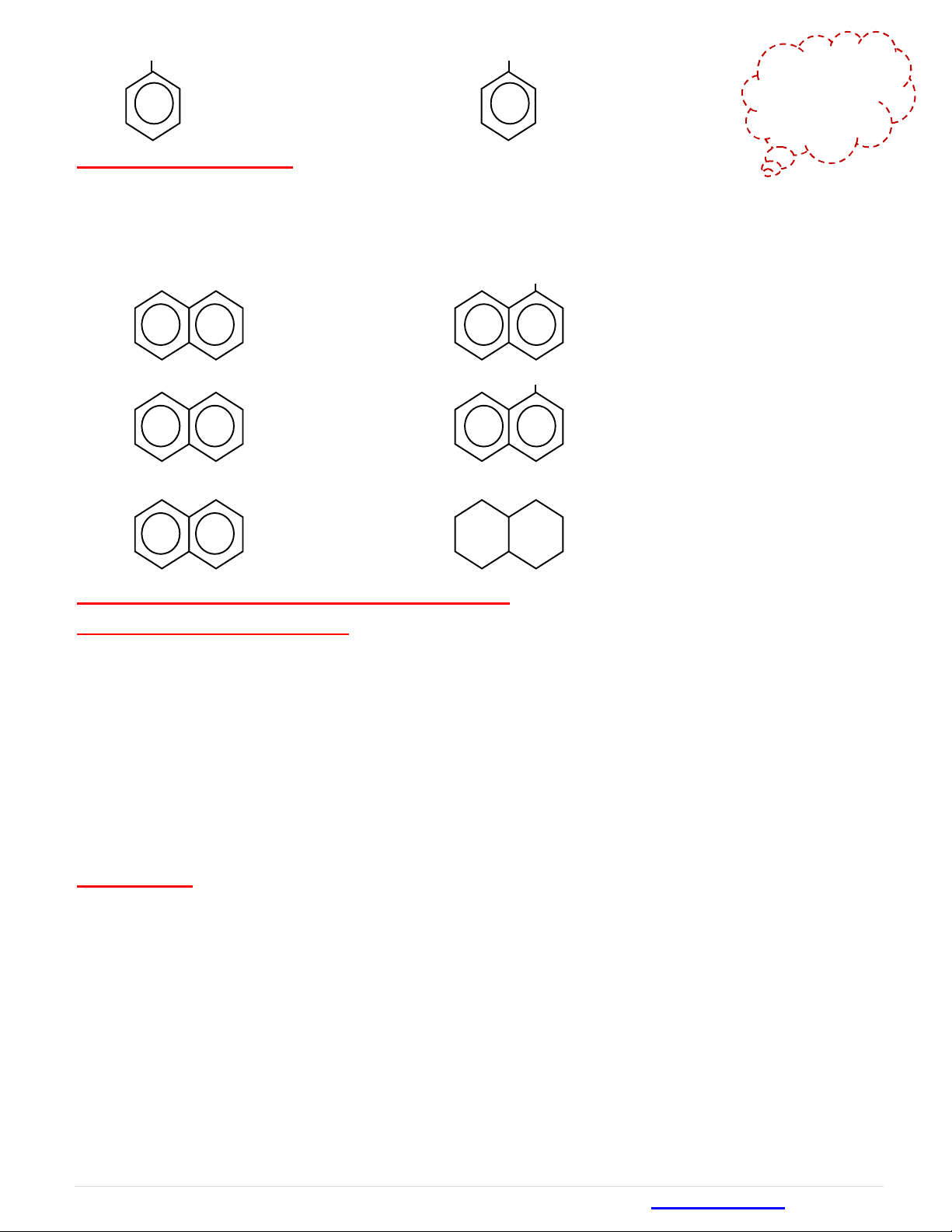
III) NAPHTALEN (C10H8)
1. Đặc trưng: cóhaivòngbenzen,dễthănghoangayởnhiệtđộthường.
2. Tính chất hoá học:
a. Phản ứng thế
Br
+Br2 3
CH COOH
+ HBr
NO2
+HNO3 2 4
H SO ,d
+ H2O
b. Phản ứng cộng H2
+5H2
0
Ni,t
(C10H18)
D. DẪN SUẤT CỦA HIĐRÔCACBON
I. DẪN XUẤT HALOGEN
1) Phản ứng thế nguyên tử X bằng nhóm (–OH)
CH3-CH2-CH2-Cl+NaOH
0
t
CH3-CH2-CH2-OH+NaCl
(ancolpropylic)
2) Phản ứng tách hiđrôhalogenua
CH3-CH2-CH2-Br+KOH
0
2 5
C H OH,t
CH3-CH=CH2+KBr+H2O
3) Phản ứng với Mg.
CH3-CH2-CH2-Br+Mg khan
ete
CH3-CH2-CH2-Mg-Br
(etylmagiebromua)
II.ANCOL
1. Danh pháp: tên hiđrôcacbon ứng với mạch chính + số chỉ vị trí nhánh + ol
Ví dụ:
4 3 2 1
3
3 2 |
C H C H C H C H
OH
butan-2-ol
3 2 1
3
C
3 2
|
C H C H H OH
CH 2-metyl propan-1-ol
2. Tính chất hoá học
a. Phản ứng thế với kim loại kiềm
2C2H5OH + 2Na
2C2H5ONa + H2
Haõy hoïc vì
töông lai cuûa
moãi chuùng ta
vàconchúng


















![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



