
Ph n 1: C u t o nguyên tầ ấ ạ ử
Khái ni m nguyên tệ ử
Th i c Hi L p: các ch t đ u c u t o t nh ng ph n t r t nh g i ờ ổ ạ ấ ề ấ ạ ừ ữ ầ ử ấ ỏ ọ
là “atomos” – không th chia nh h n đ c.ể ỏ ơ ượ
Đ n gi a th k XIX: các ch t đ u đ c t o nên t nh ng h t c c ế ữ ế ỉ ấ ề ượ ạ ừ ữ ạ ự
kì nh bé không th phân chia đ c n a, g i là ỏ ể ượ ữ ọ nguyên tử.
Cu i th k XIX, đ u th k XX: th c nghi m ch ng minh nguyên t ố ế ỉ ầ ế ỉ ự ệ ứ ử
có th t và c u t o ph c t p.ậ ấ ạ ứ ạ
→ Đ nh nghĩa m i:ị ớ nguyên t là nh ng h t c c kì nh bé và không ử ữ ạ ự ỏ
th phân chia trong ph n ng hóa h c thông th ng.ể ả ứ ọ ườ
TR N M NH C NGẦ Ạ ƯỜ
I. Thành ph n c u t o c a nguyên tầ ấ ạ ủ ử
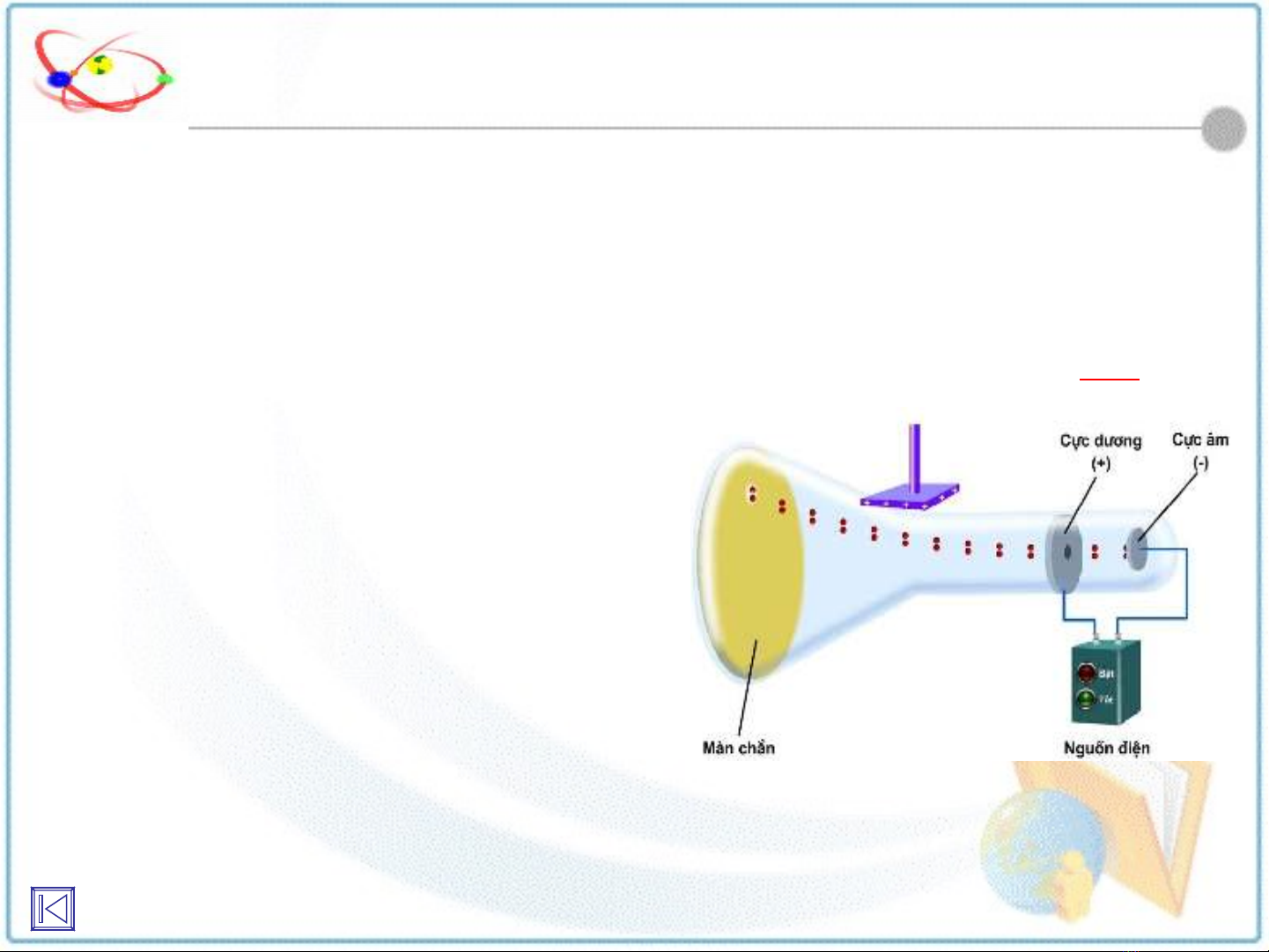
•Phóng đi n hi u đi n th r t l n qua 2 ệ ệ ệ ế ấ ớ
đi n c c g n vào đ u ng kín rút g n h t ệ ự ắ ầ ố ầ ế
không khí, th y màn huỳnh quang trong ấ
ng th y tinh phát sáng → có 1 chùm tia ố ủ
không nhìn th y đ c đi t c c âm đ n ấ ượ ừ ự ế
c c d ng (g i là tia âm c c).ự ươ ọ ự
•Tia âm c c l ch h ng v phía c c ự ệ ướ ề ự
d ng khi đ t ng th y tinh trong đi n ươ ặ ố ủ ệ
tr ng → tia âm c c là chùm h t mang ườ ự ạ
đi n tích âm.ệ
1. S tìm ra electronự
Năm 1897, Thomson phát hi n ra tia âm c c mà b n ch t là các chùm h t ệ ự ả ấ ạ
nh bé mang đi n tích âm g i là electron (e).ỏ ệ ọ
Mô t thí nghi m phát hi n c a Thomson:ả ệ ệ ủ TN1
TR N M NH C NGẦ Ạ ƯỜ





![Bài giảng Cấu tạo vật thể ThS. Nguyễn Hoàng Thông [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250707/nguyenhoangthong.hui@gmail.com/135x160/197_bai-giang-cau-tao-vat-the-ths-nguyen-hoang-thong.jpg)
















![Đề thi học kì 2 môn Vật lí 1 năm 2023-2024 có đáp án [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/64291778553454.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2023-2024 có đáp án [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/1381778553461.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2022-2023 có đáp án [kèm PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/21778553462.jpg)




